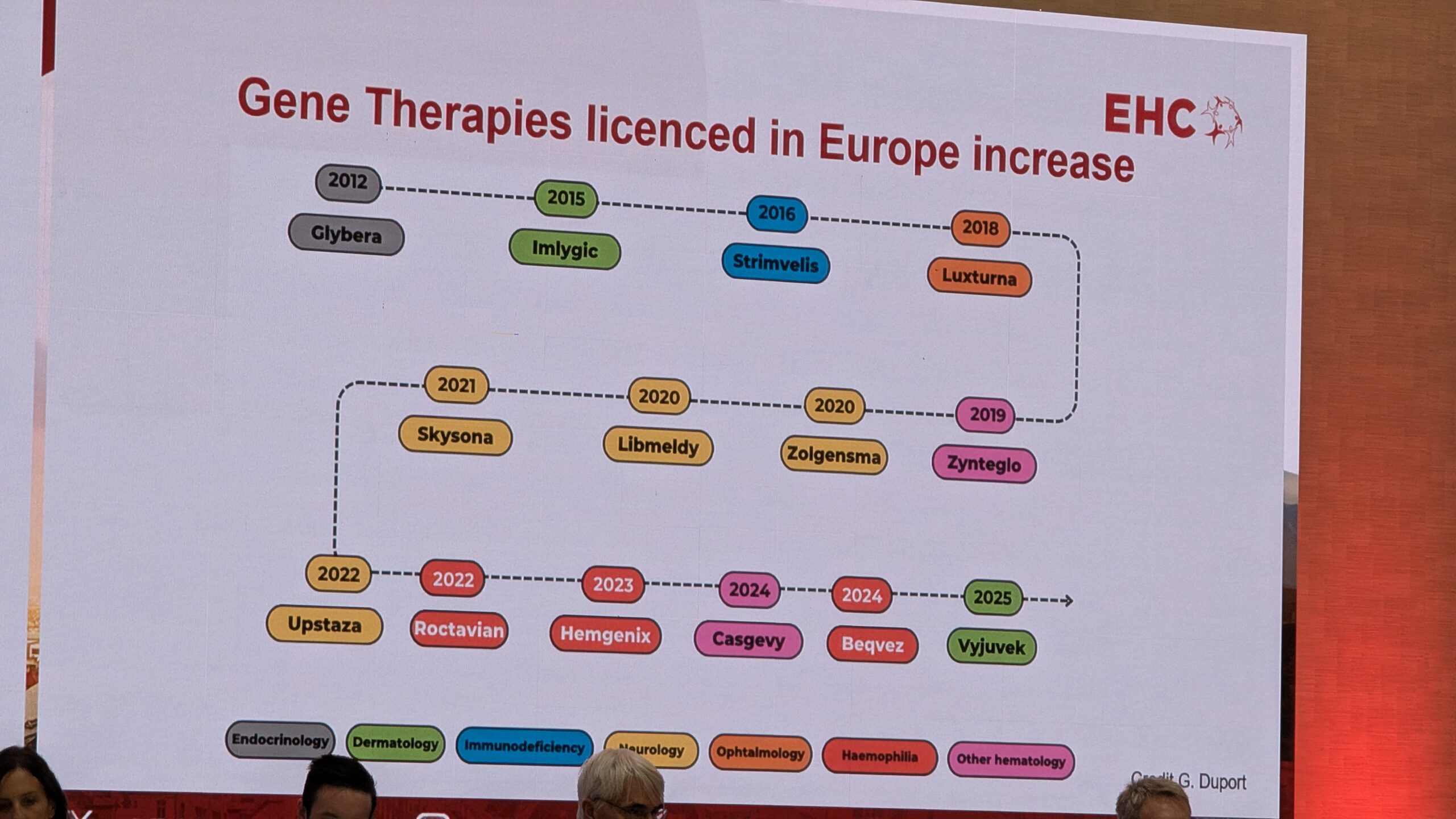
Oktoobris toimus Viinis Euroopa Hemofiilia Konsortsiumi (EHC) 2025 aasta Kongress.
EHC kongress koondab patsientide liikmesorganisatsioone (NMO), nende esimehi, tervishoiutöötajaid, teadlasi, poliitikakujundajaid ja valdkonna eksperte.
Konverentsi eesmärk oli jagada viimaseid teadustulemusi ja edendada kogukonna koostööd.
Konverentsi loengud tutvustasid edusamme ravis, uuringutulemusi ja rõhutati sotsiaalsete vajaduste tähtsust. Samaaegselt tugevdati sotsiaalsete üritustega kogukonna koostööd. Eesmärgiks toodi vajadus parandada veritsushäiretega inimeste elukvaliteeti, selleks toodi arutellu uued ravivõimalused ja tutvustati uusi teaduse arenguid Euroopas.
Esitletud ettekannetes, räägiti veritsushäiretega patsientide ravist, diagnostikast ning psühhosotsiaalse käsitluse edusammudest ja väljakutsetest.
Konverentsi peamine eesmärk oli anda üheltpoolt ülevaade viimastest teaduse saavutustest ja teisalt püüti seda siduda kogukonnakeskse veritsushäirete käsitluse visiooniga.
Põhiprogrammis räägiti uutest ja vanadest ravimitest, multidistsiplinaarsuse ja vajalike tervishoiuteenuste osutamise tähtsusest, Juhiti tähelepanu haruldastele veritsushäiretele (nt fibrinogeeni puudulikkus ja BDUC – veritsushäired teadmata põhjusega), SLAM-meetoditest (Scientific, Leadership, Advocacy, Management) ning arutati traditsiooniliselt EHC noorte probleeme.
Arutati järgmisi olulisi valdkondi:
- Ravi innovatsioon ja tulevik:
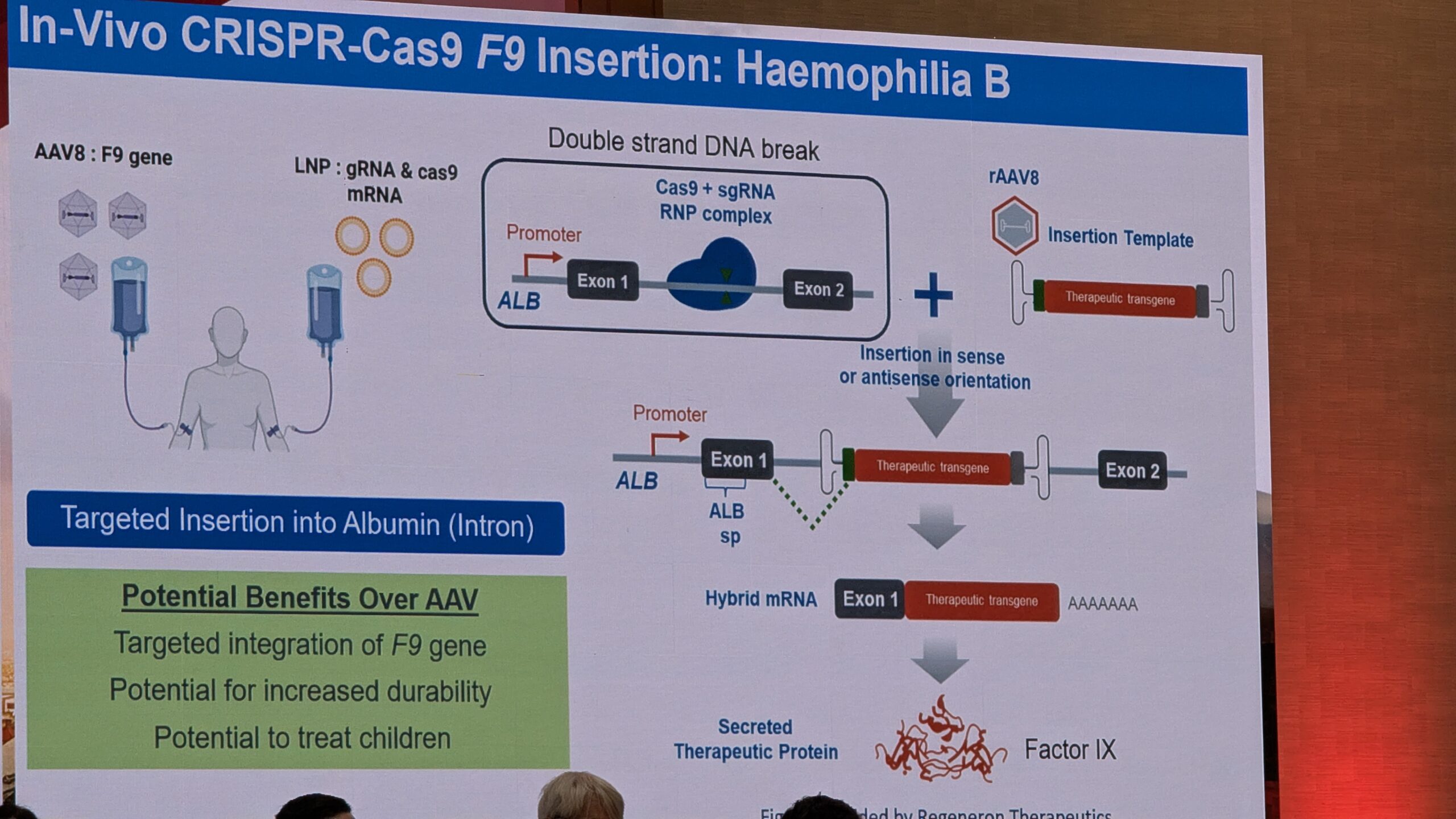
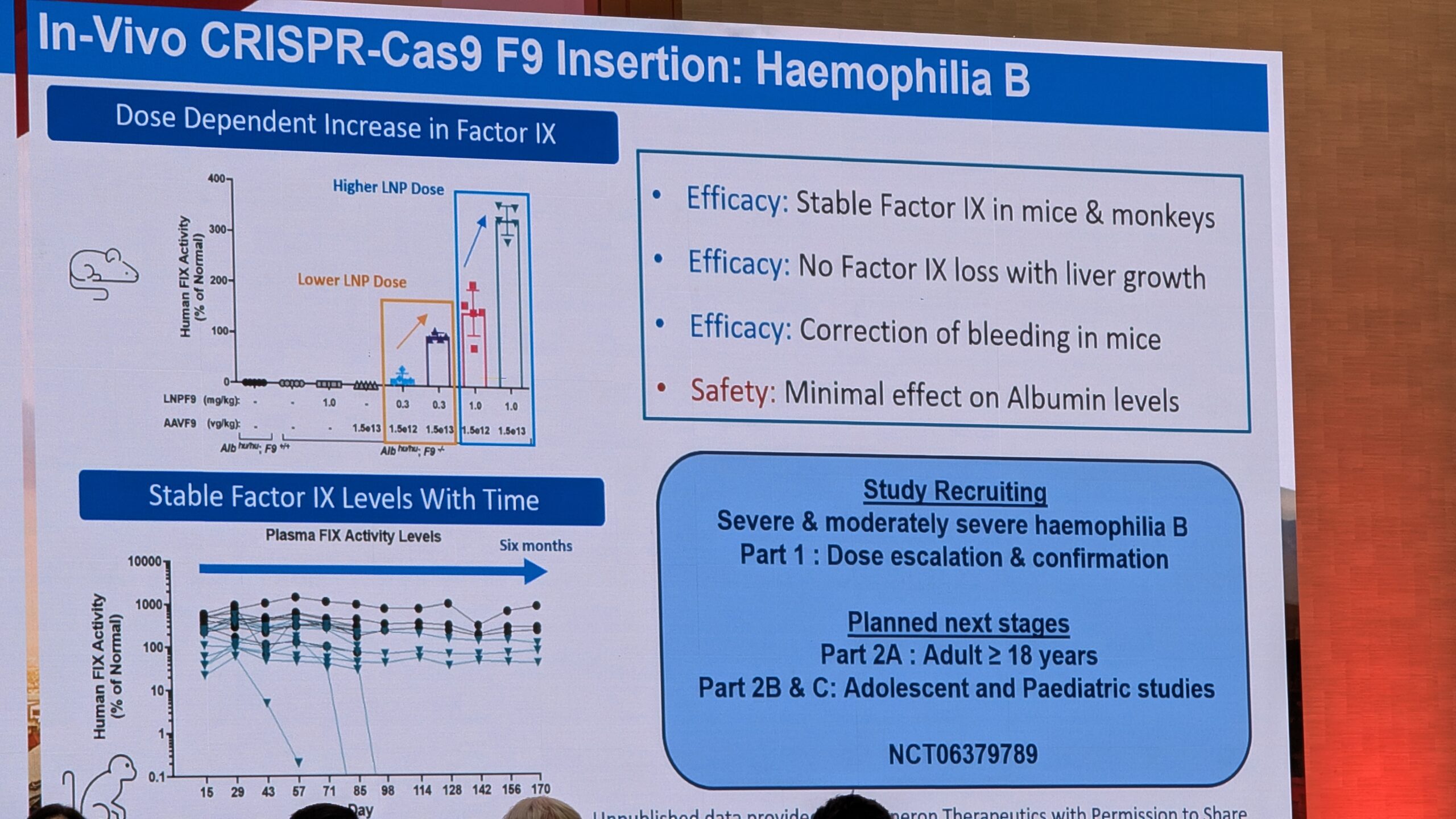
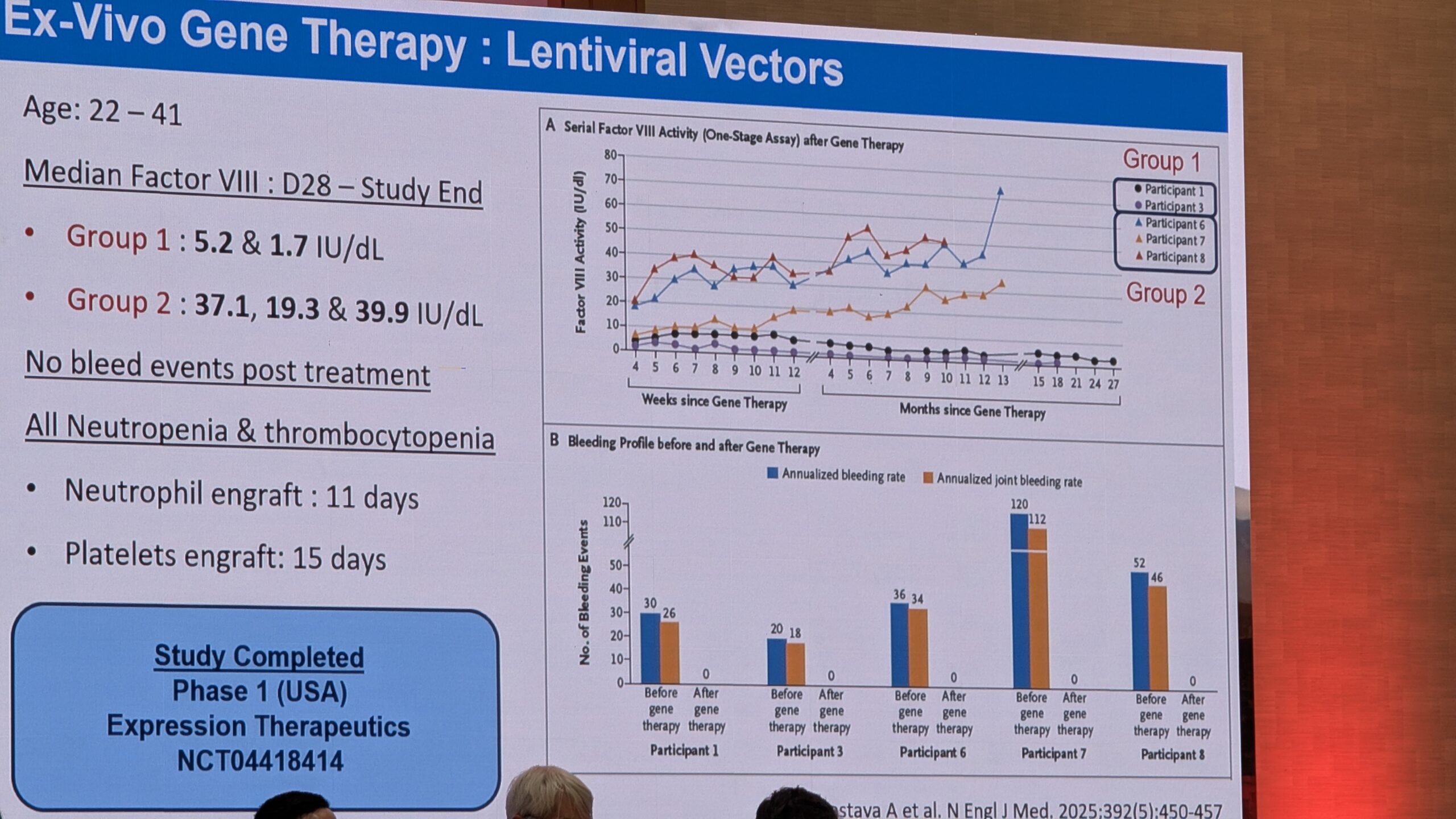
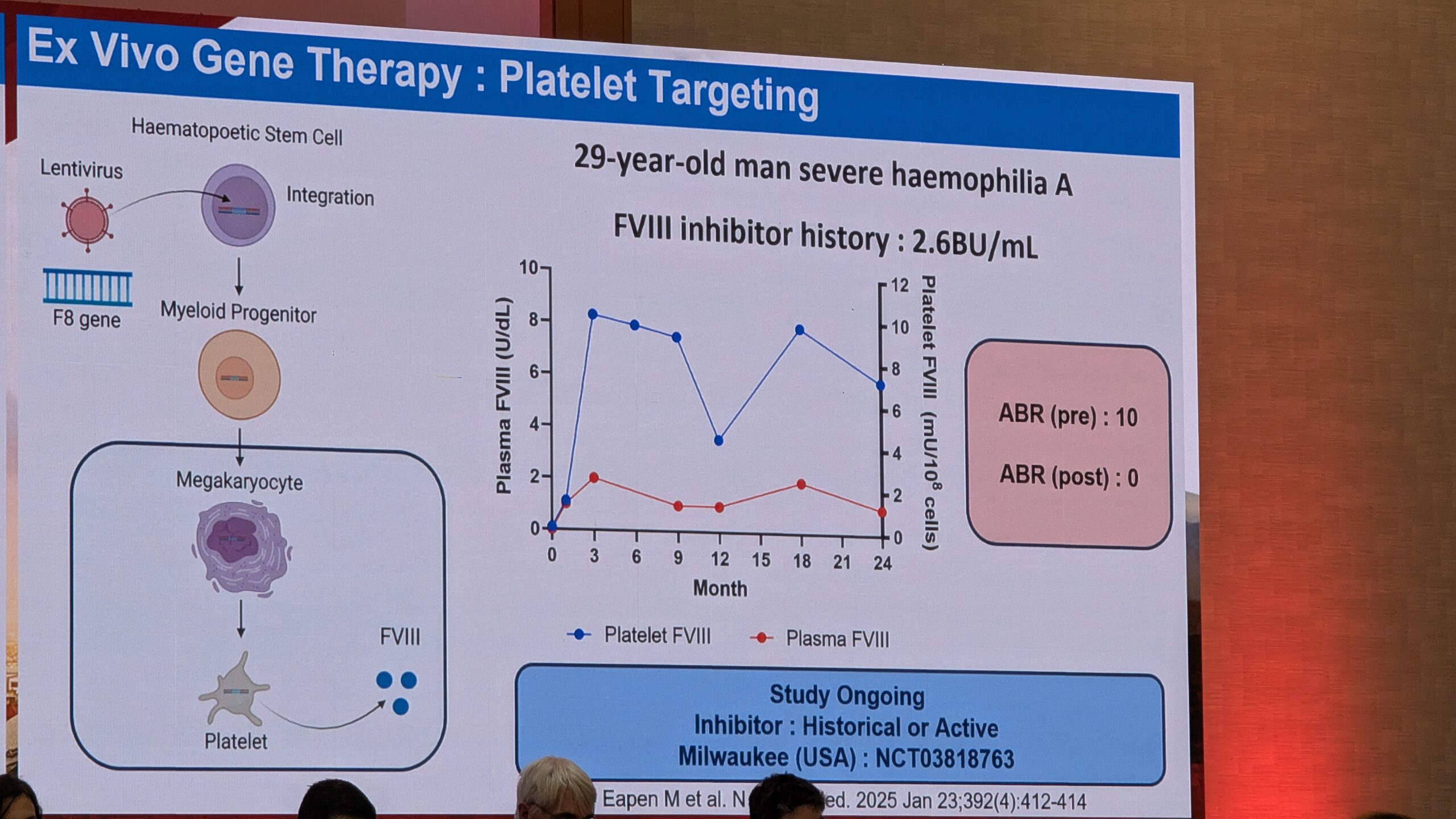
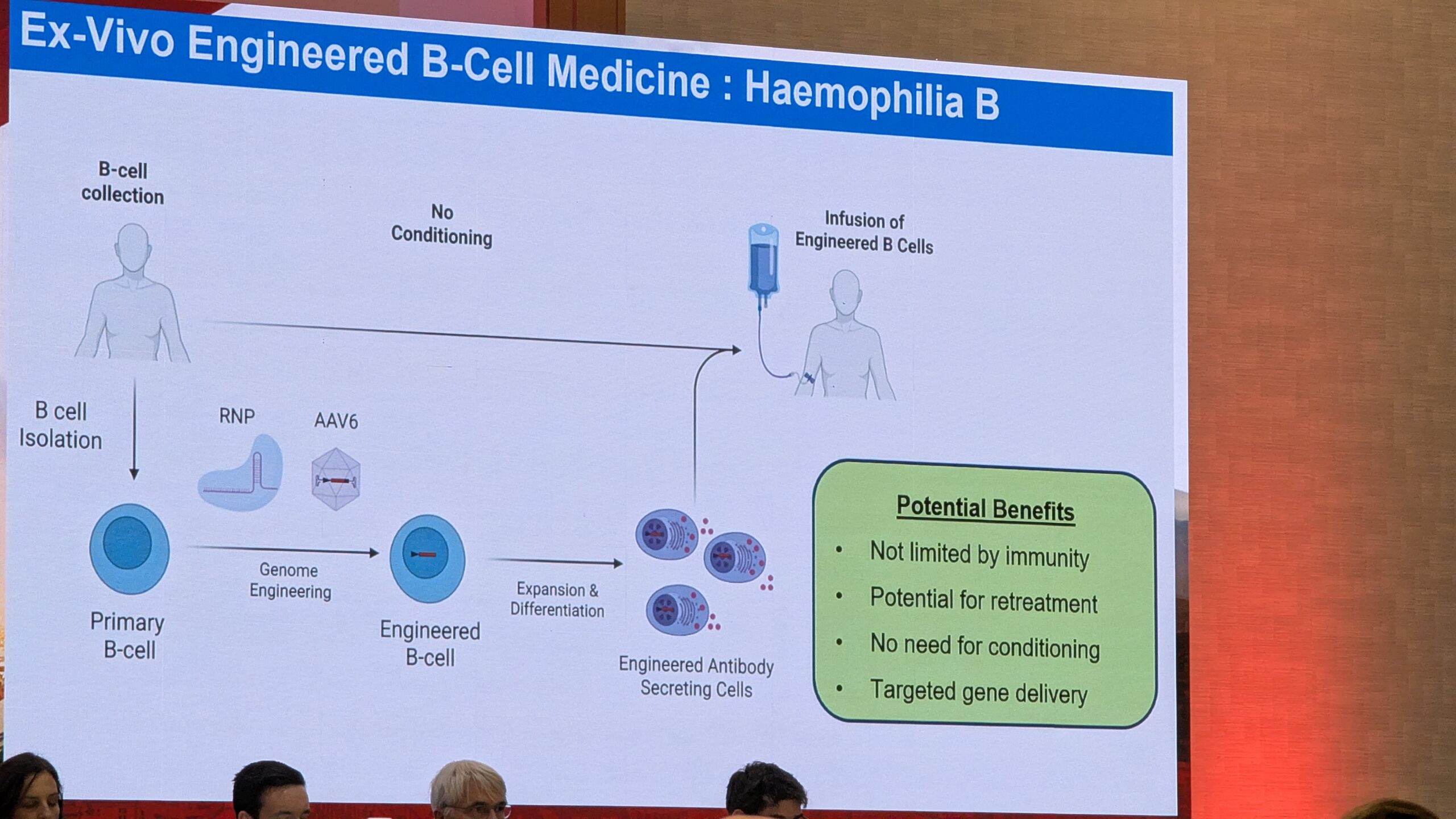
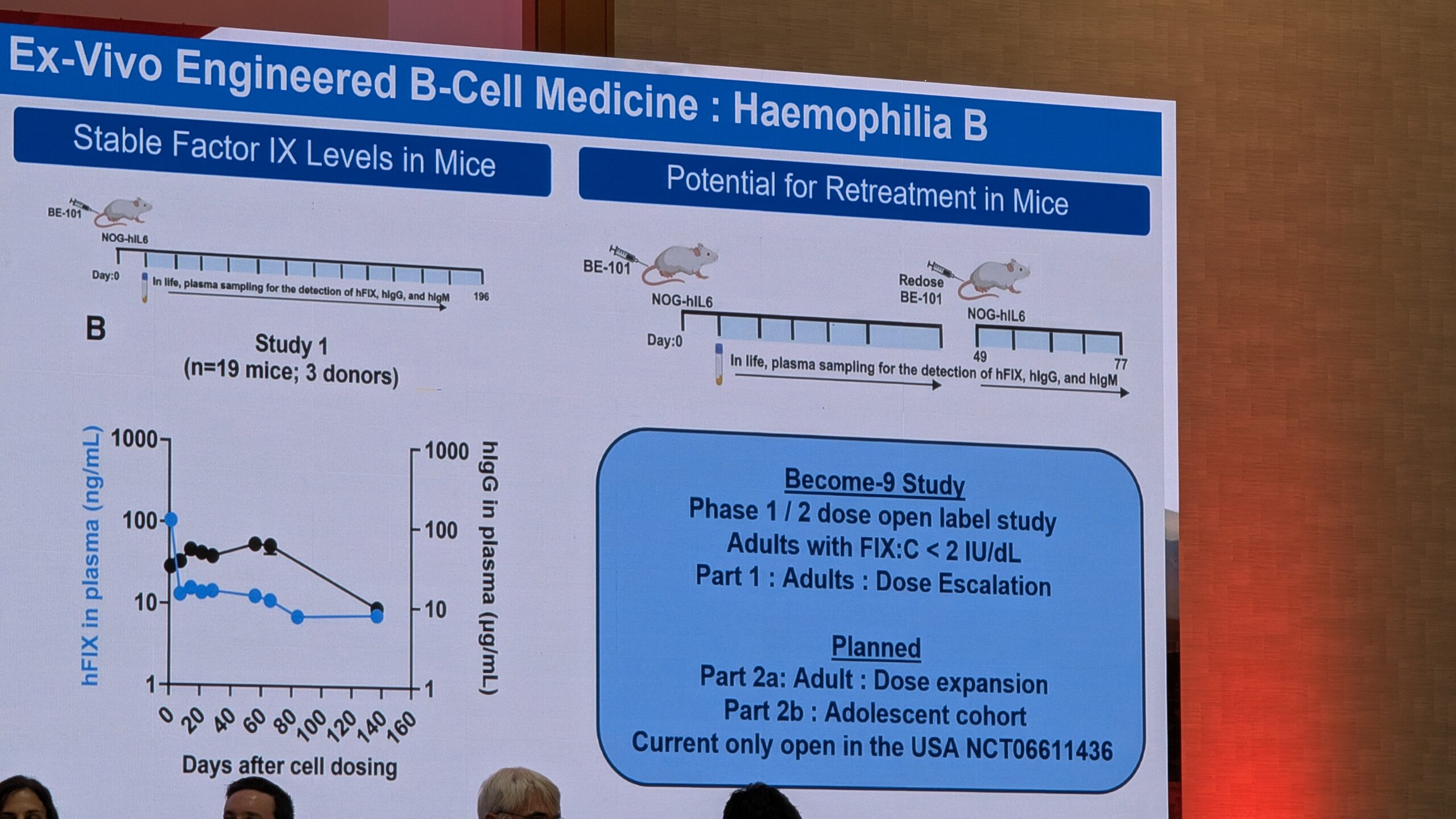
- Geeniteraapia reaalne kogemus ja selle pikaajalisele ohutus
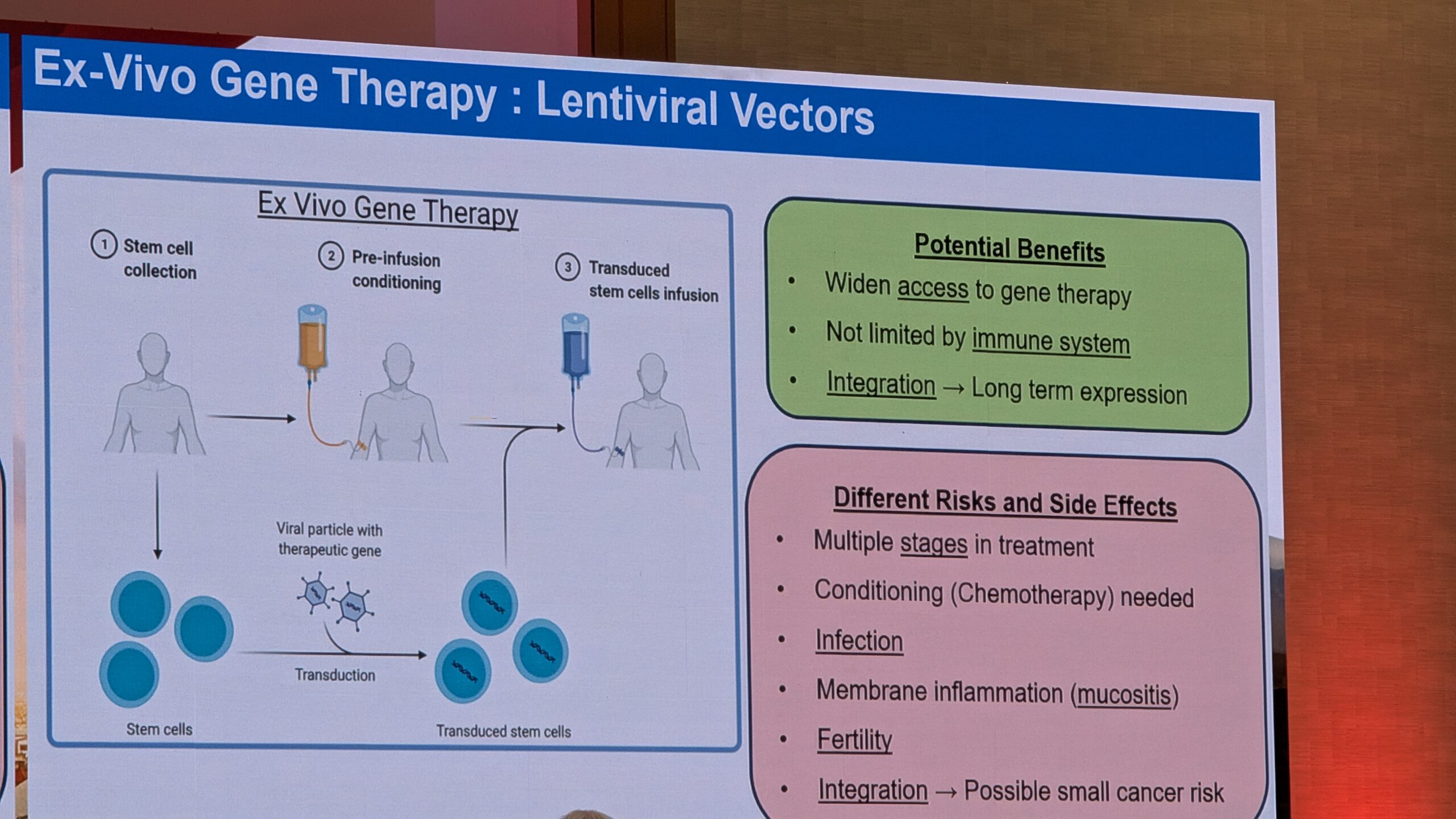
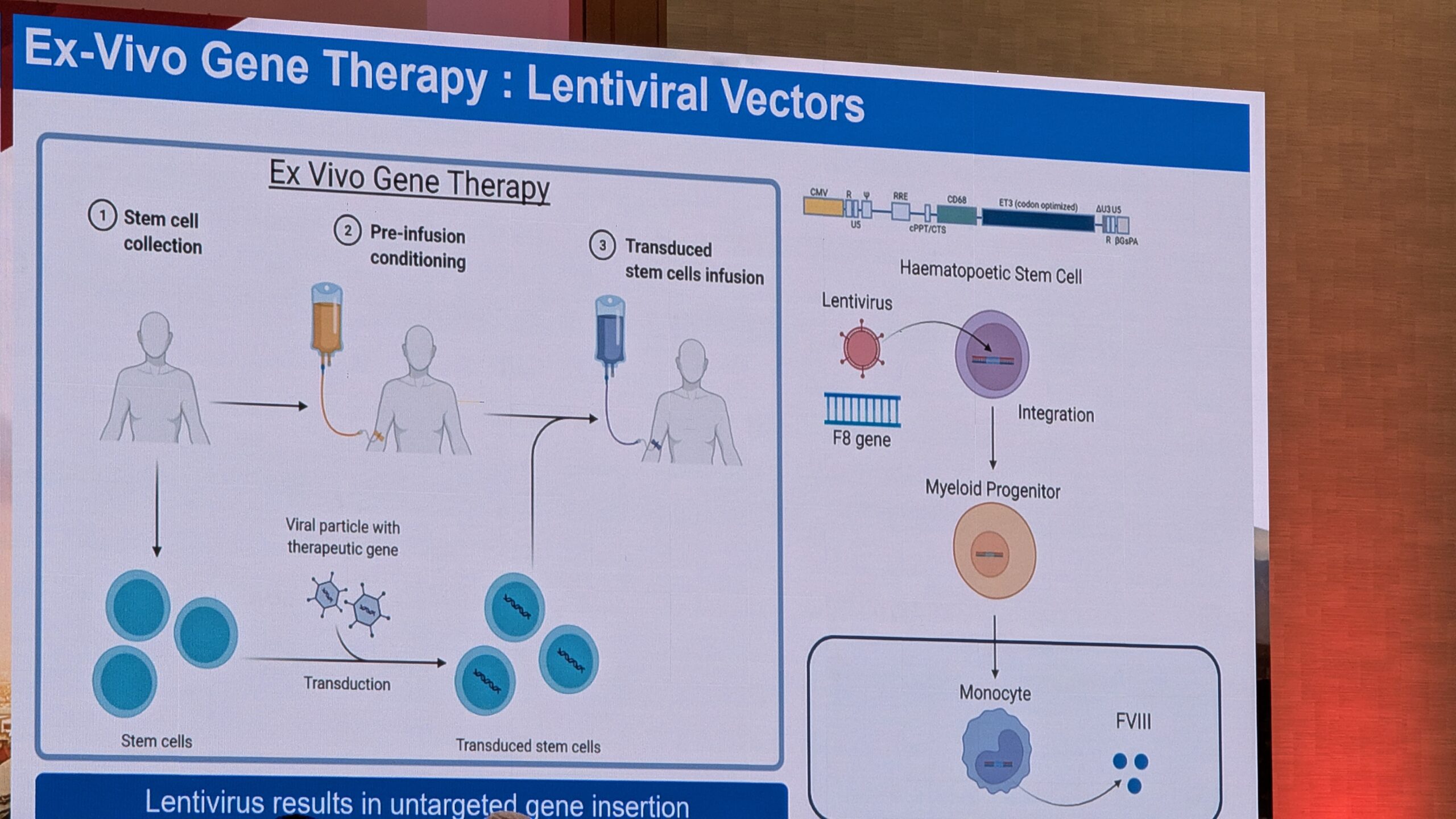
- Hemostaasi tasakaalustavad ravi variandid (nt TFPI ja antitrombiini inhibiitoritele) ning AAV-vektoritest erinevatele lähenemisviisid (nt geenide redigeerimine ja tüvirakkude teraapia).
- Haruldased veritsushäired ja uus grupp veritsejaid:
- Fibrinogeeni defektid,
- VWD (Von Willebrandi tõbi)
- Diagnoosimine on keeruline ja uusi ravivõimalusi ei ole. Eraldi toodi välja uus grupp veritsejaid: teadmata põhjusega verejooksuhäiretega (BDUC) patsiendid.
- Psühhosotsiaalne ja multidistsiplinaarne mudel: Rõhk oli vaimsel tervisel, eriti seoses uute ravimeetoditega ja muutunud identiteediga (liikumine “kangelasest” “tavaliseks” inimeseks). Oluline teema: suuhügieeni ja valu krooniline mõju veritsushäiretega patsientide elukvaliteedile.
- Ravimite kättesaadavus ja eestkostetöö: Tutvustati WHO põhiravimite loendi (EML) uuendusi ja jagati kogemusi ravimite hüvitamise mudelite (nt tulemuspõhised lepingud) osas.
EHC konverentsil osalesid Eesti Hemofiiliaühingust (EHÜ) Martin Kaal, Kaido Vaatemäe ja dr. Ines Vaide. Konverentsil osalemist toetas EHC ja Sobi.
Esitlused millel osalesime:
- Sessioon – hemofiilia ravi Austrias (Session 1 – Haemophilia Care in Austria)
1.1 Austria hemofiilia register (The Austrian Haemophilia Registry) – Dr. Ingrid Pabinger-Fasching
1.2 Austria hemofiilia ravijuhised (Austrian Guidelines for Haemophilia Treatment) – Christoph Male-Dressler
1.3 Kuus kümnendit propageerimist: Austria Hemofiiliaühing (Six Decades of Advocacy: The Austrian Haemophilia Society) – Thomas Schindl - Sessioon – Barjääride murdmine: naiste tervis ja veritsushäired (Session 2 – Breaking Barriers: Women’s Health and Bleeding Disorders)
2.1 Diagnoos ja nõustamine, naised ja tütarlapsed (Diagnosis and counselling in women and girls) – Margareta Holmström
2.2 Menopausi vanuse juhtimine (Management of menopausal age) – Nina Kovacevic
2.3 Sümptomaatiline Kandja – Patsiendi Perspektiiv (Symptomatic carrier – patient perspective) – Brina Zaman - Ravimitööstuse toetatud sümbioosium 1: „Veritsemisest kaugemale: vaimne tervis veritsushäirete kogukonnas“ (Industry Symposium 1 : “Beyond bleeding: Mental Health within the Bleeding Disorders Community”)
3.1 Hemofiilia vaimse tervise koormus: Kuidas saab ravivalik aidata? (The mental health burden of haemophilia: How can choice of therapy help?) – Evelien Krumb
3.2 Vaimse koormuse lahendamine hemofiilia korral: Patsiendi ja psühholoogi vaatenurk (Addressing the mental burden in haemophilia: Perspectives from someone living with haemophilia and a psychologist) – Marius Tanese ja Catia Damiao
3.3 Laps sündis hemofiiliaga: Vanema perspektiiv (Having a child born with haemophilia: Perspectives from a parent) – Blanka Krivicic Hyrat
3.4 Kuidas saab laiem tervishoiumeeskond toetada hemofiiliahaigeid vaimse koormuse korral? (How can the wider healthcare team support people with haemophilia with mental burdens?) – Catia Damiao ja Evelien Krumb - Tööstussümpoosion 2: „Hoolitse oma tulevase liigeste tervise ja liikuvuse eest: mida arvestada ja millele juba täna mõelda“ (Industry Symposium 2: “Caring for Your Future Joint Health and Mobility: What to Be Aware of and Start Thinking About Today”)
4.1 Pikaajalise liigeste tervise tagamine: tänaste valikute ja otsuste mõju (Ensuring Long-Term joint health: Impact of today’s choices and decisions) – Dr. Christoph Könings
4.2 Tuleviku liikuvuse kaitsmine: tegevused, mida saate kohe ette võtta (Protecting future mobility: Actions you can take now) – Ruth Elise Dybvik Matlary
4.3 Piiride ühine uurimine: tasakaal ettevaatlikkuse ja lahtilaskmise vahel (Exploring boundaries together: Balance between caution and letting go) – Angelika Isler - 3. sessioon – Von Willebrandi tõve tuleviku avamine (Session 3 – Unlocking the Future of Von Willebrand Disease)
5.1 Kogu pere vaimne tervis (Mental health of the whole family) – Cathy Verbraeken
5.2 VWD: esitlusest ja sõeluuringust geneetikani (VWD: From presentation and screening to genetics) – Giancarlo Castaman
5.3 Eelvaade tulevastesse VWD ravimeetoditesse (Sneak-peek in the future treatments for VWD) – Karin van Galen - 4. sessioon – Haruldaste veritsushäirete keerukuse uurimine: Inhibiitorid, BDUC ja fibrinogeeni defektid (Session 4 – Exploring the Complexities of Rare Bleeding Disorders: Inhibitors, BDUC, and Fibrinogen Defects)
6.1 Fibrinogeeni häirega veritsushaigused ja nende ravimeetodid (Fibrinogen defects: treatment approaches) – Dr. Alessandro Casini
6.2 Hemofiilia B inhibiitoritega: kas see on endiselt tähelepanuta jäetud rühm? (Haemophilia B with inhibitors: still a neglected group?) – Dominik Cepic
6.3 BDUC: uus rühm, mis väärib tähelepanu (BDUC: a new group that deserves attention) – Johanna Gebhart - 5. sessioon – SLAM-sessioon (Session 5 – SLAM Session)
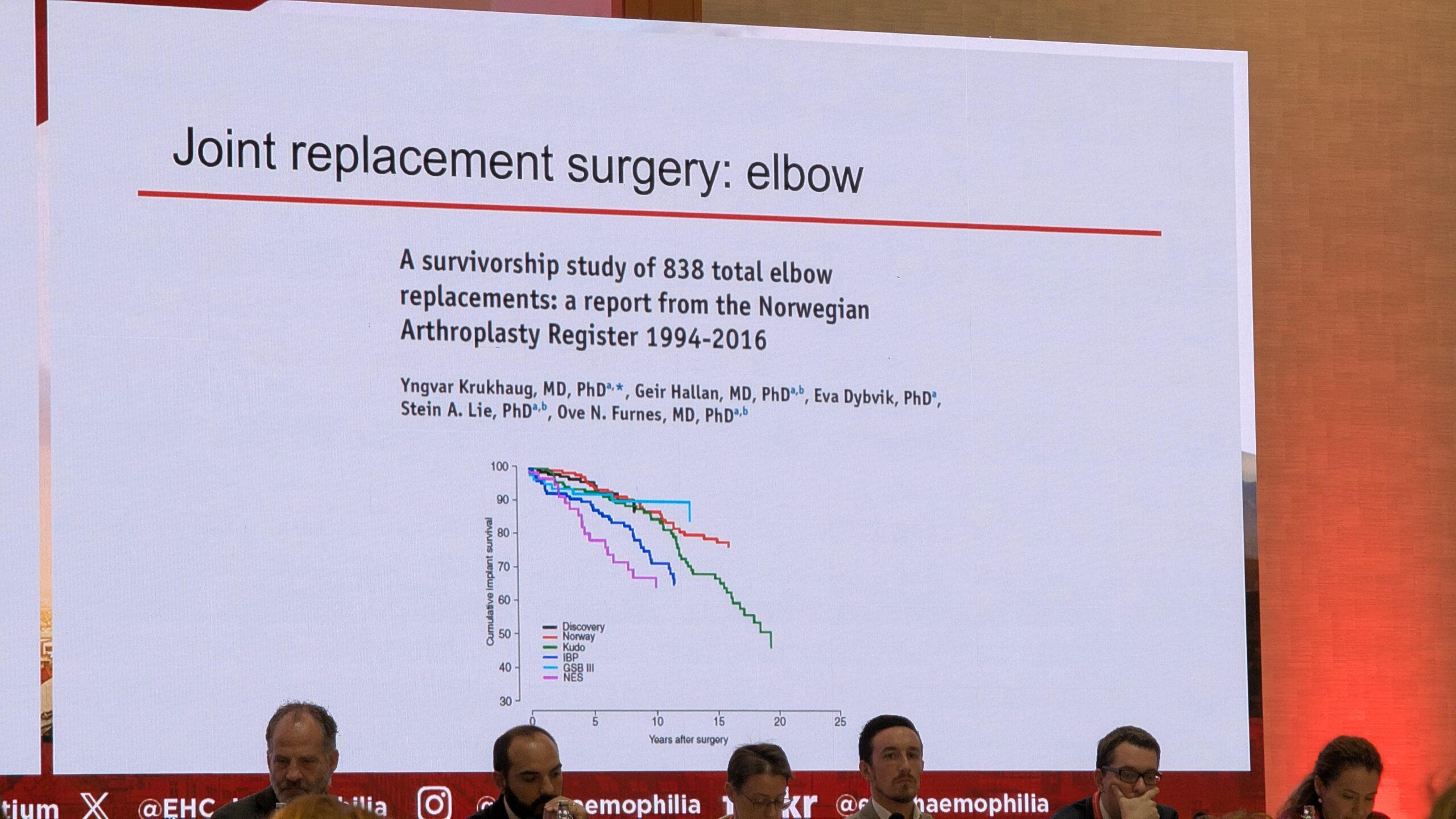
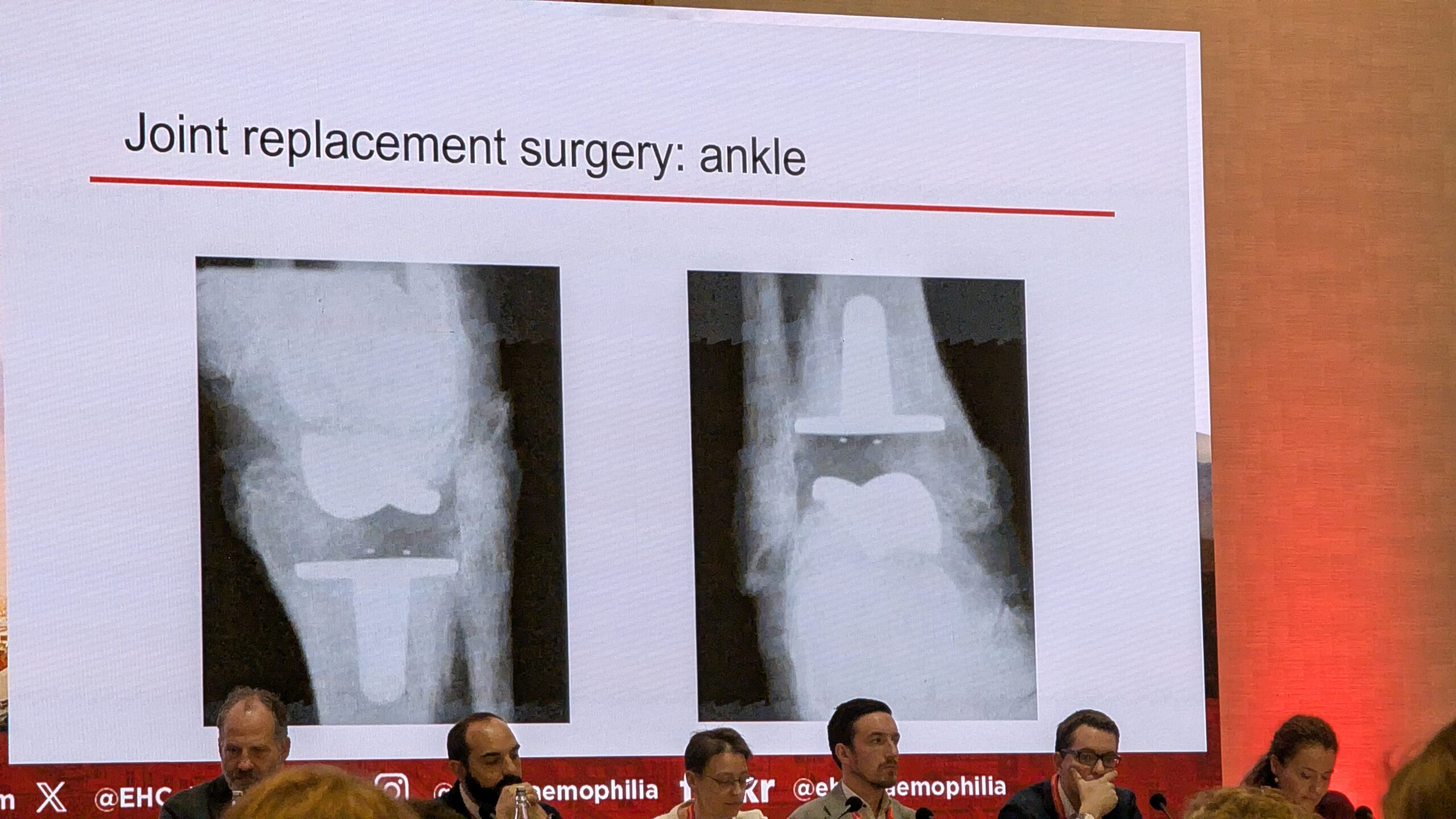
7.1 Ortopeedia edusammud: liigeseasendusest kõhrekoe konstrueerimiseni (Advances in orthopedics: from joint replacement to cartilage engineering) – Dr. Gianluigi Pasta
7.2 Millal ja kuidas alustada profülaktikat varem ravimata patsientidel? (When and how to start prophylaxis in PUPs?) – Dr. Christoph Königs
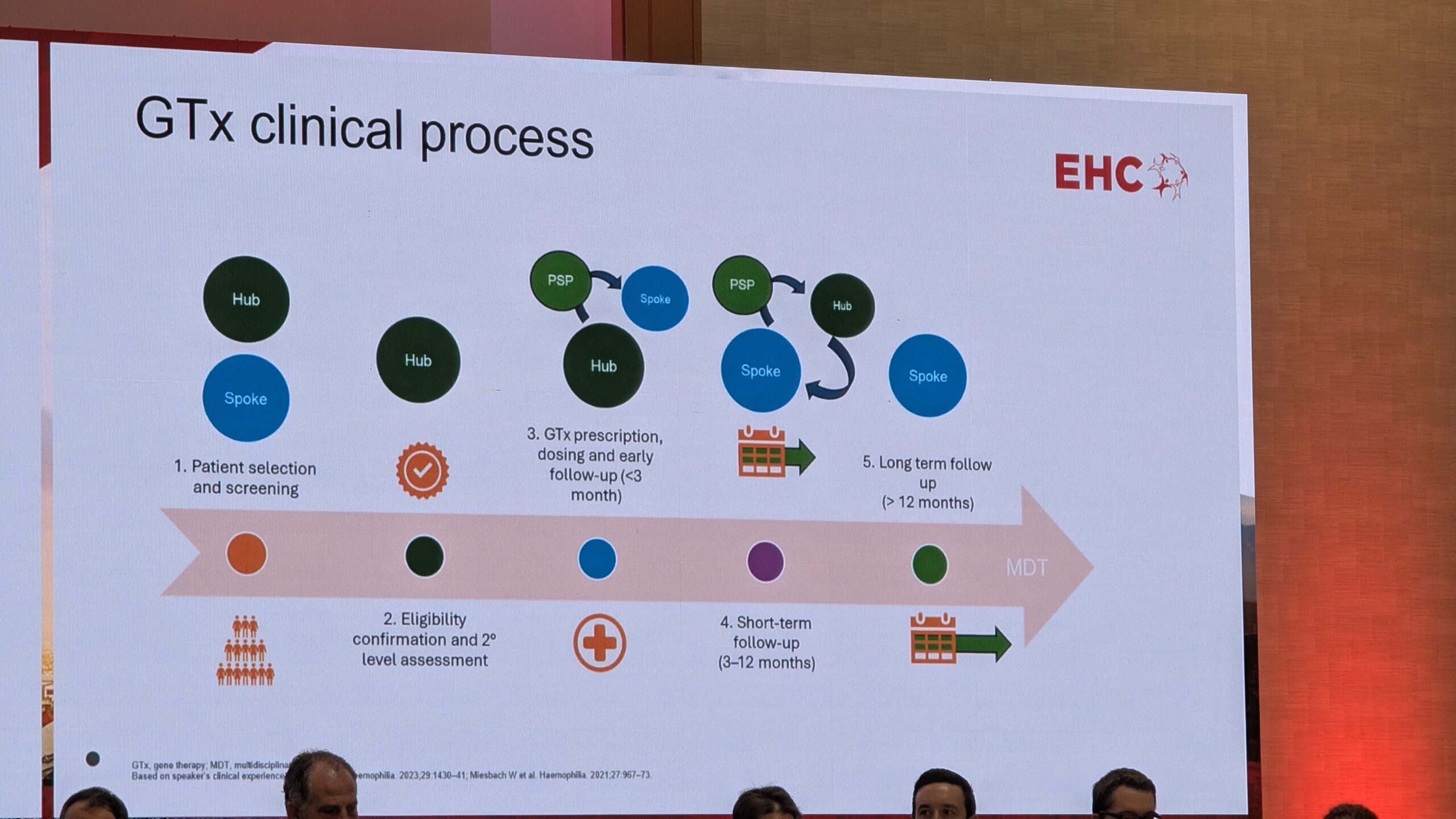
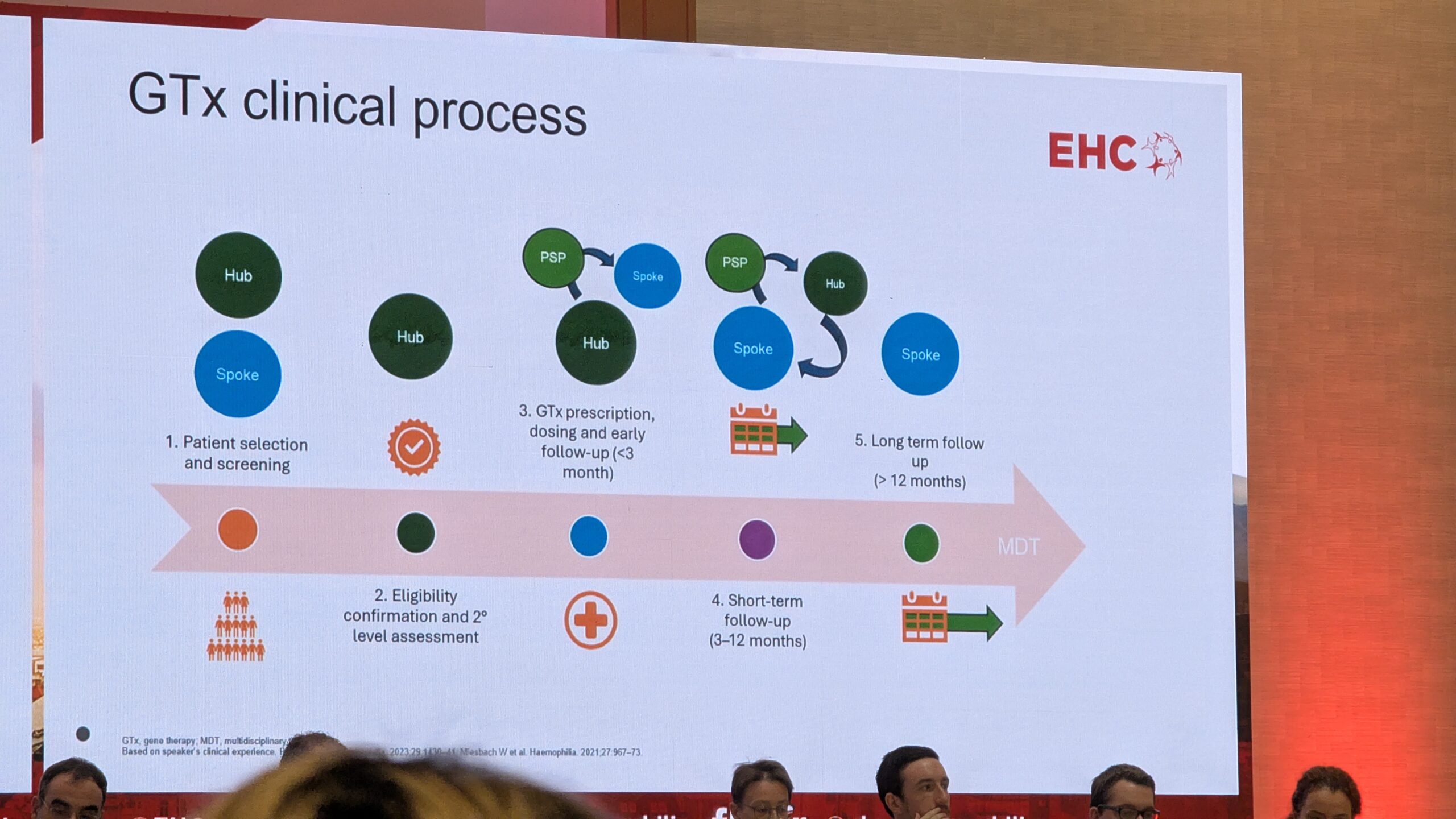
7.3 Geeniteraapia: reaalse maailma kogemused EL-i patsienditeekonnalt (Gene therapy: Real-world experience from the EU Patient journey) – Dario Di Minno
7.4 Valu leevendamine verejooksu häirete korral (Pain management in bleeding disorders) – Nathalie Roussel
7.5 Vananev aju hemofiilia korral (The Ageing Brain in Haemophilia) – William McKeown
7.6 Miks me oma haavu lakume? (Why are we licking our wounds?) – Johannes Thaler
7.7 ITI emitsizumabiga ravitud patsientidel (ITI in patients treated with Emicizumab) – Maria Elisa Mancuso - Tööstussümpoosion 3: „Hemostaasi (taas)tasakaalustamine, patsiendihoolduse tasakaalustamine: teaduse, hoolduse ja kogukonna ühendamine“ (Industry Symposium 3: “(Re)balancing haemostasis, balancing patient care: bridging science, care and community”)
- Tööstussümpoosion 4: „Uued horisondid VWD ravis“ (Industry Symposium 4: “New Horizons in Management of VWD”)
9.1 Veritsemisest kuuluvustundeni: elamine von Willebrandi tõvega (From Bleeding to Belonging: Living with von Willeband Disease) – Baiba Ziemele
9.2 Von Willebrandi tõve kaasaegne diagnostiline lähenemine – von Willebrandi faktori tasemest kaugemale (Modern Diagnostic Approach to von Willebrand Disease – Beyond von WIllebrand Factor Level) – Giancarlo Castaman
9.3 Von Willebrandi tõve isikupärastatud ravi – mis on patsientide jaoks oluline? (Personalized Treatment of von WIllebrand Disease – What Matters for patients?) – Cihan Ay - 6. sessioon – Uued piirid hemofiilia geenteraapias (Session 6 – New Frontiers in Haemophilia Gene Therapy)
10.1 Reaalsed andmed kliinilistest uuringutest (Real world data out of clinical trials) – Wolfgang Miesbach
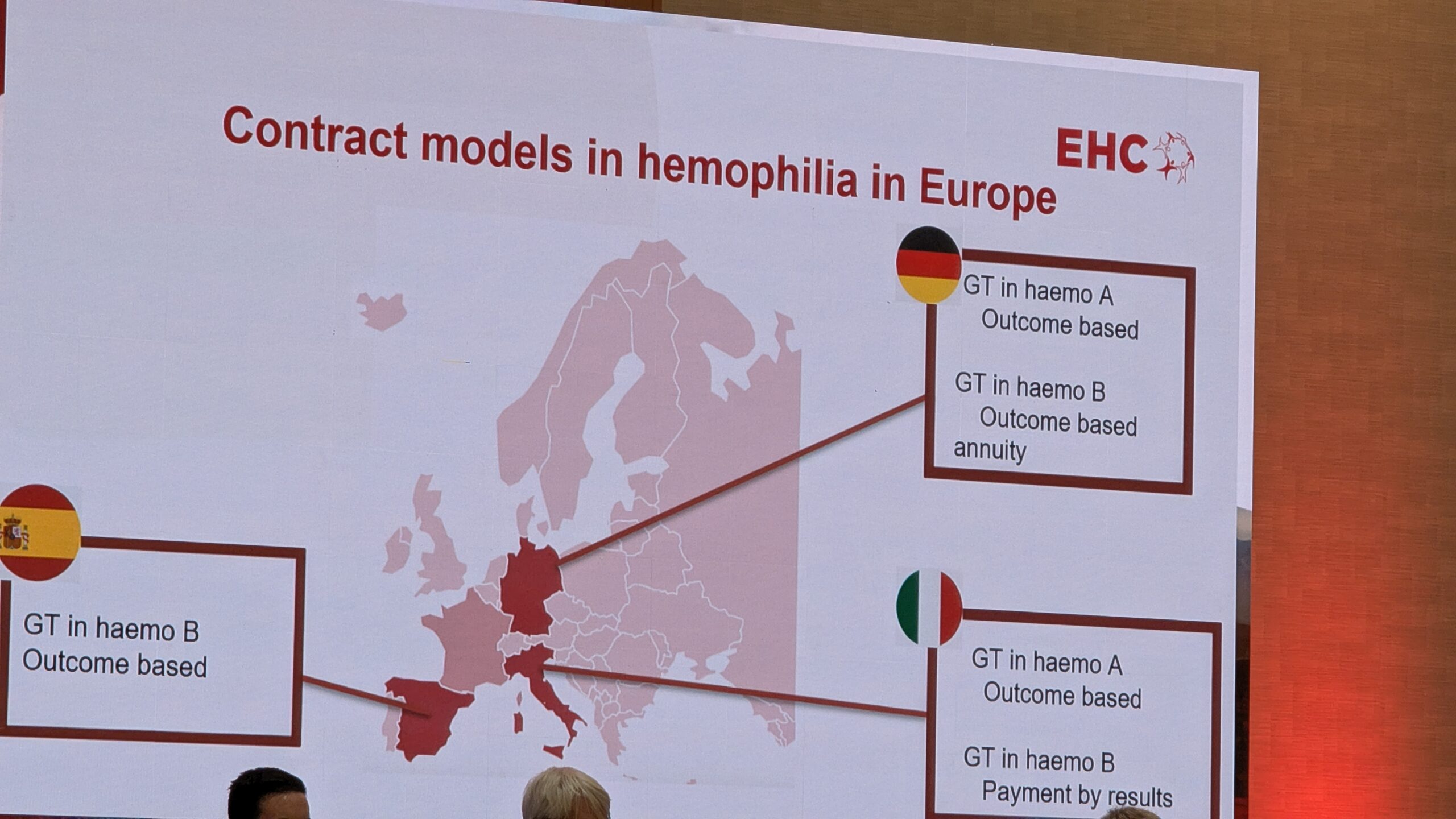
10.2 Seni vastuvõetud hüvitamismudelid (Models of reimbursement adopted so far) – Gaetan Duport
10.3 Uued lähenemisviisid, mis erinevad AAV-vektoritest (New approaches different from AAV vectors) – Paul Batty - 7. sessioon – Noorte debatid (Session 7 – Youth Debates)
11.1 Kas vaimset tervist tuleks tervikliku ravi raames füüsilise raviga võrdselt prioriseerida? (Should mental health be prioritised equally with physical treatment in comprehensive care?) – Rebecca Mosling & Giacomo Centenaro
11.2 Normaalse hemostaasi poole püüdlemine – julge samm edasi või ohtlik uus standard? (Striving for Normal Haemostasis – a bold step forward or a dangerous new standard?) – Adrian Vaduva & Ziv Bozo - 8. sessioon – Ravi psühhosotsiaalse mõju navigeerimine (Session 8 – Navigating the Psychosocial Impact of Treatment)
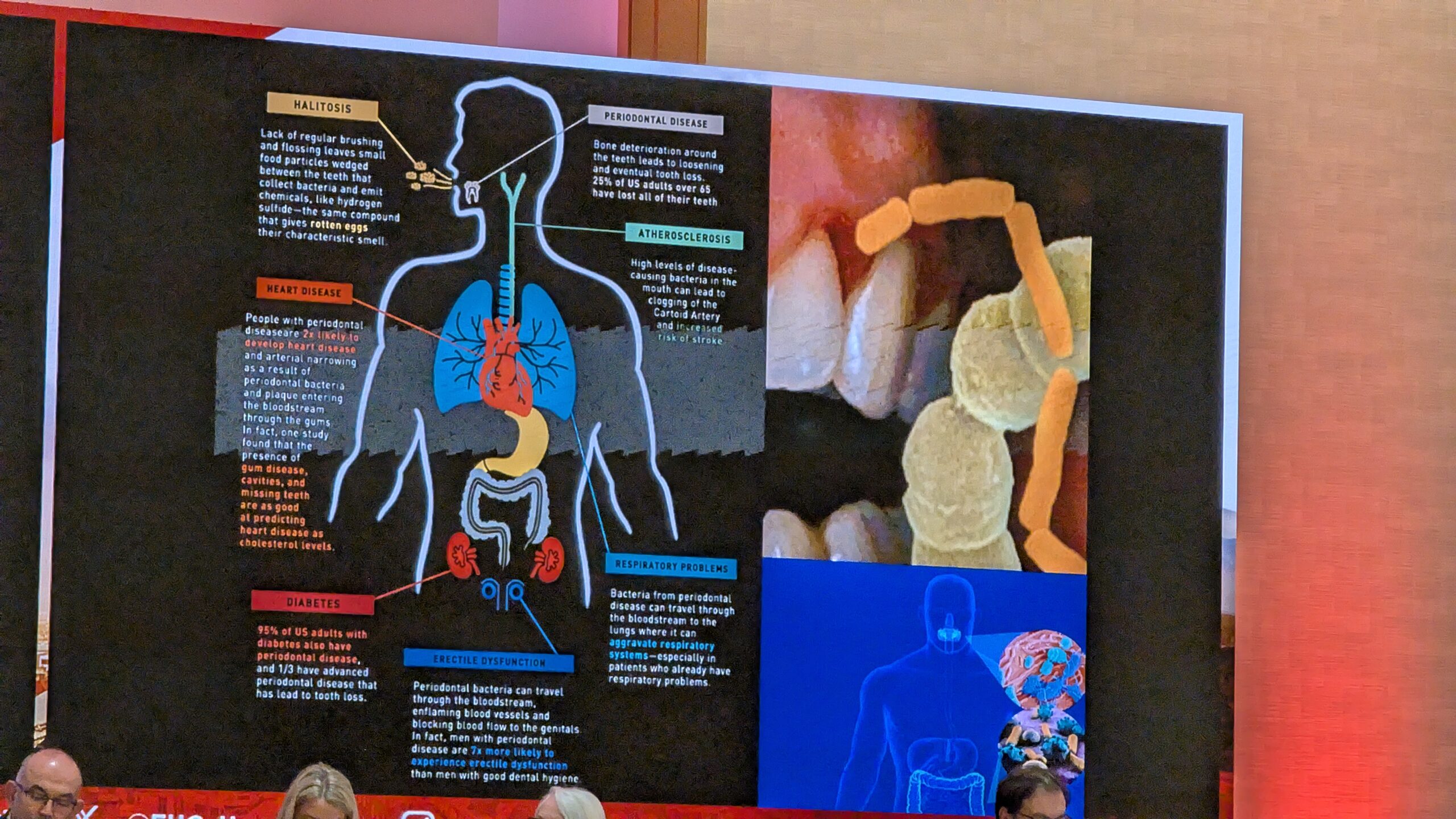
12.1 Suuõõne tervis: ühiskondlik koorem? (Oral health: a societal burden?) – Alison Dougall
12.2 Uute ravimeetoditega seotud vaimse tervise väljakutsed (Mental health challenges with new therapies) – Christina Burgess
12.3 Kangelastest tavalisteks inimesteks (From heroes to normal people) – Miguel Crato - Tööstuse sümpoosion 6: „Väljakutsuvad väärarusaamad patsientide teekonnad ja VWD hoolduse tulevik” (Industry Symposium 6: “Challenging Misconceptions Patient Journeys & Future of VWD Care”)
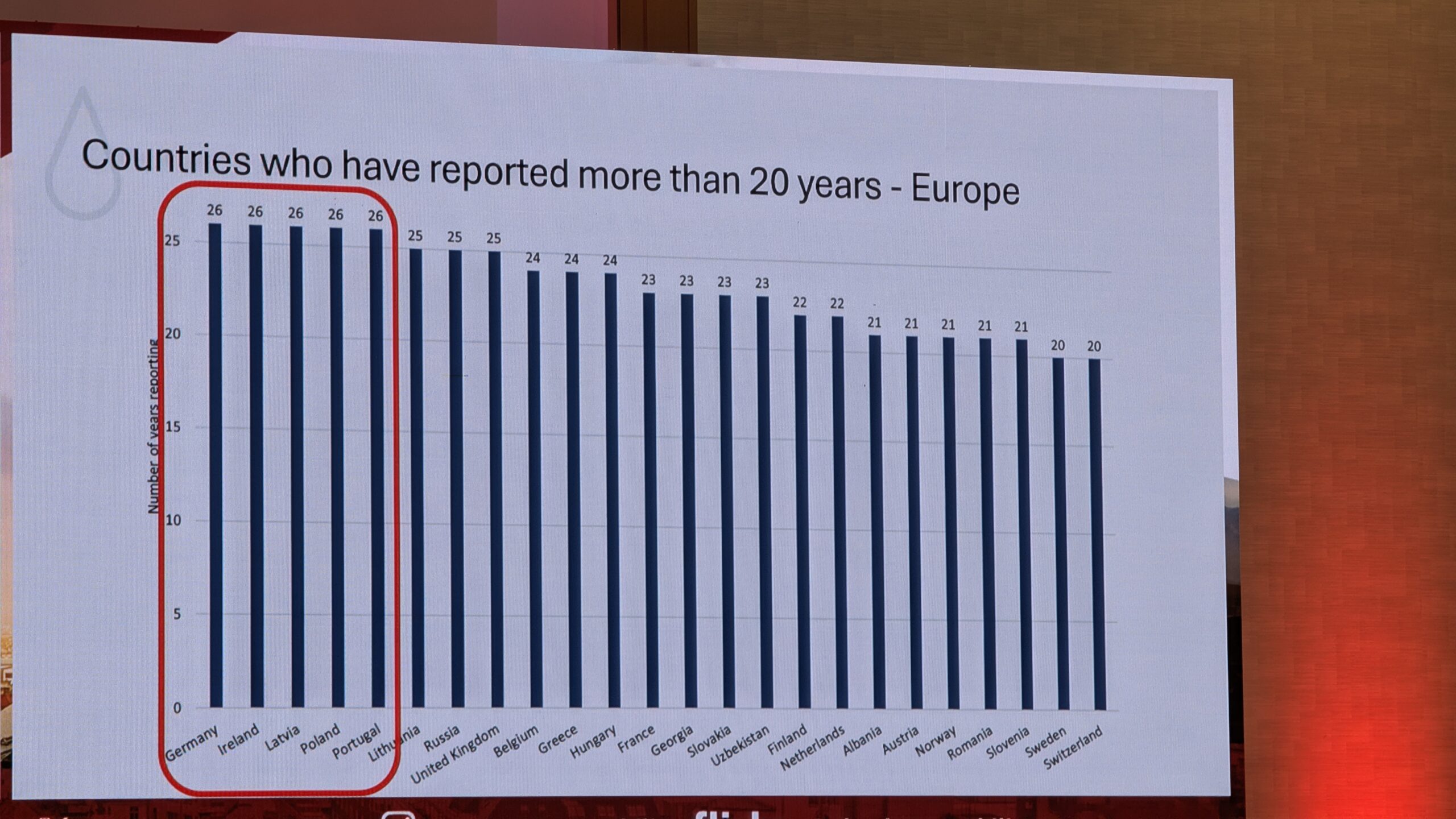
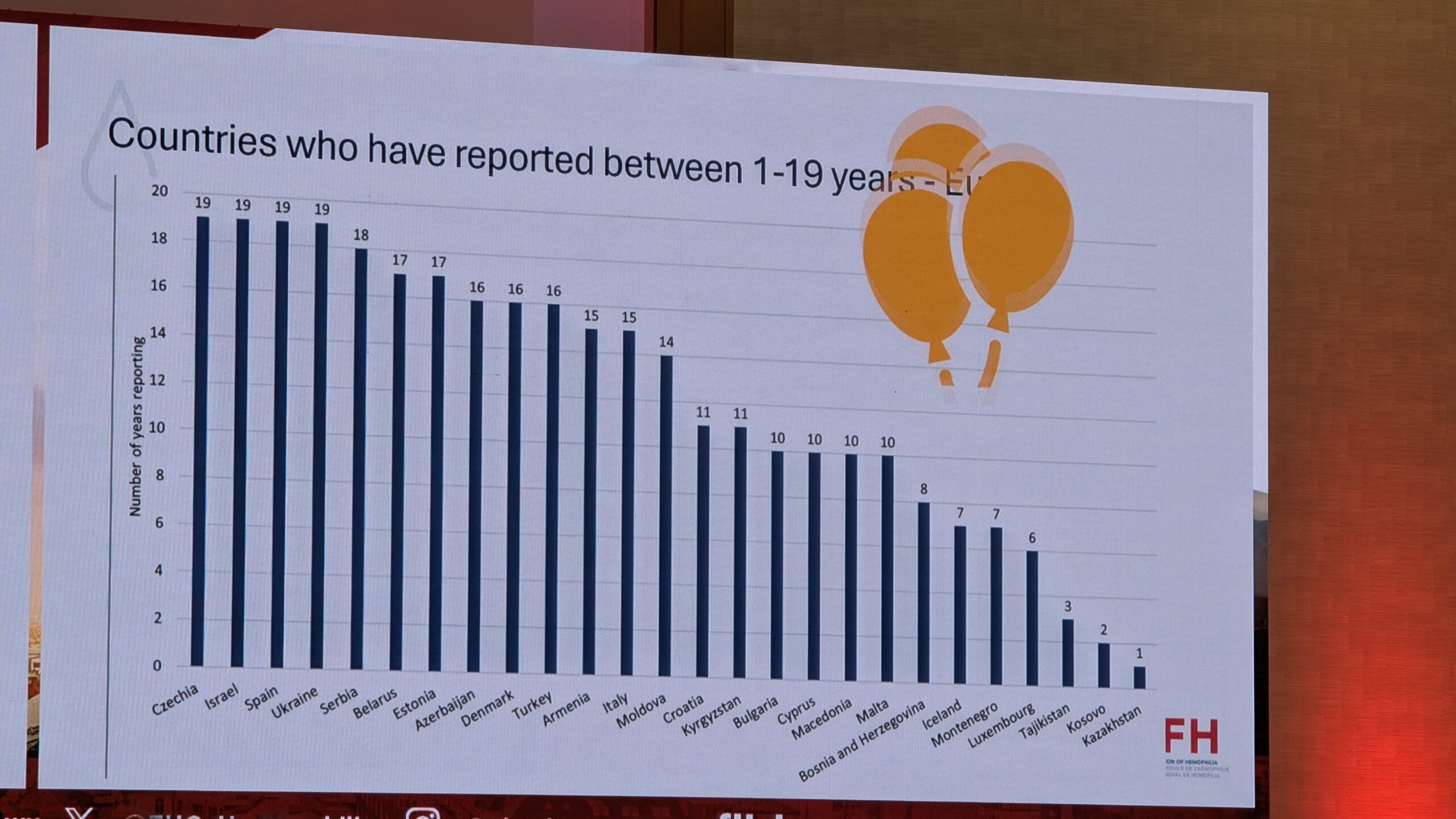
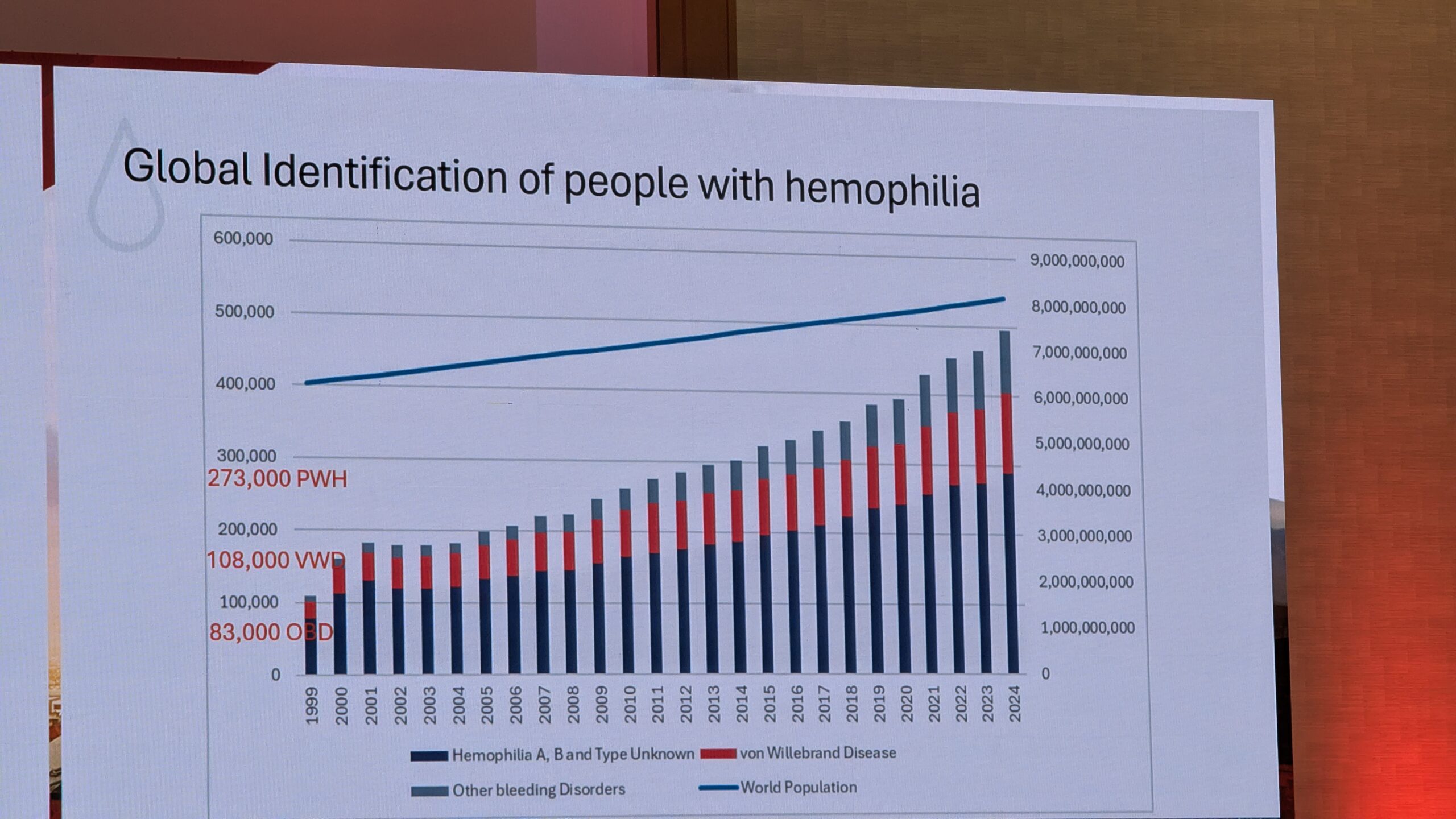
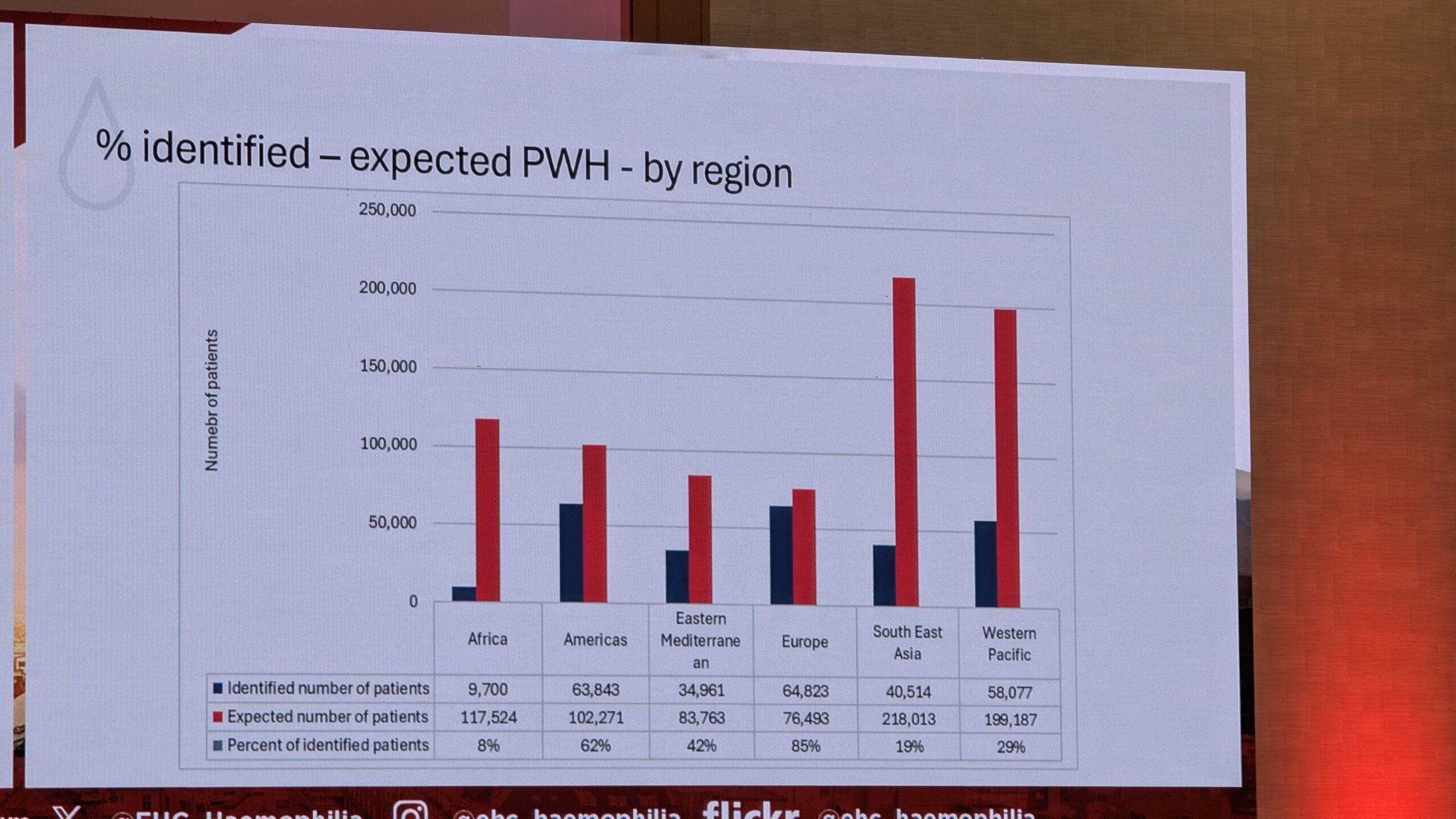
Ülevaade WFH eestkostetööst, ravijuhistest ja globaalsest seirest (Overview of WFH advocacy, treatment guidelines, and global monitoring)
1. Sessioon – hemofiilia ravi Austrias
1.1 Austria hemofiilia register – Dr. Ingrid Pabinger-Fasching
Austria hemofiilia register on Austria Hemofiiliaühingu ja selle teadusliku nõukogu koostööprojekt, mis on loodud koostöös kõigi Austria hemofiiliakeskuste ja Viini Meditsiiniülikooliga. Selle registri loomine tulenes vajadusest täita rahvusvahelisi dokumentatsiooninõudeid ning täita aruandluskohustusi Euroopa ja ülemaailmsel tasandil. Dr. Pabinger mainis, et selle registri loomisel oli suureks motivaatoriks ja liikumapanevaks jõuks endine Euroopa Hemofiilia Konsortsiumi (EHC) president Hubert Battel.
Registri peamised eesmärgid on epidemioloogiliste andmete kogumine, ülevaate saamine hemofiiliaravi seisust Austrias ning võimalus võrrelda Austria ravi- ja epidemioloogilisi andmeid rahvusvahelisel tasandil. See hõlbustab ka koostööd Austria keskuste vahel ja teiste riiklike registritega (näiteks Saksamaa ja Suurbritannia registriga). Kuigi soovitakse registrit laiendada, on fookus ressursipuuduse tõttu hetkel peamiselt hemofiilial, ehkki kaasatud on ka Von Willebrandi tõvega ja teiste veritsushäiretega isikud.
Projekti rahastamine on suur probleem. Ehkki tervishoiuministeerium pakkus rahalist toetust kuni 2008. aastani, on register pärast seda täielikult sõltuv farmaatsiatööstusest ja sponsoritest. Sponsoritele ja Austria Hemofiiliaühingule edastatakse anonüümseid koondandmeid (epidemioloogilised andmed ja ravivõimalused), mitte otsest individuaalset teavet patsientide kohta.
Register on jagatud kolmeks osaks: esiteks, epidemioloogiliste põhiandmete kogumine ja kvaliteedi tagamine, mis on ühekordne iga patsiendi puhul. Teiseks, laiendatud kvaliteedi tagamine, mis on andmekogum, mida uuendatakse igal aastal ja alati, kui patsient kontrollis käib (see puudutab eelkõige raskema häirega patsiente, mitte kergete häiretega patsiente). Kolmandaks, kalibreerimine, mis on iga-aastane uuring patsiendi praeguse tervisliku seisundi kohta.
Eetilistel kaalutlustel peavad patsiendid allkirjastama kirjaliku nõusoleku vormi. Registri protokoll on heaks kiidetud Viini Meditsiiniülikooli ning kõigi Austria meditsiiniülikoolide eetikakomiteede poolt, mis on ka kõige olulisemad hemofiiliakeskused. Andmete edastamise leping on sõlmitud haigla operaatori ja Viini Meditsiiniülikooli vahel. Register kogub andmeid diagnoosi raskusastme, haigusloo, ravi tüübi, liigeste seisundi, laboratoorsete testide (maksafunktsioon, vereanalüüs), inhibiitori staatuse ja psühholoogiliste testide tulemuste kohta.
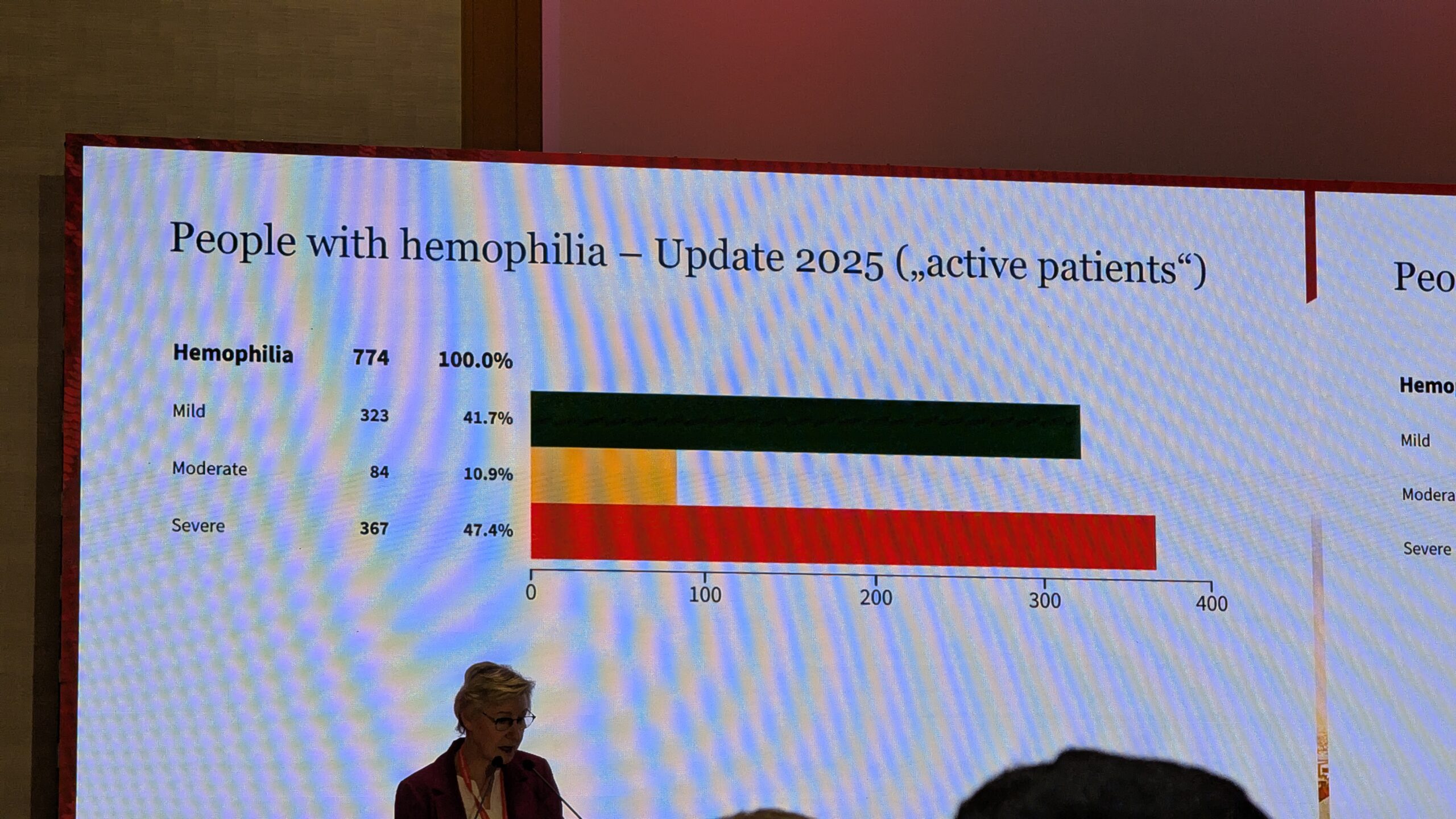
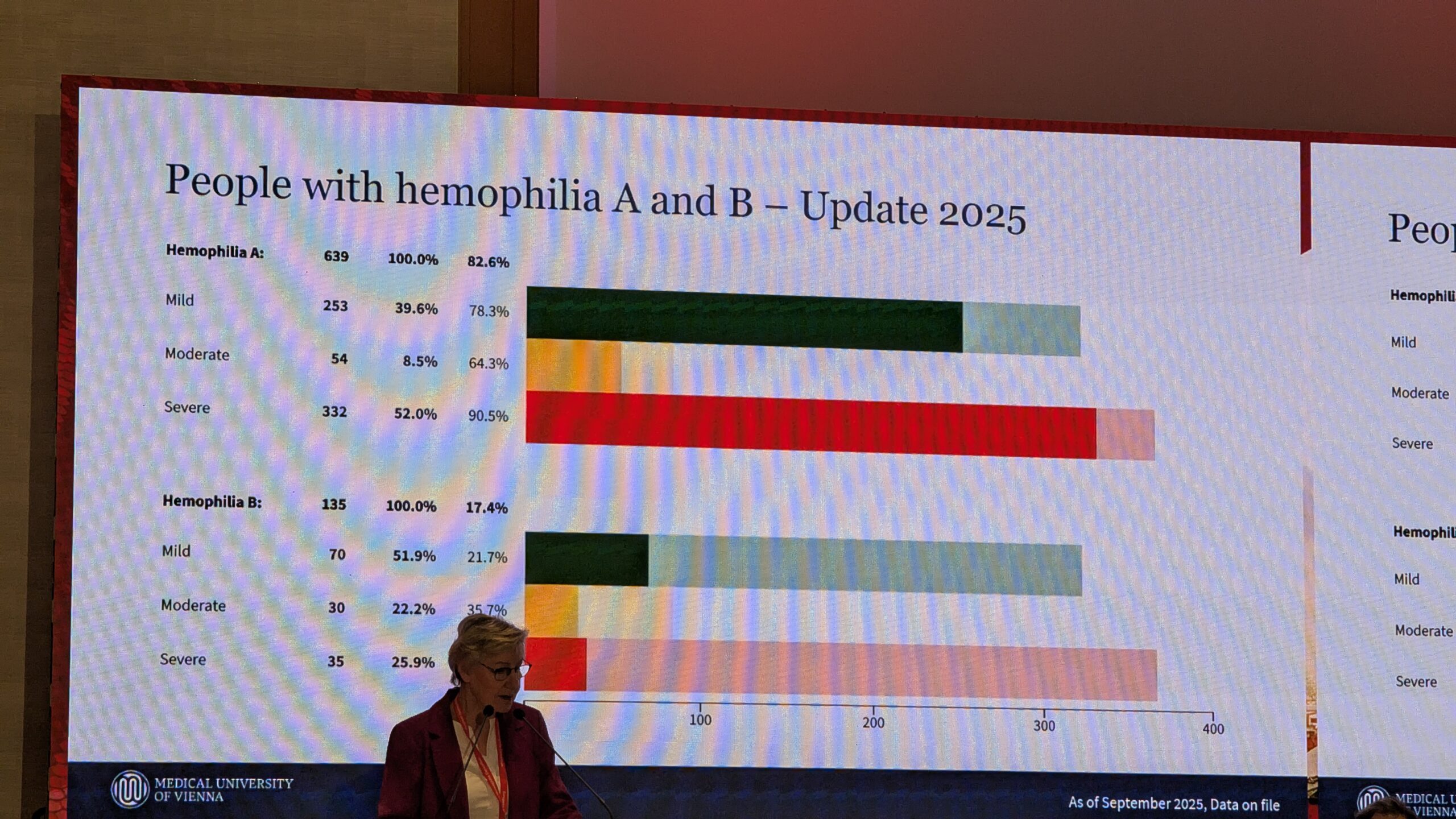
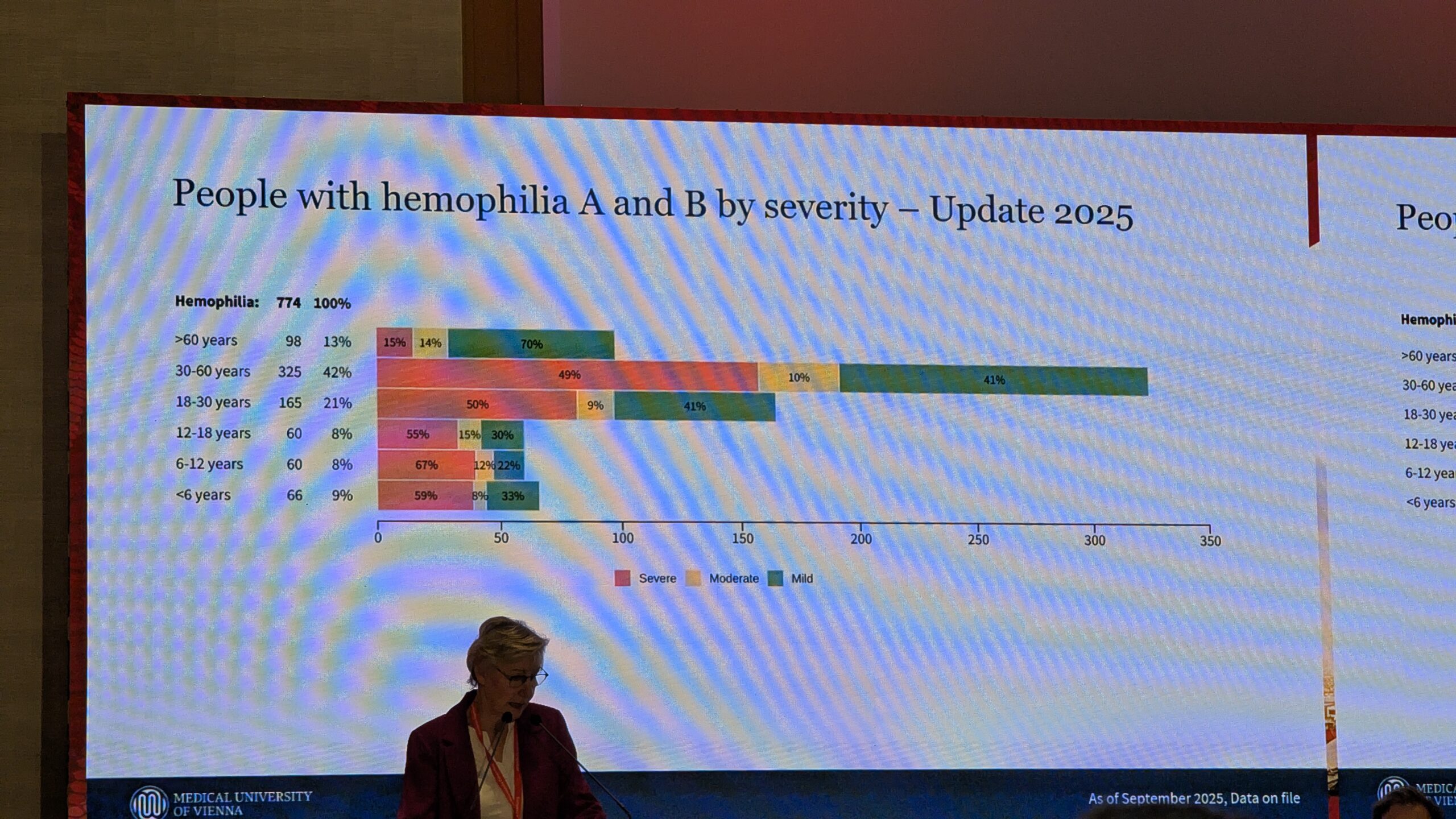
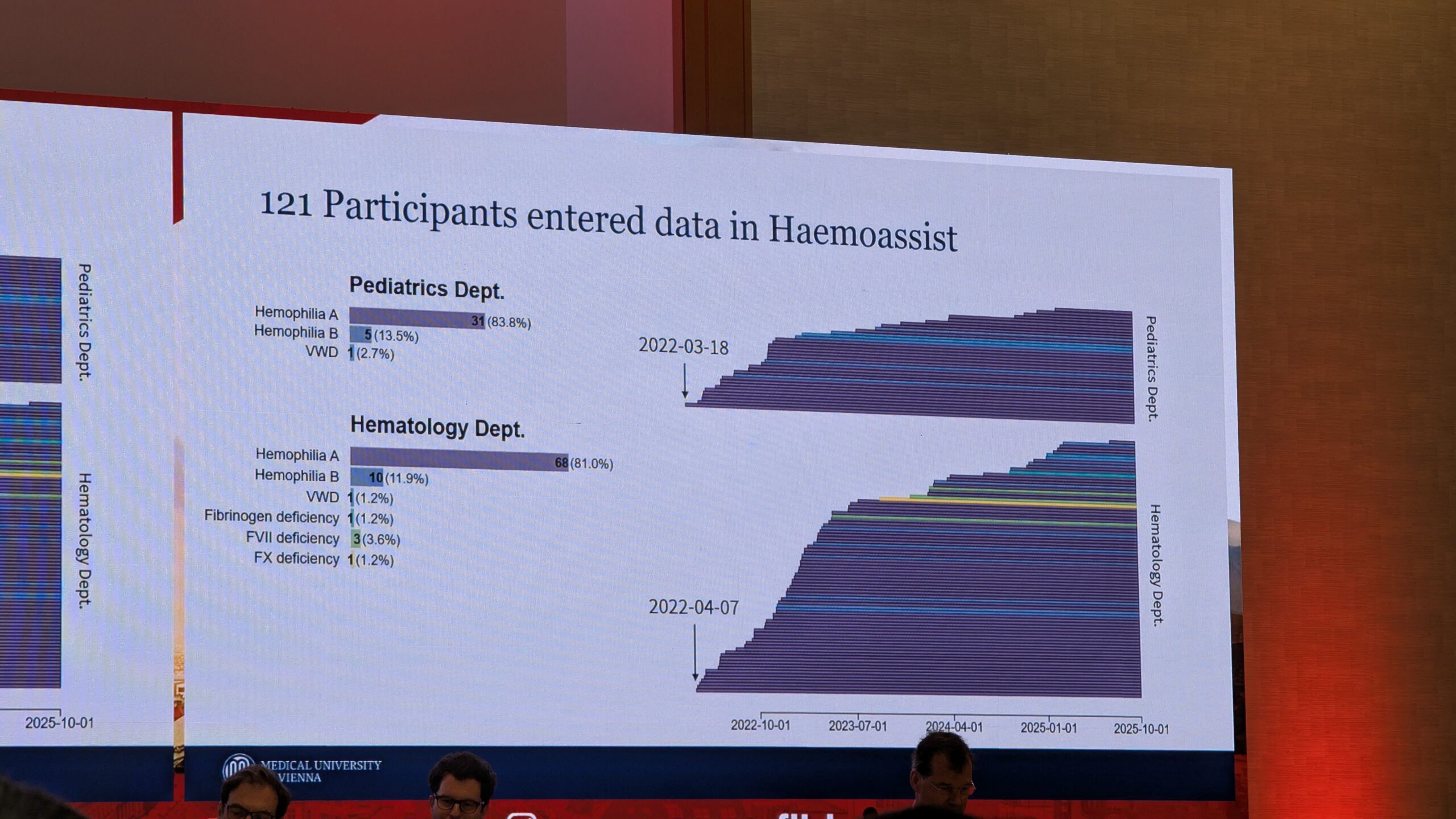
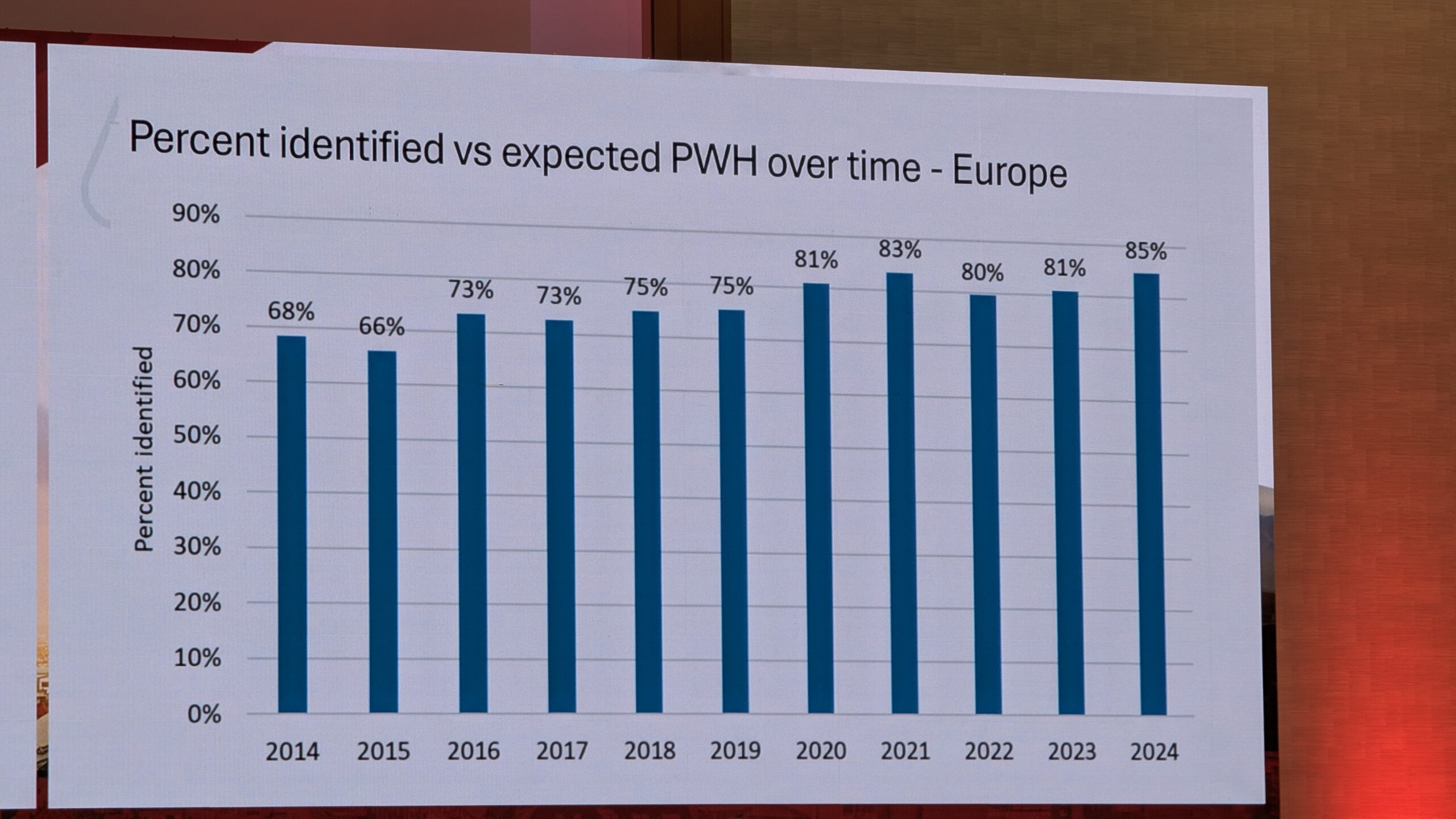
Statistilised andmed ja tulemused (seisuga 2025. aasta värskendus) Register hõlmab üheksat osalevat hemofiiliakeskust kaheksas Austria liidumaa osariigis. Süsteemi on laaditud 846 patsienti (Viini keskuste täiskasvanute ja laste osakondades), mis moodustab hinnanguliselt umbes 85% kõigist Austrias elavatest hemofiiliapatsientidest. 774 registreeritud patsiendil on hemofiilia. Ligi pooltel neist on raske hemofiilia.
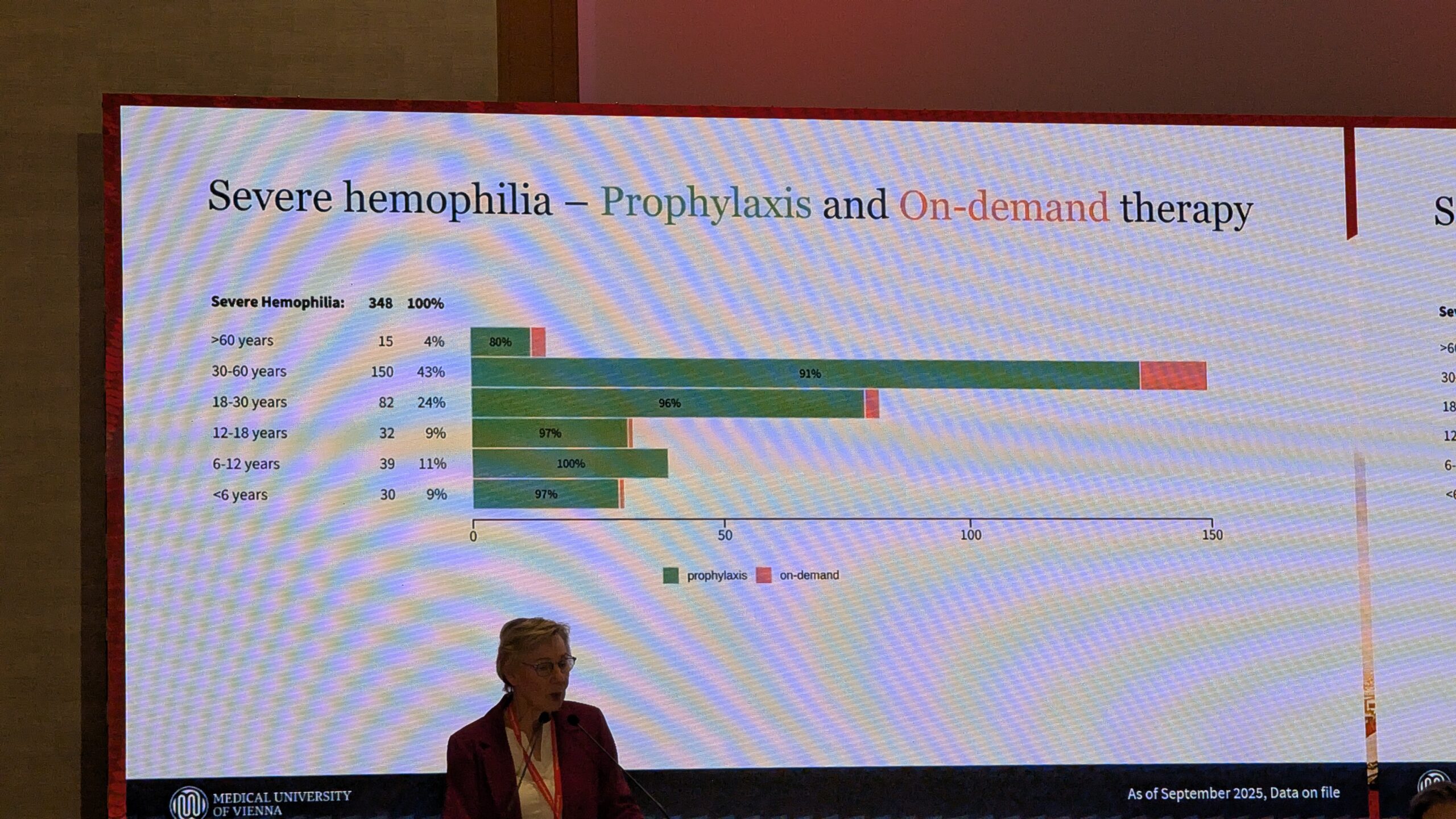
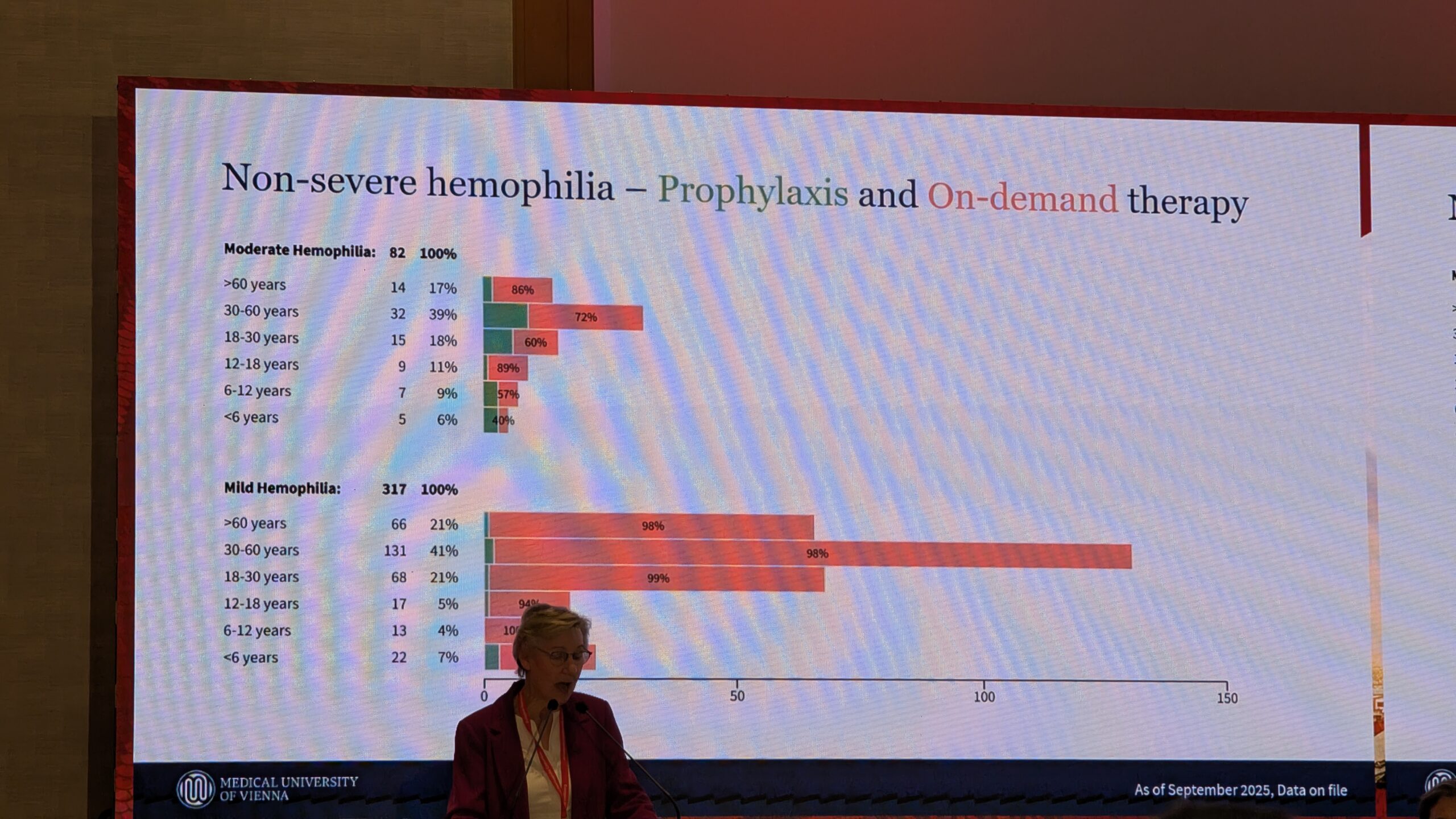
Peaaegu kõik raske hemofiiliaga patsiendid on profülaktilisel ravil. Väike hulk vanemaid patsiente ei ole profülaktikat omaks võtnud. Mõõduka hemofiiliaga patsientidel on profülaktika osakaal madalam ja nad on enamasti vajaduspõhisel ravil.
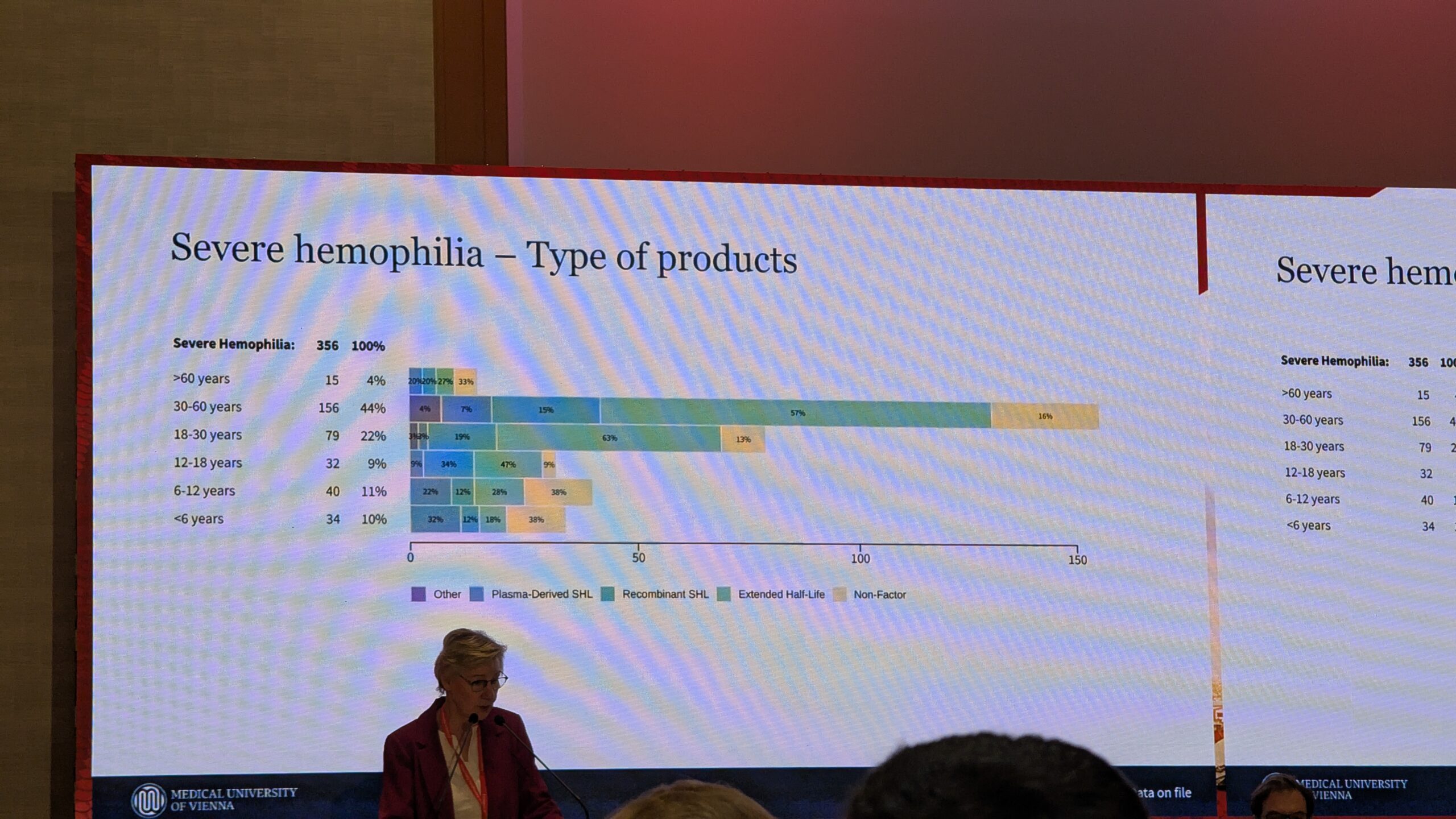
Austrias kasutatakse laia valikut tooteid, sealhulgas rekombinantseid standard- ja pikendatud poolväärtusajaga faktoreid (laste seas kasvavas koguses). Kasutatakse ka plasmast saadud tooteid, lähtudes varasemast ideest, et inhibiitorite teke võib olla madalam, kui neid kasutatakse varases elueas.
Üle 60 eluaastaste hemofiilia patsientide arv on Austrias üsna madal. Seda seletatakse asjaoluga, et paljud patsiendid surid varasemates aastakümnetes nakkushaiguste (eriti HIV ja C-hepatiidi) tõttu.
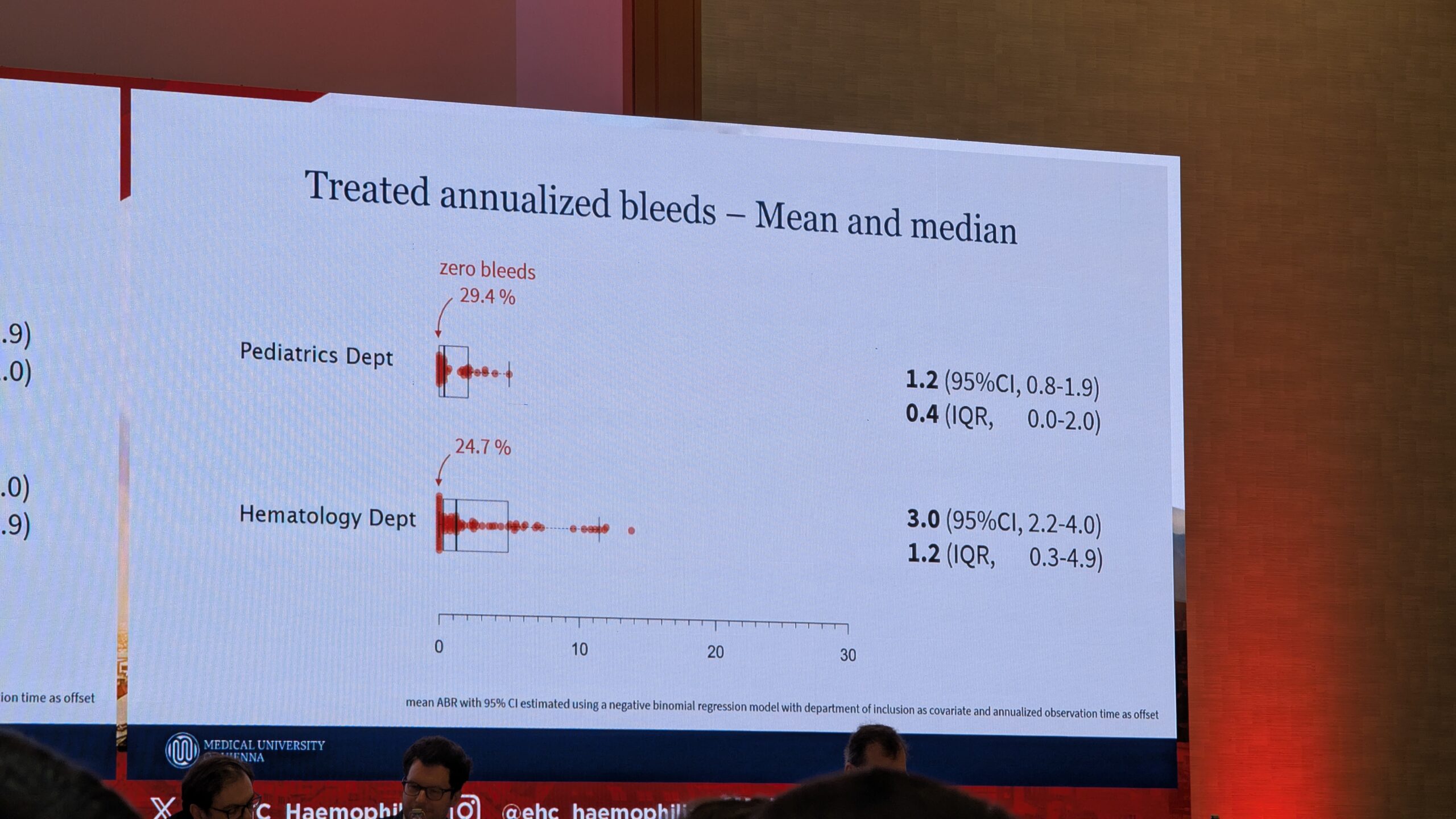
Autrias on laste keskmine aastane verejooksu sagedus (median Annualized Bleed Rate) 1.2. Lasteosakonnas on liigese veritsuste mediaan sagedus null. See näitab olulist edasiminekut võrreldes varasemate tulemustega, kus mediaan ABR oli umbes viis. See vähenemine on seotud uute ravimeetodite, profülaktika sagenemise ja pikendatud poolväärtusajaga faktorteraapiate kasutuselevõtuga. Elektrooniline dokumentatsioon (HEMOSIS) Viinis, kus on 150 kaasatud patsienti, võimaldab andmete automaatset edastamist registrisse.
1.2 Austria hemofiilia ravijuhised – Christoph Male-Dressler
Christoph Male-Dressler esitles Austria hemofiilia ravijuhiseid, mida ta kirjeldas kui head näidet Austria ravikeskuste ja Hemofiiliaühingu vahelisest koostööst.
Juhiste väljatöötamist juhtis Austria Hemofiiliaühingu Meditsiiniline Teaduslik Nõukogu. See nõukogu asutati algselt eesmärgiga nõustada ühingut teaduslikes küsimustes ajal, mil nakkused olid peamised probleemid. Nõukogusse kuuluvad kõigi Austria keskuste juhtivad arstid ning spetsialistid erinevatelt erialadelt, nagu taastusraviarstid, ortopeedid, sünnitus ja günekoloogia, laborispetsialsitid ja transfusioloogid, õed ja farmatseudid.
Austria juhised kujundati Maailma Hemofiilia Föderatsiooni (WFH) juhiste järgi, mis avaldati 2013. ja 2020. aastal. Eesmärk ei olnud juhiseid kopeerida, vaid järgida ühist põhimõtet: ühised juhised kõigile, kes on Austrias hemofiiliaraviga seotud.
Juhised avaldati esmakordselt 2015. aastal ja uuendatud versioon avaldati 2024. aastal. Uuem versioon on mahukam ja sisaldab oluliselt rohkem teavet uute ravimeetodite, sealhulgas geeniteraapia ja mittefaktorteraapiate kohta. Juhised on kirjutatud saksa keeles.
Juhised sisaldavad peatükke diagnostika, ravi (mis on põhiosa ja kõige kiiremini muutuv sihtmärk), tulemusnäitajate ning eriaspektide kohta lastele ja täiskasvanutele. Eraldi käsitletakse spetsiifilisi ravimeetodeid ja asendusravi operatsioonide ajal.
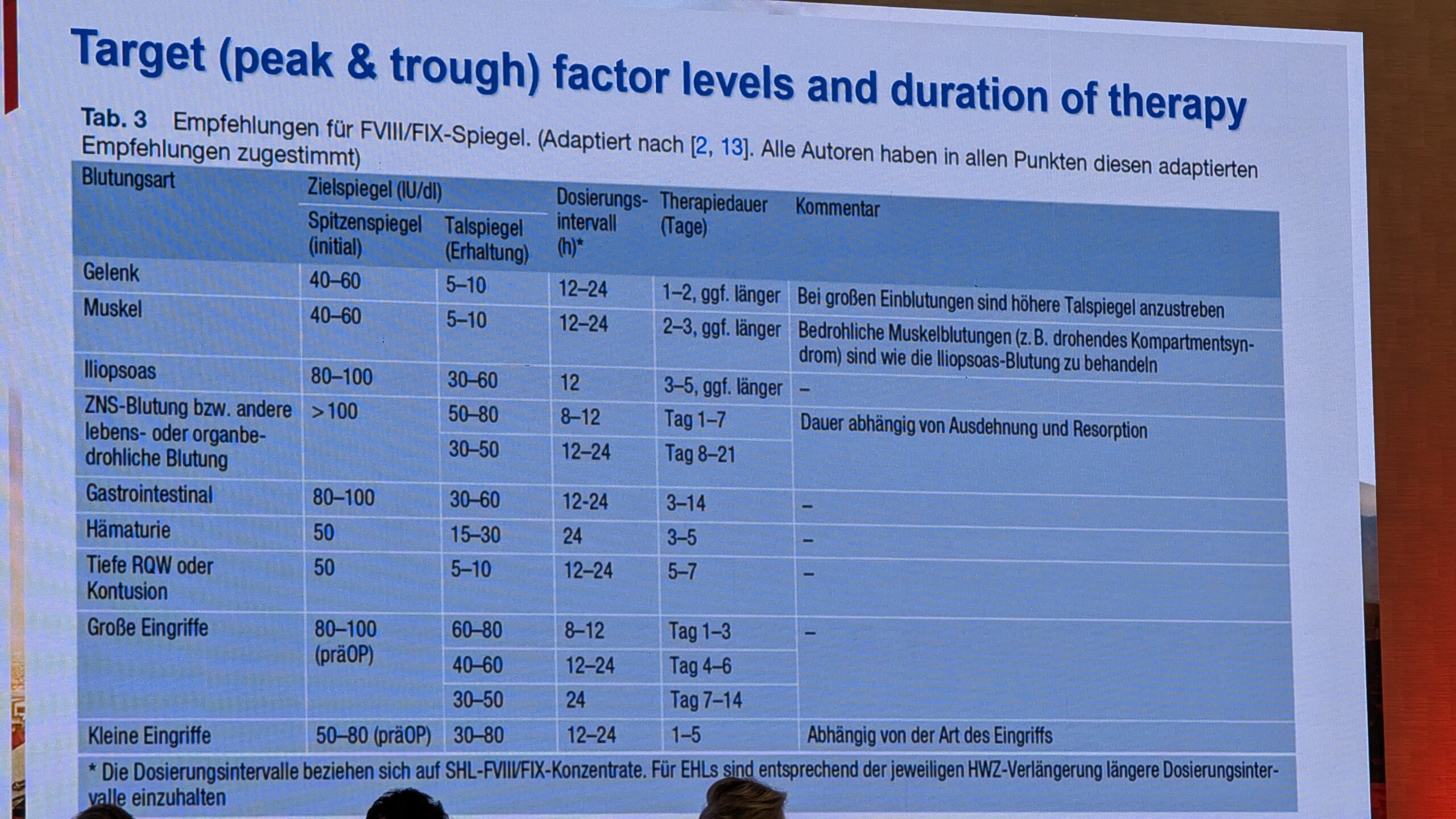
Soovitused on esitatud kokkuvõtvalt, et muuta teave võimalikult selgeks. Näiteks rõhutatakse ravi peatükis saavutatavaid faktorite tipptaset ja ravi kestust (nt soovitatakse kergete operatsioonide korral hoida asendusfaktori taset 10–15% hemofiilia A ja B korral). Juhistes rõhutatakse ka seda, et liigeste seisundit tuleks hinnata regulaarselt.
Juhise väljaandmist finantseeris Austria Hemofiiliaühing. Esineja rõhutas, et juhised on kirjutatud kõigile, kes on Austrias hemofiiliast huvitatud, sellega seotud või sellest mõjutatud. Kirjutamisprotsess ise, mis hõlmas aastaid kestnud arutelusid, parandas samal ajal ka Austria ravikogemust ja uute ravimeetodite tundmist.
1.3. Kuus kümnendit propageerimist: Austria Hemofiiliaühing – Thomas Schindl
Thomas Schindl andis ülevaate Austria Hemofiiliaühingu 60-aastasest ajaloost ja selle arengust.
Asutamine ja varane ajalugu (1960ndad)
Ühingu asutas 1966. aastal professor Lechner, kes oli pioneer. Lechner asutas Austrias esimese tervikliku hemofiiliakeskuse, registreerides patsiente Viinist, Alam-Austriast ja Burgenlandist. Algselt oli ühing asutatud peamiselt meditsiinilise seltsina, kolm aastat pärast WFH-i loomist. Lechneri algatusteks oli hemofiiliapatsientidele suunatud statsionaarse raviosakondade loomine. Värskelt külmutatud plasmal ja protrombiini kompleksi kontsentraatidel (krüopretsipitaat) ravi läbiviimine. Loodi lastele ka internaatkool, et tagada lastele regulaarne haridus ravi ajal.
Organisatsiooniline muutus ja programmid (1970ndad)
1970. aastal toimus oluline muutus, kui presidendiks sai Berma Williams, hemofiiliaga poja ema. See muutis organisatsiooni fookuse meditsiiniliselt ühingult tänapäevaseks patsiendiorganisatsiooniks. Samal aastal korraldas ühing kuuendat WFH konverentsi.
1970 ndatelalustati programmiga, mille üle ollakse eriti uhked: suvelaager lastele, 1972. aastal. See on teadaolevalt pikim kestev programm maailmas. Algselt taastusraviasutusena loodud laager on nüüd spordilaager, kus osaleb ka alati arst ja õde. Eesmärk on õpetada patsientidele süstimist, haiguse haldamist, füsioteraapiat ja julgustada füüsilist tegevust. Dr. Christoph Male-Dressler on olnud laagri meditsiiniline juht enam kui 20 aastat. Austria ühing pakkus toetust ka Ida Euroopa hemofiiliaga laste osalemisel nende laagris.
Kriis ja taastumine (1980ndad ja hilisemad aastad)
1980. aastad tõid suuretagasilöögi – HIV ja C-hepatiidi nakkused. Ühingu eesmärk suunati ümber, asutades erakorralise fondi. See programm, mis pakub juriidilist, psühhosotsiaalset ja rahalist abi ning sotsiaalmeetmeid, on kasutusel tänapäevani.
Pärast rasket aega õnnestus 1994. aastal võita kohtuasi viirusnakkuste hüvitamiseks, mis viis riikliku HIV-fondi loomiseni. Toimus organisatsiooniline ümberkorraldus, avati büroo ja võeti tööle osalise tööajaga töötaja. Meditsiinilise arengu toetamiseks käivitati 1998. aastal HEMOCARE programm, mis toetab Austria hemofiiliakeskuste tegevusi ja projekte. Programm toimib sponsorplatvormide kaudu ja edendab keskuste vahelist peer-to-peer suhtlust. 1990. aastatel asutati lisaks Austria hemofiilia talvelaager, kus õpetatakse patsiente ohutult sporti tegema.
Kaasaegne tegevus ja tuleviku väljakutsed
Ühing on aktiivne ka rahvusvahelises koostöös ja humanitaarabi programmides, mis hõlmavad faktori kontsentraatide annetusi Ida-Euroopasse (eriti Ukrainasse) ning meditsiinitöötajate praktikat Toimub tihe koostöö EHC ja WFH-iga.
Ühing annab välja 44 aastat ilmunud liikmete ajakirja “Faktor”, haldab veebisaiti ja sotsiaalmeediat ning on esindatud riiklikus meedias. Noorema põlvkonna jaoks asutati 2001. aastal Active Days noortekohtumised, mis keskenduvad spordile, vabaajale ja hariduse ning tööhõive küsimustele.
Viimastel aastatel on toimunud organisatsiooni mitmekesistamine. 2018. aastal asutati Women with Bleeding Disorders (Naised Verejooksuhäiretega) töörühm, mis keskendub naiste teemadele. 2019. aastal valiti ka uus, mitmekesisusele avatud juhatus.
Thomas Schindli hinnangul on tuleviku väljakutseks see, et väljakutsete mitmekesisus (vanuse, soo, diagnoosi, raskusastme või ravi alusel) võib viia kogukonna killustumiseni. Ühing peab keskenduma oma põhiväärtustele, tegelema püsiva ebavõrdsusega (nii Euroopas kui ka Austrias) ja hoidma ravi teemasid fookuses. Oluline lahendamata teema on ka vananev hemofiiliaga elanikkond, millega kaasneb vajadus luua teenuseid ja töörühmi kardiovaskulaarsete haiguste, vähiravi ja dementsuse juhtimiseks.
2. Sessioon – Barjääride murdmine: naiste tervis ja veritsushäired
2.1 Diagnoos ja nõustamine, naised ja tütarlapsed – Margareta Holmström
Margareta Holmström andis ülevaate verejooksuhäirete erinevatest aspektidest, mis puudutavad naisi ja tütarlapsi. Naine võib olla hemofiilia A või B kandja või tal võib olla Von Willebrandi tõbi (VWD) või trombotsüütide funktsiooni defektid.
Peamised sümptomid ja diagnoosimine
Peamised sümptomid, mis eristavad naisi verejooksuhäiretega teistest populatsioonidest, on raske menstruaalverejooks ja risk tõsisteks verejooksudeks sünnituse ajal.
Raske menstruaalverejooks (HMB), mida defineeritakse kui veritsust, mis ületab 80 milliliitrit menstruatsiooniperioodi jooksul, on juba iseenesest raske veritsus. HMB võib olla esimene märk verejooksuhäirest, mis võib ilmneda juba menarhe (esimese menstruatsiooni) ajal.
On oluline märkida, et umbes 20% kõigist naistest kannatab HMB all, ning 20–25% nendest omavad varjatud verejooksuhäiret, mis on enamikul juhtudel diagnoosimata.
HMB on seotud mitmete negatiivsete tagajärgedega:
- See põhjustab ebamugavust.
- Võib suurendada puudumisi koolist ja vähendada võimet osaleda spordis ja muudes füüsilistes tegevustes.
- Sellel on risk põhjustada rauapuudust ja rauapuudusaneemiat. See on eriti levinud verejooksuhäiretega naistel.
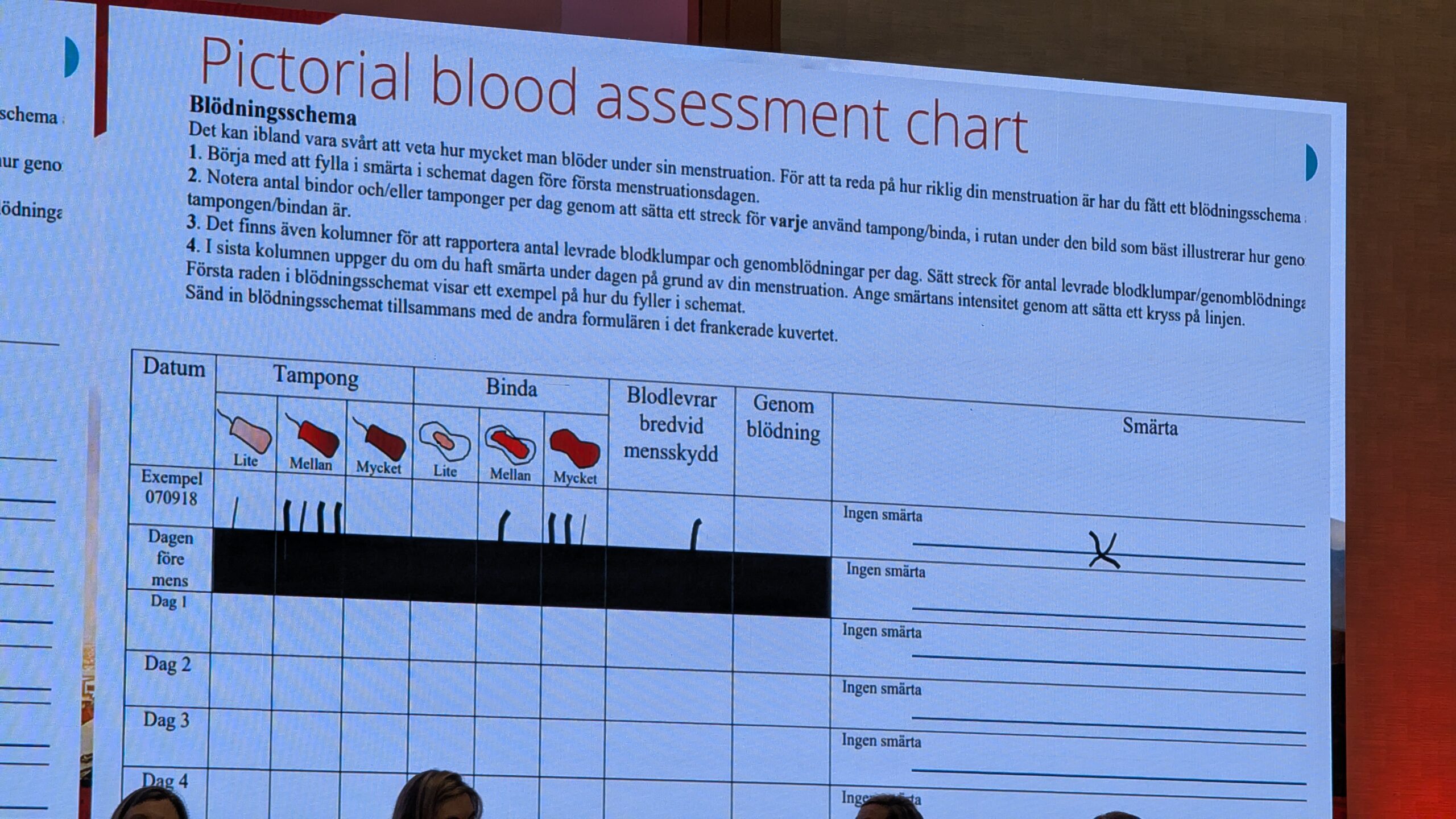
Diagnoosimisel on kasulik vahend Pictorial Blood Loss Assessment Chart (PBAC), mida saab kasutada patsiendi veritsuse jälgimiseks ja hindamiseks iga päev menstruatsiooni ajal. Tulemuste summeerimisel saadud punktid näitavad, kas tegemist on raske veritsusega või mitte. Lisaks on oluline teha vereanalüüs, et uurida punaliblesid ja aneemiat.
Hematoloogina ei tohiks keskenduda ainult faktori tasemetele. Vajalik on mitmekülgne lähenemine, mis hõlmata ka günekoloogi konsultatsiooni, et välistada muud HMB põhjused, nagu fibroidid, polüübid, koagulatsioonihäired või isegi pahaloomulised kasvajad.
Ravi ja rasedus
HMB ravivõimalused on järgmised:
- Traneksaamhape, mis on efektiivne ja suudab raskust vähendada.
- Desmopressiin (DDAVP), mida kasutatakse VWD tüüp 1, trombotsüütide funktsiooni defektide ja hemofiilia kandjate puhul.
- Spetsiifiliste faktoripuudulikkuste korral saab kasutada faktorikontsentraate või mittefaktorteraapiaid.
- Hormonaalne ravi (nt rasestumisvastased vahendid ja emakasisesed vahendid) on sageli väga efektiivne.
- Kindlasti ei tohi unustada rauapuuduse ravi tablettide või veenisiseste süstetena, mis on oluline aneemiast tingitud väsimuse raviks ja üldise tervise parandamiseks.
Raseduse ja sünnituse ajal toimub palju füsioloogilisi muutusi. Emake loodus on tark, kuna mitmed hüübimisfaktorid (nagu VWF ja FVIII) suurenevad, et minimeerida primaarset verejooksu riski. Siiski suureneb plasma maht, mis võib ringlust mõjutada.
Sünnitusjärgne verejooks (PPH) on tõsine mure, eriti arteriaalne veritsus, mis võib olla kuni 600 ml minutis. PPH riski suurendavad ka muud tegurid, mis ei ole seotud verejooksuhäirega, näiteks emaka atoonia emakas ei tõmbu korralikult kokku) või platsenta peetumine emakas.
Verejooksuhäirega naise raseduse ja sünnituse planeerimine nõuab:
- Riski hindamist emale ja teavet pärilikkuse kohta.
- Teades faktori taset enne rasedust, raseduse ajal ja raseduse lõpus.
- Kui naine on hemofiilia kandja ja laps on poiss, on risk hemofiiliaks 50%. Mõnedel peredel on võimalus kasutada ka rasedusaegset geneetilist diagnoosi (PGD).
- Multidistsiplinaarset lähenemist sünnitusel, mis kaasab ämmaemanda, anestesioloogi, hematoloogi ja vajadusel pediaatri.
Epiduraalanesteesia on üldiselt valikuvõimalus. Pärast sünnitust kasutatakse tavaliselt traneksaamhapet ja sõltuvalt diagnoosist faktorikontsentraate tavaliselt ühe kuni kahe nädala jooksul.
Esineja rõhutas, et naised peaksid olema aktiivsed ja informeeritud HMB osas, sest paljud naised ootavad diagnoosi liiga kaua – isegi 10–15 aastat.
2.2 Menopausi vanuse juhtimine – Nina Kovacevic
Nina Kovacevic keskendus menopausi ja perimenopausi etappidele naistel ja sedaverejooksuhäirete kontekstis.
Menopaus on defineeritud kui 12 järjestikust kuud ilma menstruatsioonita. See saabub tavaliselt vanuses 45–55 aastat, keskmiselt umbes 51. eluaastal. Tähtis on teada, et elu ei lõpe 50-aastaselt, vaid umbes 31 aastat elust on veel ees.
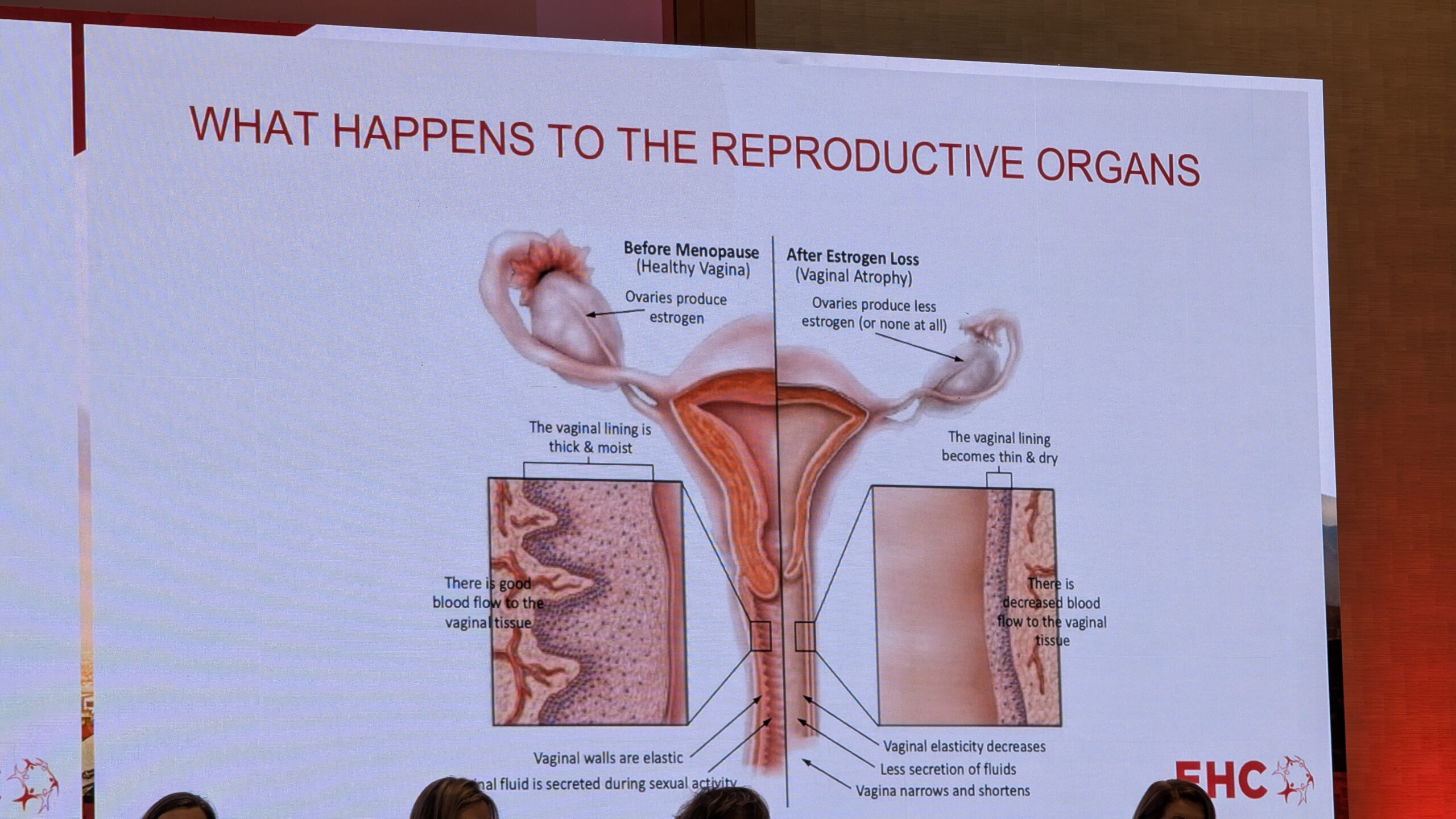
Perimenopaus on üleminekuperiood, kus hormoonide (östrogeeni ja progesterooni) tase hakkab langema, progesterooni tootmine menopausis lakkab ja östrogeeni tase stabiliseerub madalal tasemel. Östrogeeni ja teiste hormoonide puudus mõjutab tervet keha, mitte ainult emakat ja munasarju.
Kuigi menstruaalverejooksu puudumine võib olla “täisesti OK”, muutub tupe limaskest madala östrogeenitaseme tõttu õhukeseks ja kuivaks. See põhjustab genitourinaarseid sümptomeid menopausis (GSM), nagu tupe elastsuse vähenemine, kuivus ja ebamugavustunne. Need sümptomid võivad negatiivselt mõjutada elukvaliteeti ja seksuaalelu. Seks aga on oluline osa elust, ja seda ka keskeas.
Üldised menopausi sümptomid hõlmavad kuumahooge, öist higistamist, nahamuutusi, meeleolumuutusi ja väsimust.
Verejooks ja ravi menopausi ajal
Põhisõnum naistele menopausi järgselt – ükski veritsus või eritis ei ole normaalne pärast 12 kuud menstruatsiooni puudumist. Igasugune punakas või pruunikas eritis tupest nõuab kohest günekoloogi külastust, et viia läbi uuringud (nt ultraheli), et välistada tõsised põhjused, pahaloomulised kasvajad.
Perimenopausi raskete, ebaregulaarsete verejooksude raviks on valikud järgmised:
- Traneksaamhape ja hüübimisfaktori taseme mõõtmine.
- Hormonaalsed vahendid, nagu emakasisesed süsteemid, kombineeritud suukaudsed kontratseptiivid või progestiinid.
- Kirurgiline lähenemine (nt endomeetriumi ablatsioon, mille käigus eemaldatakse ainult emaka siseosa) juhul, kui veritsus on väga raske või seda ei saa peatada, või kui esineb fibroome või polüüpe.
Hormoonasendusravi (HRT) asendab östrogeeni ja progesterooni (viimast emaka kaitseks) sümptomite leevendamiseks. Kuid kõik naised ei tohi hormoonravi kasutada.
GSM-i ja teiste sümptomite mittemedikamentoosne ravi:
- Niisutajad ja libestid, et muuta seksuaalvahekord meeldivamaks.
- Regulaarne seksuaalne aktiivsus, mis suurendab verevoolu tuppe ja aitab säilitada elastsust (seksuaaltegevuse vältimine ei lahenda probleeme).
- Vaagnapõhjalihaste harjutused ja lõdvestustehnikad (nt jooga), mis aitavad leevendada valu ja ebamugavust.
- Laserravi genitaalpiirkonnas, mis on mitteinvasiivne ja aitab kaasa uute kudede moodustumisele.
Esineja rõhutas ka elustiili muutuste olulisust. Suitsetamisest loobumine on hädavajalik, kuna suitsetamine muudab emaka limaskesta õhemaks ja vanemaks. Oluline on ka igapäevane 30-minutiline füüsiline koormus, mis tõstab südame löögisagedust. Seejuures- iga naise keha on unikaalne ja ravi peab olema individuaalne, et leida parim soovitud tulemus.
2.3 Sümptomaatiline kandja – Patsiendi perspektiiv – Brina Zaman
Brina Zaman jagas oma isiklikku ja emotsionaalset teekonda hemofiiliakandjana 20 aasta jooksul. Ta rääkis, et on siin naise, ema ja kogukonna juhendajana.
Tema teekond algas võitlusega rasestumise ja viljatusega. Pärast ebaõnnestunud katseid rasestuda ja normaalsete testitulemuste saamist suunduti kehavälisele viljastamisele (IVF). IVF-i tulemusel arenes 21 folliikulit ja loodi külmutatud embrüod. Kuid ta kannatas raske munasarjade hüperstimulatsiooni sündroomi (OHSS) all, mis nõudis kahenädalast haiglaravi. Seejärel järgnesid südantlõhestavad raseduse katkemised.
Esimene sünd ja šokk
Esimese õnnestunud raseduse ajal veritses ta kaks korda, ja isegi lihtne WC-külastus oli hirmutav. Kohe pärast esimest sünnitust kaotas ta peaaegu ühe liitri verd.
Šokk saabus mõni aeg hiljem, kui lastearst märkas vastsündinud pojal midagi ebatavalist. Nad suunati otse lastehaiglasse, kus pojal diagnoositi mõõdukas hemofiilia A (Faktor VIII puudulikkus). See diagnoos muutis nende elu igaveseks, kuid nad leidsid tuge kohalikust kogukonnaseltsist. Esineja rõhutas, et nende poeg on õnnelik ja seiklushimuline poiss ning nad soovivad talle täisväärtuslikku elu, mis on nõudnud küll rohkem planeerimist.
Esialgu toimusid haiglakülastused pojaga iga veritsuse korral. Kolm aastat hiljem, kui poeg oli kolmeaastane, anti perele luba alustada regulaarset profülaktilist ravi kodus. See periood oli stressirohke ja kurnav, kuna vanemad pidid õppima tegema süsti veeni iga kolme päeva tagant.
Teine rasedus ja kergendus
Teise lapse saamise küsimus tekitas aastaid kõhklusi, kuna Brina tundis hemofiilia geeni kandjana endas suurt süüd. Küsides endalt, kas tal on õigus tuua maailma veel üks laps hemofiiliaga, või kas see on liiga suur koormus olemasolevale lapsele. Nad pöördusid geneetiku poole, kes aga tagasi ei helistanud. Lõpuks otsustasid nad proovida uuesti külmutatud embrüodega, ja ta jäi rasedaks esimesel katsel.
Neli päeva pärast teise raseduse lõppu kannatas ta uuesti, seekord veelgi raskema verekaotuse all, kaotades 1.3 liitrit verd. Ta sattus intensiivravi osakonda ja sai rauainfusiooni.
Suurim kergendus saabus tundi hiljem, kui arst teatas talle unustamatu sõna: “Teie vastsündinud beebi faktori tase on teada. Lapsel ei ole hemofiiliat.”. Kergendus oli tohutu, sest soov saada teine laps oli kaalunud üle hirmu hemofiiliaga lapse võimalikuks sünniks.
Lõpetuseks jagas esineja oma sõnumit: ta ei valinud seda teed, kuid ta valis armastuse elu kingituste eest, seljatades nii hirmu. Ta räägib oma kogemusest selleks, et keegi teine, kes seda teekonda läbib, ei tunneks end nähtamatuna või üksinda.
3. Ravimitööstuse toetatud sümbioosium 1: „Veritsemisest kaugemale: vaimne tervis veritsushäirete kogukonnas“
3.1 Hemofiilia vaimse tervise koormus: Kuidas saab ravivalik aidata? – Dr Evelien Krumb
Dr. Evelien Krumb andis ülevaate hemofiiliaravi arengust ja selle mõjust patsientide elukvaliteedile ning vaimsele tervisele.
Ravi ajalooline taust ja areng
1970. aastatel Ameerika Ühendriikides oli eluohtlikku verejooksu võimalik ravida vaid toetavate meetmetega. 1960. ja 1970. aastatel said kättesaadavaks krüopretsipitaat ja desmopressiin (DDP), mis võimaldasid spetsiifilisemalt ravida ka rasedusi. Kuigi tehti suuri investeeringuid tervemate faktorravimite väljatöötamiseks, jäi see areng varju 1980. aastatel, mil HIV ja C-hepatiidi epideemiad levisid hemofiilia populatsioonis saastunud vereproduktide kaudu, põhjustades suurt haigestumust ja suremust.
Tänu edasistele arengutele biotehnoloogiates ja plasmatoodete viiruse inaktiveerimismeetodites muutusid kättesaadavaks ohutumad ravimid. Võimaldasid ka verejookse tõhusamalt ennetada ja vähendada. Need ravimeetodid täiendati 2000. aastate alguses ning 2010. aastatel neid täiendati veelgi, võttes kasutusele pikendatud poolväärtusajaga ravimid, vajaduspõhised ravimeetodid (on demand treatments) ning esimesed mittefaktortooted.
Ravi fookus on liikunud elude päästmiselt patsientide elukvaliteedi parandamisele. Praegu on kasutusel profülaktiline ravi, pikendatud poolväärtusajaga ravimid, mittefaktortooted ja geeniteraapia, mis võimaldavad elukvaliteedi paranemist.
Mõju vaimsele tervisele ja elukvaliteedile
Hemofiilia mõjutab paljusid igapäevaelu aspekte: haridus, töö, füüsiline koormus, sport, reisimine ja inimestevahelised suhted. Vaatamata sellele, et fookus on liikunud elukvaliteedile, siiski on vaimse tervise häirete levimus hemofiiliahaigetel noortel kõrgem kui üldpopulatsioonis.
Vaimse tervise mõõtmine kliinilistes uuringutes on keeruline. Seda hinnatakse tavaliselt valideeritud vahendite abil, mis hõlmavad emotsionaalseid ja sotsiaalseid domeene. Kuid see on seotud üldise elukvaliteedi hindamisega. See tähendab, et hemofiiliaga seotud vaimse tervise täielik kogemus ei pruugi olla nende vahenditega täpselt kajastatud. Täiendatud küsimustikud hõlmavad siiski ka spetsiifilisemaid vaimse tervise aspekte, nagu stigma ja identiteet. Psühholoogilise toimetuleku hindamine tulevikus on väga oluline.
Krumb rõhutas, et õige teraapia valik leevendab olulist vaimset koormust, mitte ainult patsiendil, vaid ka nende perekonnal. Eraldi murekoht on naised ja kandjad, kellel on sageli kahekordne roll – nad on nii lähedased kui ka ise sümptomitega isikud.
Krumb tõi esile, et teraapia mõjutab patsiendi aktiivset elustiili ja füüsilist aktiivsust. See peaks olema koostöös kokku lepitud raviarstidega. Füüsiline aktiivsus hõlmab mitte ainult sporti, vaid ka igapäevaseid tegevusi, nagu töö, ostlemine ja kõndimine. Samuti on oluline arvestada, et patsiendid on kaasatud otsustusprotsessi multidistsiplinaarsetes meeskondades.
3.2 Vaimse koormuse lahendamine hemofiilia korral: Patsiendi ja psühholoogi vaatenurk – Marius Tanese ja Catia Damiao
Patsiendi perspektiiv (Marius Tanese)
Marius Tanese rääkis hemofiilia diagnoosist tingitud vaimsest koormusest isiklikus ja kogukonna vaatenurgast. Ta märkis, et vaimse koormuse allikaks on ebapiisav arusaam haigusest ja sümptomitest. Ta tõi esile, et paljudel hemofiiliaga patsientidel, sümptomaatilise veritsusega liigesesse, on liigesed ja põlved sarnased eakate inimeste liigestega juba lapsepõlves. See põhjustab vaimset koormust, millega tuleb tegeleda lisaks haiguse raviga.
Oluline koormus oli depressioon, mille põhjustab pidev valu ja kannatus, ravimite puudus ja verejooksud. Olukord mõjutas mitte ainult teda, vaid ka tema vanemaid, mis omakorda suurendas temas vaimset pinget.
Sotsiaalne isolatsioon ja madal võimekus enese eest hoolitseda on olnud samuti väljakutse. Kogemust tööturul: oli aegu, mil ta sai töötada, kuid pidi sagedaste põlveprobleemide tõttu töölt puuduma või isegi tööst loobuma mitmeks aastaks. See mõjutas tema iseseisvumist. Suuremad kulutused, eriti kui valitsus enam ei paku varasemat harjunud toetust. Ta märkis, et Rumeenias on kahjuks paljud 80ndatel ja 90ndatel sündinud hemofiiliaga patsiendid liigeseprobleemide tõttu invaliidistunud.
Psühholoogi vaatenurk (Catia Damiao)
Psühholoog Catia Damiao kinnitas, et tema kliiniline kogemus näitab ärevuse ja depressiooni suurt levimust hemofiiliahaigete seas. Lisaks on olemas suur trauma komponent, mis tuleneb isiklikest veritsuskogemustest, ravist ja tervishoiuteenuste puudustest. Paljud tema patsiendid ei ole varem psühholoogilist nõustamist saanud, mistõttu on neil vaja turvalist ruumi, kus nad saaksid tegeleda haigusega seotud vaimse koormuse ja kannatustega, mis mõjutavad nende elukvaliteeti.
Vaimse tervise murede allikad on:
- Haiguse ja ravi kohta liiguvad segased uskumused ja kahtlused (eriti uute ravimeetoditesuhtes).
- Vajadus kirurgilise sekkumiste järele ja mure seoses taastumisega. Faktorravi efektiivsus.
- Psühhosotsiaalsed aspektid, nagu madal enesehinnang ja enesetaju.
- Perekondlikud ja sotsiaalsed probleemid. Perekonna tugi ja abi, isolatsioon ning sotsiaalne ja rahaline toetus.
Damiao tõi esile, et probleemid kipuvad muutuma sõltuvalt patsiendi elutsükli etapist. Täiskasvanueas on fookus tööl ja tervisel. Noortel aga vastutus ning juurdepääs tööturule.
Psühholoogilise toe pakkumine
Psühholoogilise tugi on vestlus diagnoosi järgselt patsiendi või tema vanematega. Hinnatakse haiguse aktsepteerimist ja arusaamist haigusest ning selle tagajärgedest. Oluline tuvastada patsiendi toimetulekumehhanismid ja leida viise kriisidega tegelemiseks. Soov saada psühholoogilist tuge peab olema isiklik otsus ja soov.
3.3 Laps sündis hemofiiliaga: Vanema perspektiiv – Blanka Krivicic Hyrat
Blanka Krivicic Hyrat jagas oma vaatenurka hemofiiliaga lapse kasvatamise emotsionaalsetele ja praktilistele aspektidele.
Tema poeg sai mõõduka hemofiilia A diagnoosi kahekuuselt, pärast seda, kui märgati kummalist turset ribidel. See muutis arstide ettepaneku järgselt “kontrollime igaks juhuks” järgmisel hommikul vastuste saabudes nende elu igaveseks. Reaktsioon oli šokk ja päev täis nutmist. Pisaraid pühkides hakkas ta uurima hemofiilia kohta. Ravivalikute ja uute ravimite arendamise kohta. See andis talle lootust poja tuleviku suhtes.
Ema suurimad väljakutsed
Blanka suurim hirm pidev oht lapse vigastuste ees, hirm mis haarab kogu aeg tema mõtteid. See hirm on viinud lapse üle kaitsmiseni ja püüdeni luua lapse ümber keskkond, mis oleks vaba ohust. Ta tunneb, et ei ole suuteline seda hirmu endas välja lülitama.
Teised väljakutsed:
- Ebakindlus tegevustes: Raske aru saada, millised tegevused on lapsele lubatud ja millised mitte.
- Kahtlused ravi osas: Eriti väiksemate õnnetuste puhul kahtleb pidevalt, kas manustada ravi või mitte. Kunagi pole oma otsusega rahul.
- Sotsiaalne elu: Otsustamisraskused, kellele lapse haigusest rääkida. Inimesed reageerivad hemofiilia diagnoosi kuuldes sageli paaniliselt hirmunult. Blanka ei soovi, et poega nähtaks vaid kui hemofiiliahaiget.
- Vabaduse puudumine: Spontaansed reisile minekud pole enam võimalikud; planeerimine on alati vajalik, see aga piirab neid pidevalt.
Suur võitlus on profülaktilise ravi manustamine. See oli algusest peale stressirohke ja tekitas ärevust. Mõnikord kestis protseduur kauem kui 45 minutit ja lapsel oli üle 10 ebaõnnestunud süstekohta, põhjustades traumat nii lapsele kui ka emale. Blanka tunnistab, et püüdis varjata oma stressi. Teeseldes sageli, et kõik on korras, isegi kui see nii ei olnud. Kõik selleks, et laps ei tunneks tema hirmu.
Toetus ja lootus
Hoolimata väljakutsetest aitas Blankat:
- Kohalik kogukond: Ühendus kohaliku hemofiilia kogukonnaga Horvaatias. Organisatsiooni president ja liikmed on alati kättesaadavad küsimustele vastamiseks, teadmiste jagamiseks ja hädaolukordades aitamiseks.
- Hariduslaagrid: Nende Seltsi korraldatud hariduslaagrid pakuvad väärtuslikku teavet ja võimalust suhelda teistega, kes läbivad sama teed. Kaasteelistega rääkimisest ja olukorra jagamisest on talle olnud suur abi.
- Ravi kättesaadavus: Nad elavad piirkonnas, kus on kättesaadavad enamik ravivõimalusi ja riiklik kindlustus katab kulud. Uute toodete kättesaadavus tähendab lapsele vähem valulikke protseduure ja vähem traumat.
- Tervishoiumeeskonna toetus: Arstid ja õed juhendavad neid ravi osas, vastavad lõpututele küsimustele ja pakuvad emotsionaalset tuge.
Blanka lõpetas rõhutades, et hoolimata kõigist väljakutsetest on tema suurim rõõmuallikas nende väike poiss, tema naeratus ja energia.
3.4 Kuidas saab laiem tervishoiumeeskond toetada hemofiiliahaigeid vaimse koormuse korral? – Catia Damiao ja Dr Evelien Krumb
Catia Damiao ja Marius Tanese arutasid Marius Tanese vastuses uute ravimeetodite positiivse psühholoogilise mõju üle. Marius Tanese leidis, et uut tüüpi ravimeetodid on andnud märkimisväärse positiivse psühholoogilise mõju. Ta tõi näiteks kaasmaalased Rumeeniast, kelle elukvaliteet paranes drastiliselt uute ravimite tulekuga. Tänu uutele ravidele saavad hemofiiliahaiged elada normaalset elu, neil võivad olla perekonnad ja lapsed ning nad saavad töötada (näiteks juristina või ärivaldkonnas).
Vaimse koormuse ennetamise parim viis on sellest rääkida ja sellele mõelda. Catia Damiao ja Marius Tanese tõid esile mitu toetavat aspekti:
- Tugev terapeutiline liit: Tugev terapeutiline liit patsiendi ja arst vahel ning multidistsiplinaarse meeskond aitab psühholoogilise toe vajadust hinnata.
- Teadmiste jagamine ja koostöö: Teadmiste ja kogemuste jagamine ning partnerlus hematoloogidega on ülioluline.
- Kogukonna toetus: Marius Tanese rõhutas Euroopa Hemofiilia Konsortsiumi (EHC) ja teiste organisatsioonide toetust, mis on aidanud tagada õige hoolduse ja ravi kättesaadavuse ka riikides, kus see algselt puudus.
- Aktiivne elustiil: Ravimeeskondpeaks arvestama ravivalikute mõju patsiendi aktiivsele elustiilile ja füüsilisele tegevusele (sealhulgas tööle, ostlemisele ja kõndimisele).
- Ravimi valik: Dr. Krumb rõhutas, et õige teraapia valik võib vähendada vaimset koormust nii patsiendil kui ka lähedastele.
Dr. Krumb lõpetas, rõhutades Blanka Krivicic Hyrat’ kogemuse olulisust kogukonna ja tervishoiuteenuse osutajate jaoks. Laiem ravimeeskond, sealhulgas arstid ja õed, peavad toetama patsiente mitte ainult meditsiiniliselt, vaid pakkuma ka emotsionaalset tuge.
4. Tööstussümpoosion 2: „Hoolitse oma tulevase liigeste tervise ja liikuvuse eest: mida arvestada ja millele juba täna mõelda“
4.1 Pikaajalise liigeste tervise tagamine: tänaste valikute ja otsuste mõju – Dr. Christoph Könings
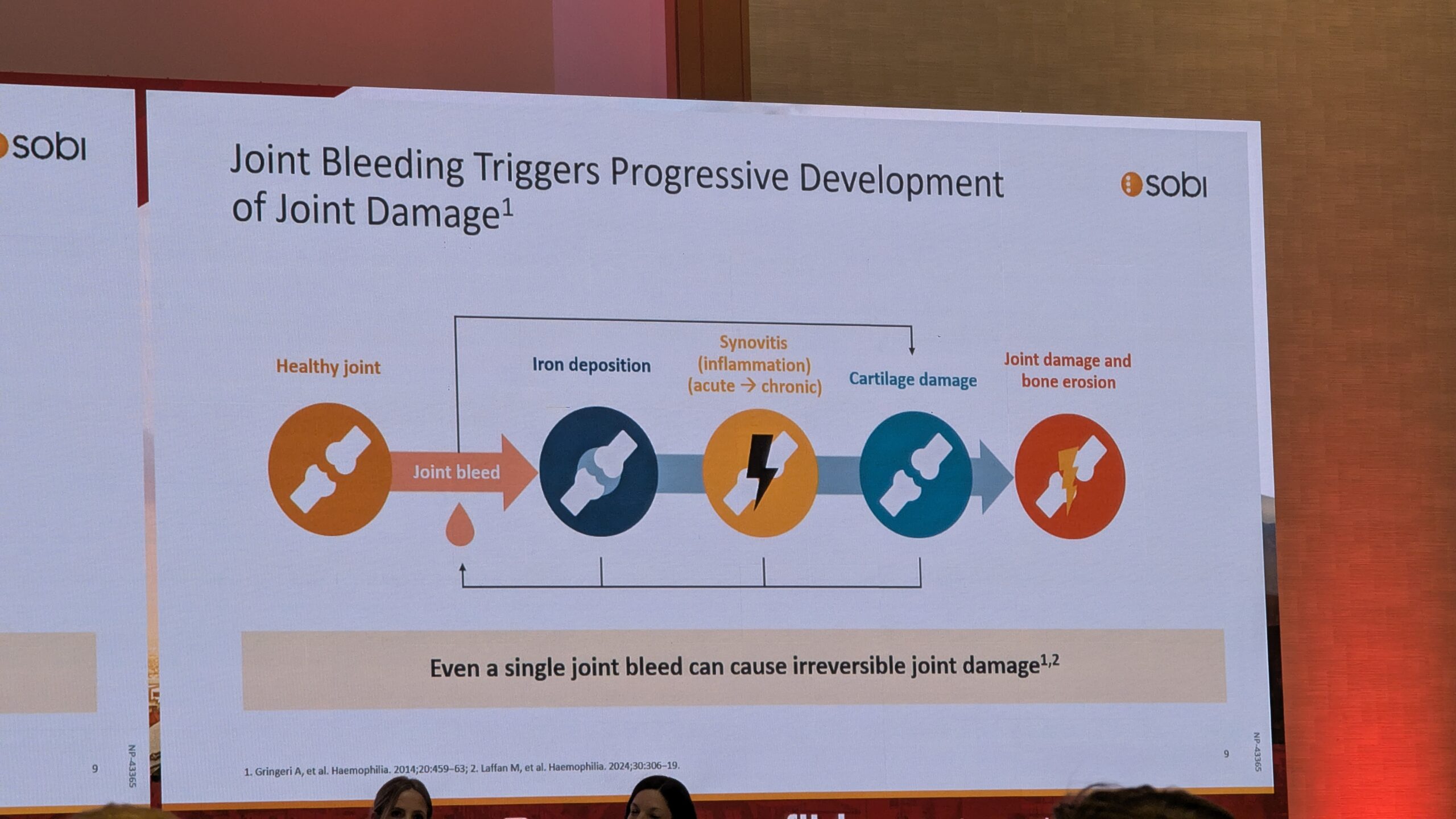
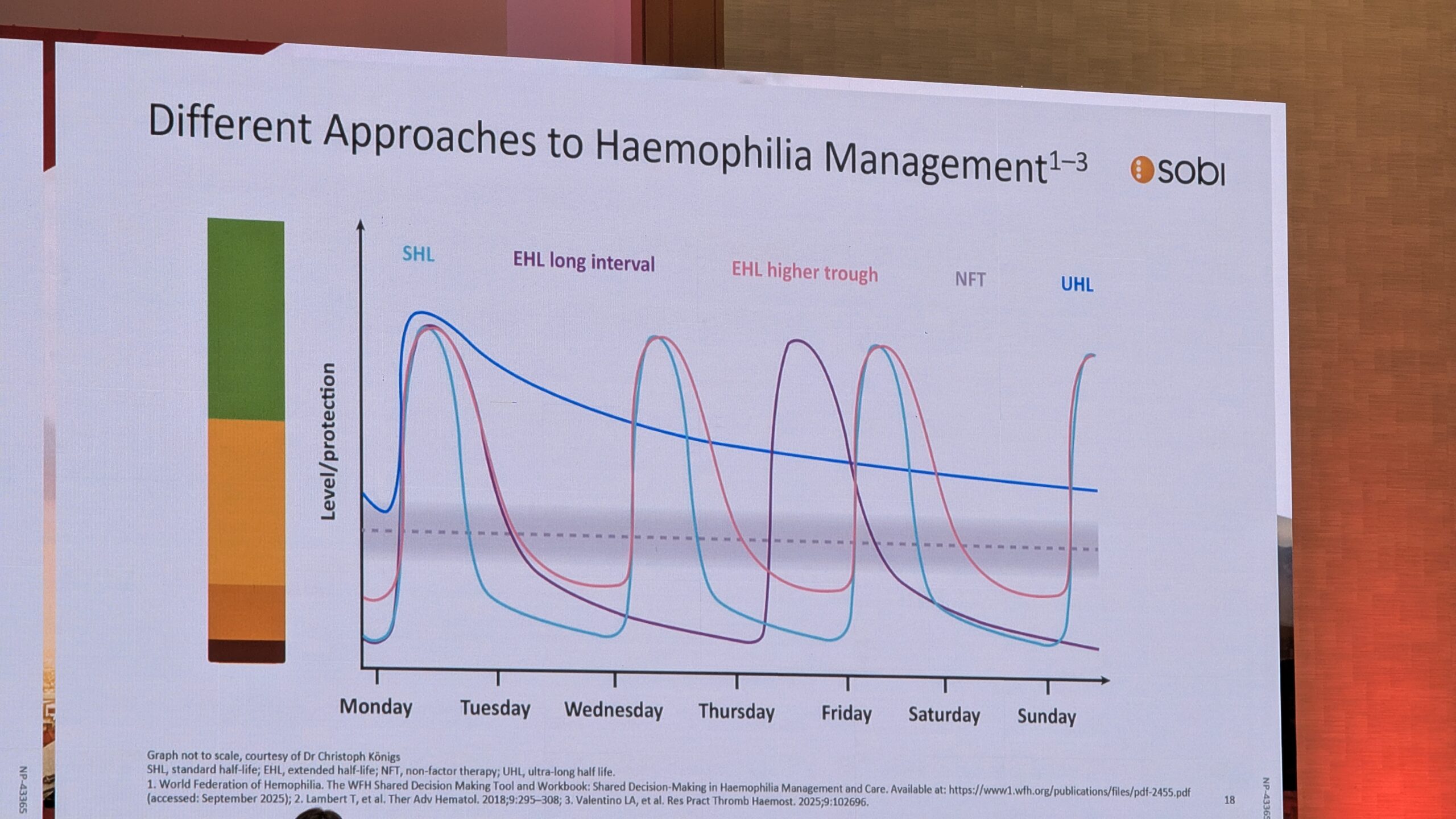
Dr. Christoph Köningsi ettekanne keskendus sellele, et liigeste pikaajalise tervise kaitsmisel on tänastel valikutel ja otsustel kaugeleulatuv mõju. Ta selgitas, et liigeseverejooksud (hemartroos) põhjustavad valu, turset ja soojatunnet ning teevad liikumise valulikuks või võimatuks. Liigeses olev veri halvendab organismi võimet liigest kontrollida. Königs rõhutas, et varajane ravi on ülioluline, sest mida kauem viivitada, seda suurem on tekkiv kahju.
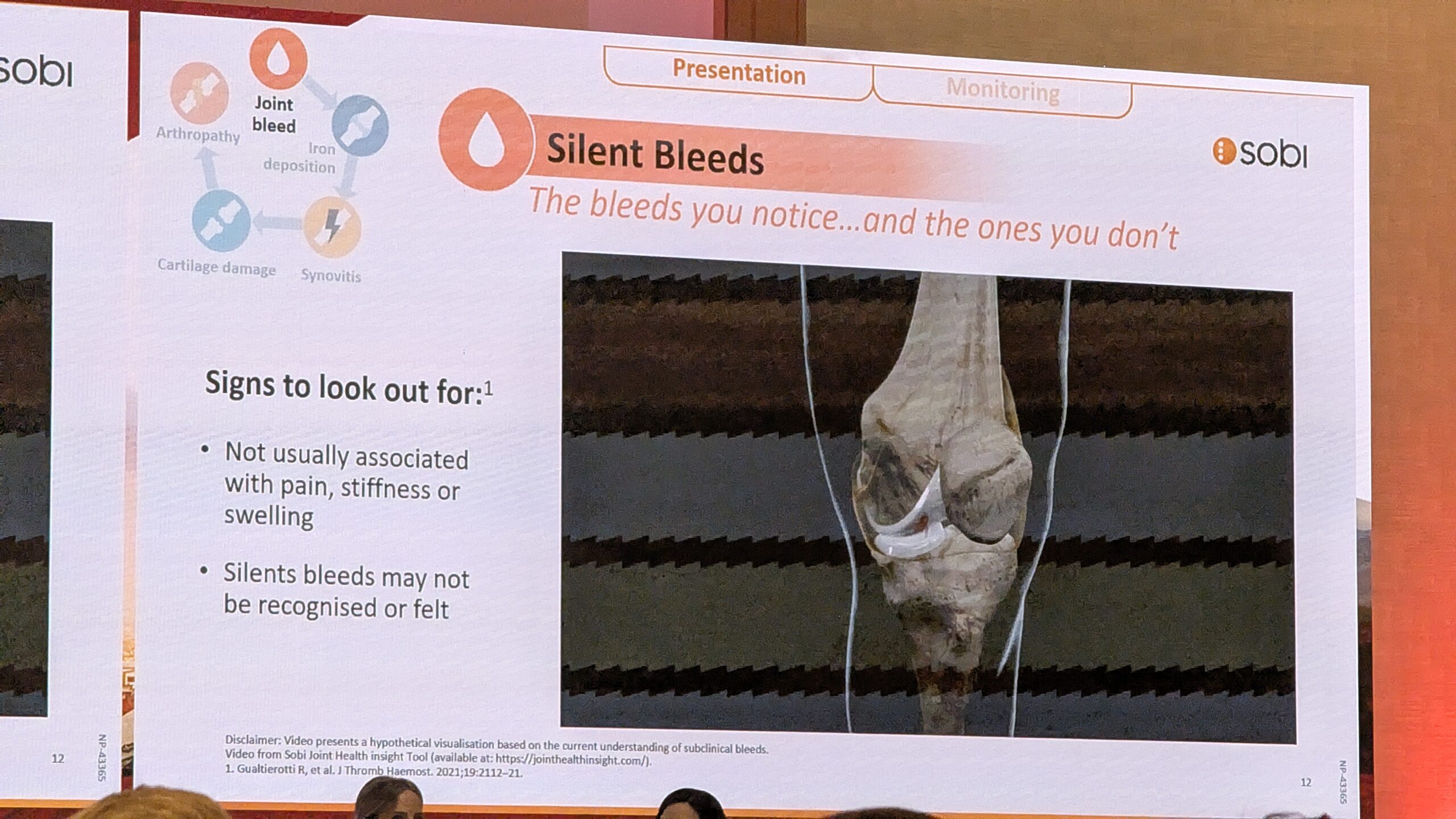
Liigeste tervise säilitamiseks on hädavajalik pidev jälgimine ja profülaktika, mis parandab liigeste tervist, vähendades verejooksude sagedust ja ulatust. Dr. Königs tõi esile nn „vaiksete verejooksude“ (ingl. silent bleeds) probleemi. Kuigi need pole alati nähtavad, kuna tegu on vaid väikeste verehulkadega, ladestub neist raud liigesesse, põhjustades liigesekahjustusi. See rõhutas vajadust tunnetada ja jälgida liigeste tervist ka siis, kui otseseid suuri probleeme ei paista. Liigeste struktuurse tervise hindamiseks on Dr. Königs sõnul elegantne tööriist ultraheli, mille abil saab näiteks tuvastada sünoviiti, jälgides sageli kuut kõige enam mõjutatud liigest: põlvi, küünarnukke ja pahkluid.
Liigeseprobleemide puhul on varajane sekkumine kriitilise tähtsusega, et vältida luu ja kõhre struktuurset kahjustust, mis võib viia liigese deformeerumiseni. Üks levinud probleem on sünoviit (liigest määrdeainega varustava koe põletik). Põletiku korral sünovium paisub ja muutub madalama kvaliteediga koeks, mis omakorda soodustab edasisi verejookse ja liigesekahjustusi. Dr. Königs toonitas ka kaasaegse ravi (nt pikema poolestusajaga tooted) võimalusi liigeste kaitsmisel, kuid rõhutas, et isegi vanemate (lühema poolestusajaga) toodetega saab liigeseid kaitsta, kui osata neid õigesti kasutada. Kõige tähtsamaks pidas Dr. Königs avatud dialoogi ravimeeskonna ja patsiendi vahel. Paljud patsiendid valivad esmaseks eesmärgiks aktiivse elustiili säilitamise. See annab neile isiklikku eneseväärikust ja kindlustunde, et nad on kaitstud.
4.2 Tuleviku liikuvuse kaitsmine: tegevused, mida saate kohe ette võtta – Ruth Elise Dybvik Matlary
Ruth Elise Dybvik Matlary rõhutas füsioterapeudi keskset rolli multidistsiplinaarses meeskonnas. Füsioterapeudid saavad aidata säilitada liigeste funktsiooni, ennetada liigeste halvenemist ja suunata inimesi parema elukvaliteedi poole. Nad annavad personaalset nõu, toetavad enesejuhtimist ning õpetavad ära tundma sümptomeid ja varajasi liigeste kahjustusi. Monitooringu käigus on oluline hinnata lisaks standardprotseduuridele ka indviduaalseid isiku funktsionaalseid võimeid.
Füüsilise Aktiivsuse Eelised ja Valuravi
Füüsiline aktiivsus (FA) võimaldab paranemist üldisest heaolus ja vaimses tervises ning kuni südame-veresoonkonna tervise hoidmiseni. Eriti hemofiilia korral füüsiline aktiivsus ka verejookse vähendada. Liigeste tervena hoidmiseks on liikumine hädavajalik. Matlary rõhutas, et tuleks valida eesmärgipärased harjutused: näiteks jõutreening üldise füüsise tugevdamiseks, teatud liigutuste sooritamise harjutamine painduvuse parandamiseks või harjutused pikema aja jooksul kõrgenenud pulsiga vastupidavuse treenimiseks. Valuravi koha pealt varajane verejooksu ravi ning füsioteraapia aitavad valu leevendada. Mõnikord on nii võimalik isegi asendada valuvaigisteid.
Lisaks mehaanilisele kaitsele (nt paindlikkus) tõi üks patsient esile uuringud, mis demonstreerivad seost lihasmassi ja liigeste põletiku vahel. See näitab, et füüsiline tegevus, eriti lihasmassi kasvatamine, võib omada ootamatut põletikuvastast toimet. See annab füsioterapeudi rollile veelgi suurema tähtsuse, eriti ka juba kahjustatud liigeste puhul, kus on võimalik parandada liigeste funktsiooni ja perifeerset seisundit, isegi kui struktuurset muutust oodata ei saa.
Nõuanded Erinevatele Vanusegruppidele
Matlary jagas nõuandeid, kuidas aktiivseks jääda või aktiivseks muutuda:
- Laste puhul on kõige tähtsam julgustada tegevsutes osalemist ja keskenduda tegevustele, mis pakuvad neile naudingut. Positiivsed seosed liikumisega aitavad kaasa heale kehatunnetusele ja arendavad motoorselt.
- Noorukite puhul on väljakutseks hoida noori aktiivsena. Üheltpoolt vältides liiga riskantseid tegevusi. Teiselt poolt otsides tegevusvaldkondi, mis ei provotseeri verejookse.
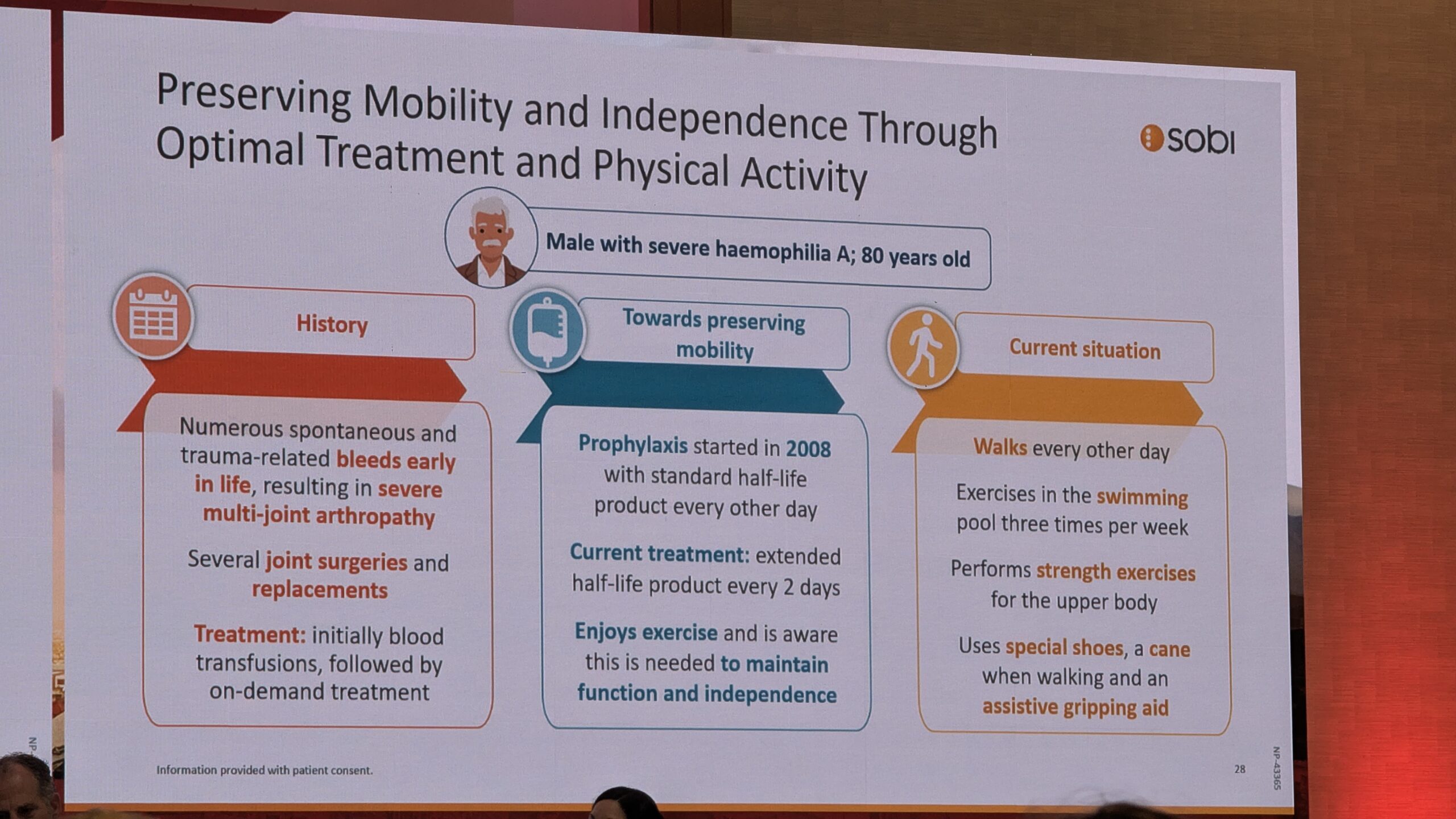
- Täiskasvanutel ja vanematel inimestel soovitas ta keskenduda jõu- ja tasakaalutreeningule, et ennetada kukkumisi ja edendada iseseisvust. Illustreerimiseks esitas ta 80-aastase mehe loo, kellel oli ulatuslik liigesekahjustus, kuid kes suutis regulaarselt tegeleda kõndimise ja ujumisega, näidates, et isegi liikumispiiranguga on aktiivsena püsimine võimalik.
Matlary sõnul on liikuvuse ja liigeste tervise säilitamise võti püsiv aktiivsus, varajaste muutuste ja liigesefunktsiooni ebamugavuse äratundmine, oma keha kuulamine ja koostöö tervishoiumeeskonnaga. Parim nipp aktiivsena püsimiseks on leida tegevus, mis toob naudingut, sest selle juurde on lihtsam jääda.
4.3 Piiride ühine uurimine: tasakaal ettevaatlikkuse ja lahtilaskmise vahel – Angelika Isler
Angelika Isler jagas oma isiklikku ja sügavalt emotsionaalset teekonda emana hemofiiliaga poja kasvatamisel. Diagnoosi saamine viiekuusele pojale oli perele šokk, mis tõi kaasa pideva küsimuse: „mis on okei ja mis mitte?“.
Ettevaatlikkuse õpetamine ja kehateadlikkus
Suurimaks väljakutseks vanemana oli leida tasakaal lapse vabaduse ja turvalisuse vahel, eriti olukordades nagu mänguväljakul. Tuli kaaluda, kas lubada lapsele suurt liumäge või tuli eelistada turvalisemat tegevust. Vanematena tekkis meil pidev sisemine konflikt: usaldada last ja samal ajal tunda hirmu, et ta end vigastab. Isler pidi õpetama pojale ettevaatlikkust, selgitades, miks on parem kõndida jooksmise asemel ja alla ronida hüppamise asemel. Veelgi olulisem oli õpetada kuidas õigesti maanduda ja liikuda. Kehateadlikkuse arendamine ja oma keha kuulamise õpetamine oli hädavajalik.
Profülaktika alustamine
Profülaktiline ravi lisati perekonna igapäevaellu ja sporditegevustesse. See tähendas teadlikkust sellest, millal on vaja doos vahele jätta ja millal lisada doos. Lasteaedades ja algkoolides pidi ta õpetama ka õpetajaid kuulama lapse keha ja reageerima koheselt, kui poiss tundis midagi ebatavalist. See andis lapsele ka suurema iseseisvuse, kuna ta õppis ise verejookse ära tundma ja ravi paluma. Isler rõhutas, et ta soovib, et poeg õpiks usaldama oma keha ja paranemisvõimet, leidma tasakaalu aktiivsuse ning puhkuse vahel, kasvaks tugevaks, iseseisvaks noormeheks. Tema soovitus teistele vanematele on julgeda pigem riskida väikeste asjadega, sobiva tee leidmiseks, kui mitte proovida üldse.
5. 3. sessioon – Von Willebrandi tõve tuleviku avamine
5.1 Kogu pere vaimne tervis – Cathy Verbraeken
Selle sessiooni alguses selgus, et Cathy Verbraeken, kes pidi rääkima pere vaimsest tervisest, ei saanud osaleda, kuna hemofiilia mõju perele on kohati sedavõrd suur, et ta vajas puhkust. Tema ettekande teemal „Kogu pere vaimne tervis“ võttis üle Manon Degenaar-Dujardin, kes jagas oma isiklikku ja puudutavat lugu.
Manon Degenaar-Dujardin keskendus Von Willebrandi tõve (VWD) perspektiivist patsiendi ja kogu pere vaimsele tervisele. Ta tõi välja, et vaimse tervishoiu teema on verejooksuhäiretega kogukonnas veel algusjärgus.
Isiklik teekond ja diagnoos
Manoni lugu algas sünnist 1977. aastal. Arstid pidasid tema korduvat oksendamist ja sagedasi ninaverejookse täiesti normaalseks. Kuna tal oli aga palju verevalumeid, ja tal oli terve õde, tunnetas Manoni ema, et midagi ei ole korras. Lõplik teadmine saabus, kui Manon 10-kuuselt kukkus ja punane laik tema rinnal muutus vaid tunniga suureks hematoomiks (verevalumiks), mistõttu ta saadeti haiglasse. Nii diagnoositi tal hemofiilia.
Varajane diagnoos tõi kaasa raskeid tagajärgi perele: vanemaid kahtlustati korduvalt laste õiguste (peksmises) rikkumises. Manoni vanemad tundsid end abituna, teadmata, kust abi otsida. Õnneks liitusid nad Hollandi ühinguga, mis asutatud paar aastat varem. Tutvus teiste patsientidega, 18- ja 19-aastaste noormeestega andis Manoni vanematele lootust, et ka nende tütar võib elada nii vanaks. Algselt oli neile öeldud, et ta ei pruugi elada täiskasvanu eani.
Kõrvalised mõjud ja varjamine
Esimesed kümme aastat möödusid raskelt: Manon puudus sageli koolist ja tema vanemad pidid koolis ühisüritustel alati kaasas olema, kuna teiste laste vanemad kartsid teda ilma saatjata oma hoole alla võtta. Kuigi ta ise ei pööranud sellele alguses tähelepanu, mõjutas häire oluliselt tema õdesid. Tema vanem õde tundis kadedust, kuna Manon sai verejooksuhäire tõttu rohkem tähelepanu. Samas Manon ise aga tajus tagantjärele, et see tähelepanu oli ju alati seotud tema haigusega, mitte aga temaga kui isikuga.
Pöördepunkt saabus 1989. aastal, kui tema ravi muutus, kuid valu ei olnud enam kontrolli all. 1990. aastal halvenes olukord veelgi, kui algas tema esimene menstruatsioon, mis kestis kolm ja pool kuud, ja ta sattus haiglasse. Manon, olles loomult introvert, otsustas kanda koormat üksi, varjates oma muresid ja kartusi isegi vanemate eest. Ta püüdis olla “laps, keda vanemad soovisid näha”, surudes alla oma tegeliku mina ja elades pidevalt ellujäämisrežiimil. Tema verejooksuhäire ja sellega seotud tüsistused olid tema “Hoia see saladuses!”.
Vaimse tervise puudumine ja kokkuvarisemine
Manon tõi kurvalt esile, et kogu tema 47 eluaasta jooksul oli vaimse tervishoiu tugi olematu. Ükski arst ega tervishoiuteenuse osutaja tema ravikeskuses ei ole kordagi küsinud tema vaimse tervise kohta või pakkunud talle või tema perekonnale abi. Ainus vaimse tervise abi, toimus siis kui, ta ise või tema vanemad seda otsisid.
31-aastaselt koges Manon täielikku sotsiaalset kokkuvarisemist. Ta oli sunnitud lõpetama loodud “tegelase” mängimise – teesklemise, et tal pole kunagi probleeme. Pärast arstide külastamist diagnoositi tal depressioon ning ta sai esimest korda vajalikku vaimset abi. See hõlmas nii ravimeid kui ka käitumisteraapiat ärevuse ja obsessiiv-kompulsiivse häire (OCD) raviks. Täna on ta veendunud, et tema lugu oleks olnud teistsugune, kui talle oleks kogu teekonna vältel pakutud psühhosotsiaalset abi.
Laste vaimse tervise mõju
Manon tõi esile ka oma poja olukorra, kellel diagnoositi 2014. aastal Henoch-Schönleini purpur (vaskuliit) – väikeste veresoonte põletik kehas. See oli halb kombinatsioon koos VWD-ga. Manon nägi, kuidas poeg kaotas usu oma kehasse ja hakkas kartma, korrates tema enda varasemat käitumismustrit. Poiss hakkas täielikult emast sõltuma, kartes isegi toast väljumist, kui ema läks vannituppa. Ravikeskus ei pakkunud abi, ja nad otsisid vanematena ise psühholoogi ja coach’i abi. Manon pidi isegi 2023. aastal Euroopa Hemofiilia Konsortsiumi (EHC) juhtkomiteest tagasi astuma ja töölt puhkuse võtma, et pühendada oma energia poja ja pere toetamisele
Manon lõpetas nentimisega, et teda ei tee murelikuks kõige rohkem haiguse sümptomid, vaid tagajärjed, mis kaasnevad täiendavate väljakutsetega, haigusega kasvamisega. Ta tegi ettepaneku investeerida rohkem vaimsesse tervishoidu, kuna see on sama oluline kui füüsiline tervishoid. „Sellest ei piisa, kui sul on terve keha, aga haige hing“ rõhutas ta.
5.2 VWD: esitlusest ja sõeluuringust geneetikani – Giancarlo Castaman
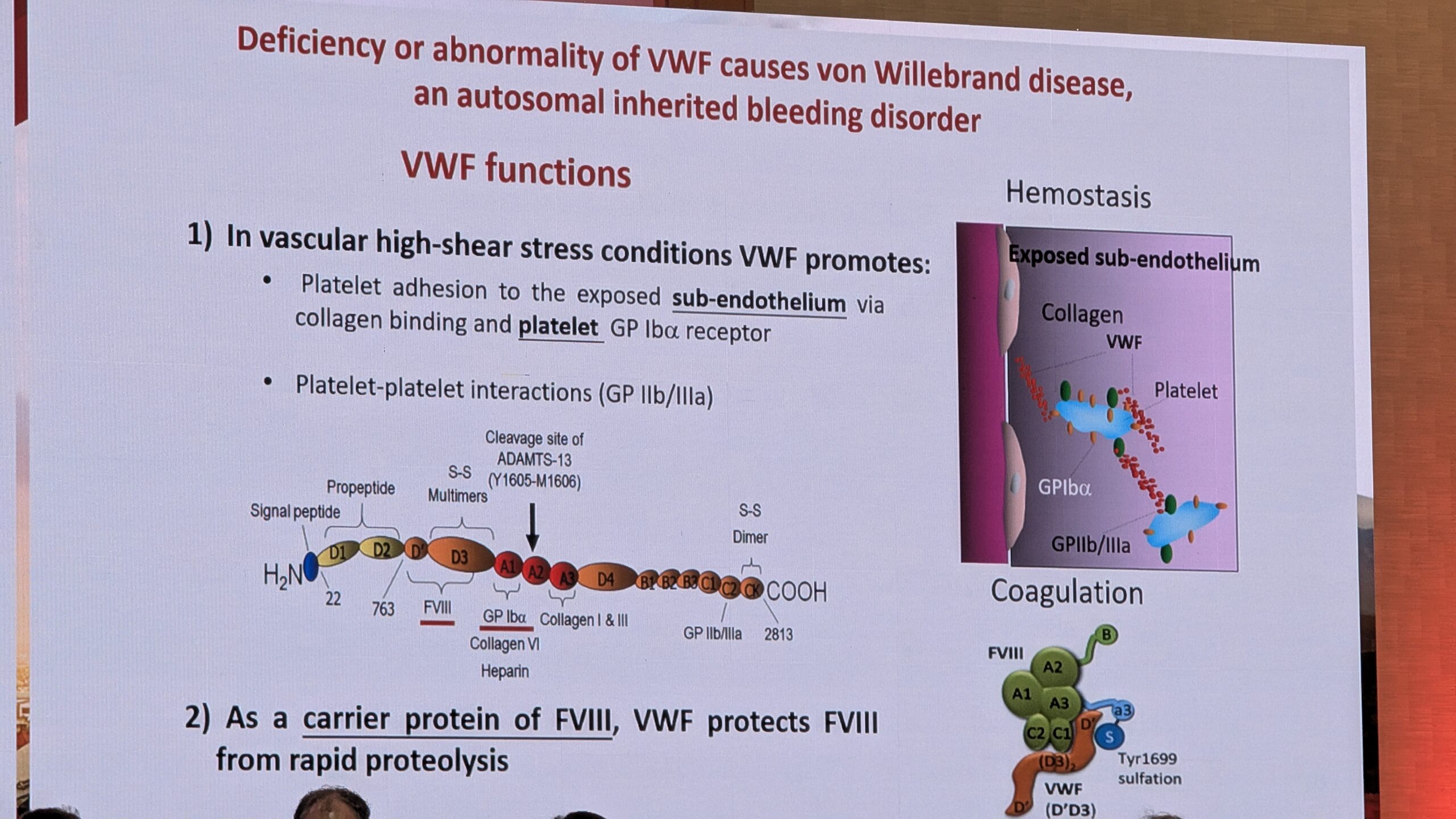
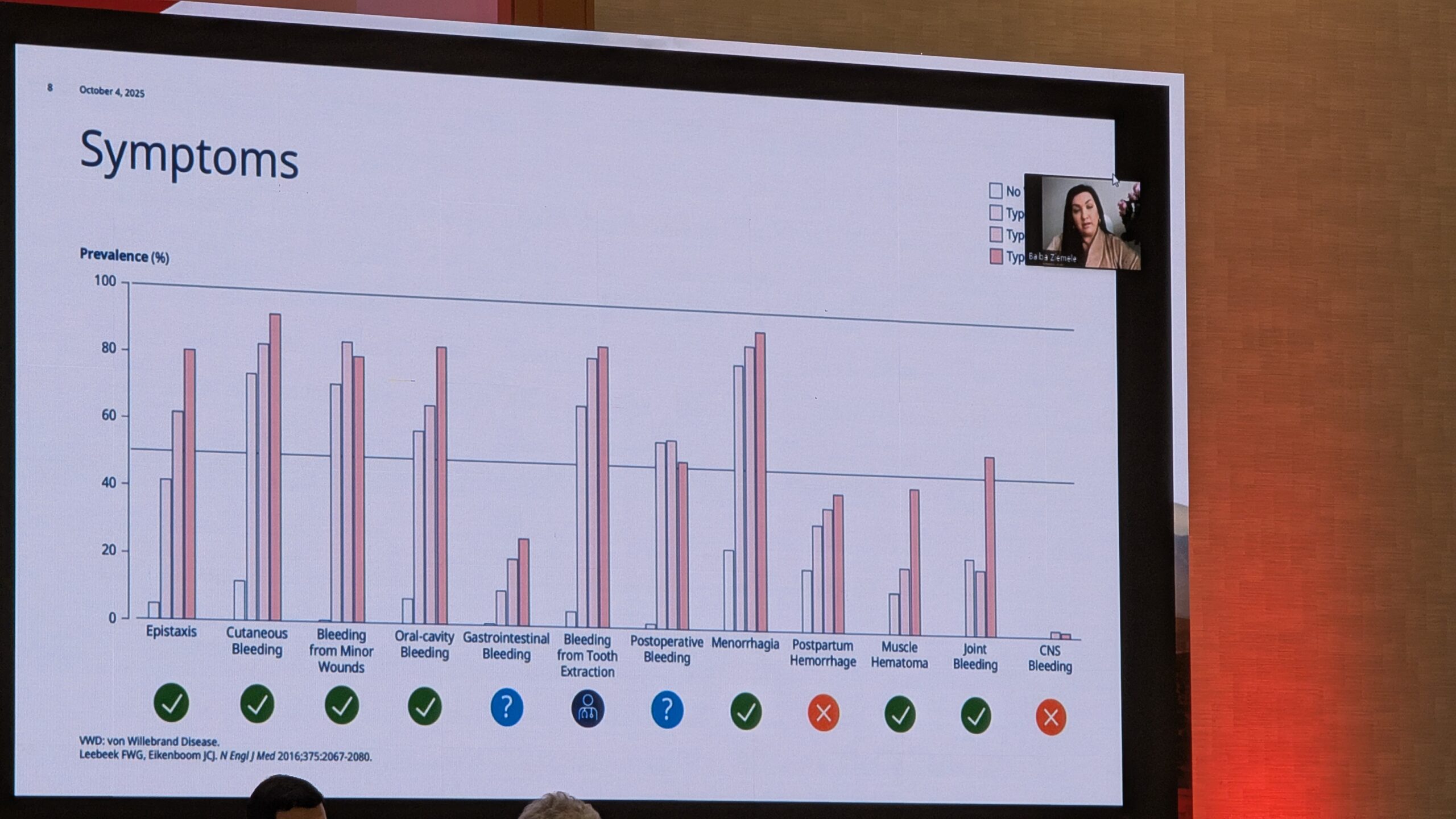
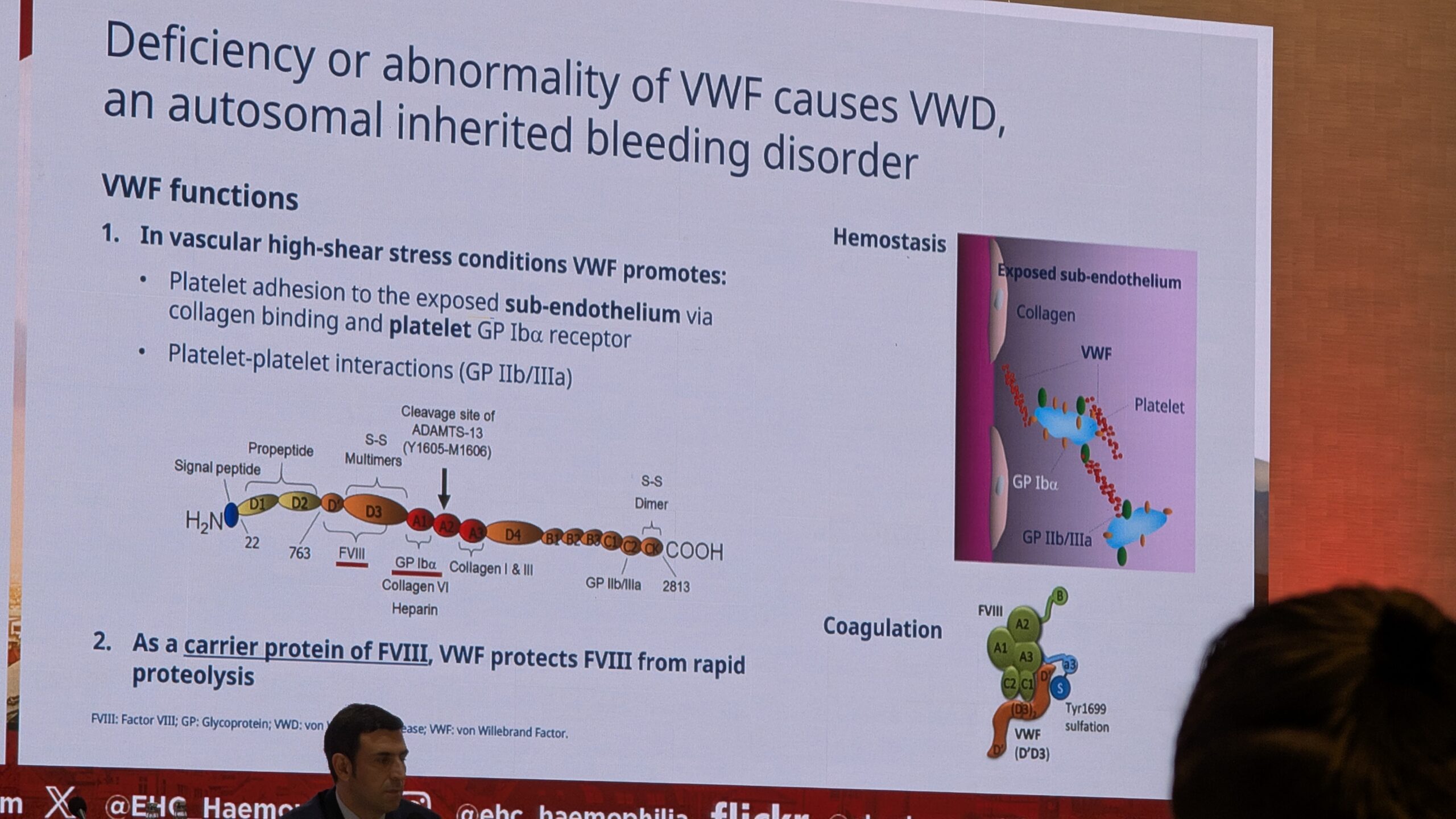
Giancarlo Castaman käsitles oma ettekandes Von Willebrandi tõve (VWD) teaduslikku ja diagnostilist aspekti. VWF-l (Von Willebrandi faktor) on kaks peamist funktsiooni: hemostaasis (veritsuse peatamine), kus ta ühendab vereliistakute ja kahjustatud subendoteel , ning koagulatsioonis (hüübimises), kus ta on Faktori VIII kandev valk.
Diagnostika ja Sõeluuring
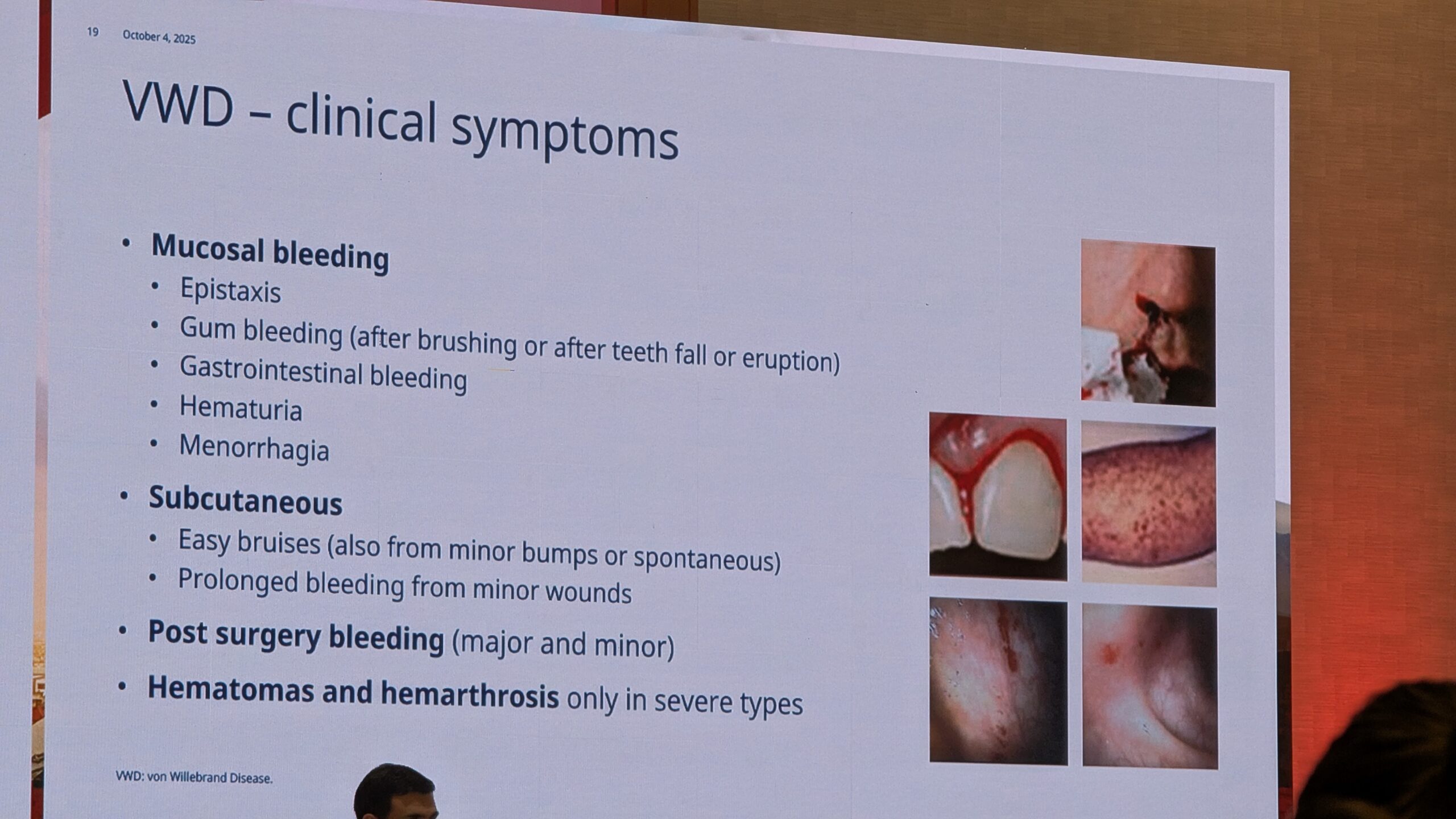
VWD täpseks diagnoosimiseks peavad olema täidetud kolm kriteeriumi: peab olema tõestatud verejooksuhäire olemasolu, VWF-i puudulikkus või kvaliteedi muutus ja pärilikkus (geneetiline alus), kuna tegemist on valdavalt autosoomselt dominantse või retsessiivse haigusega. Kliinilist tüüpi iseloomustab limaskestade verejooks (mukokutaanne verejooks).
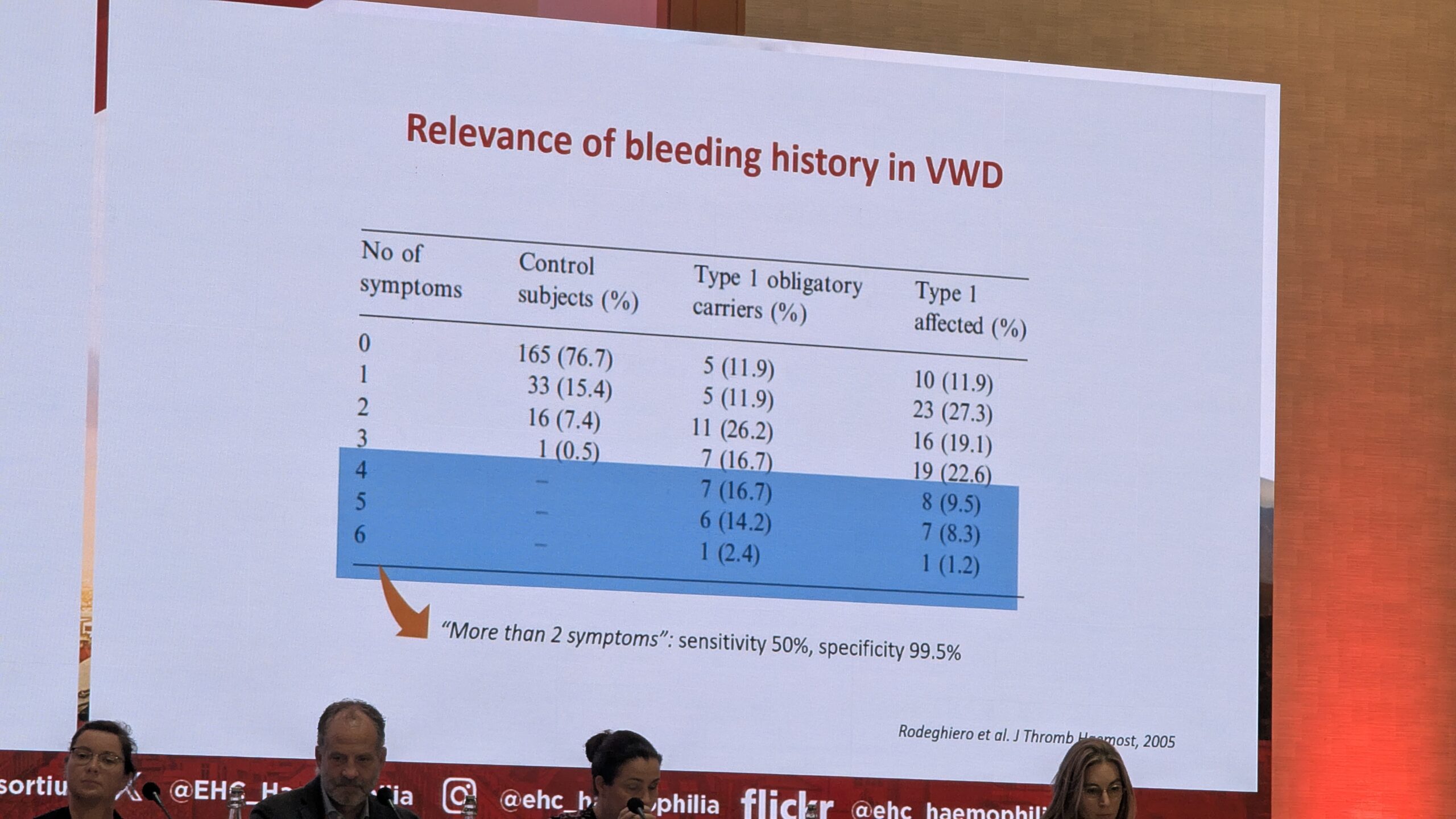
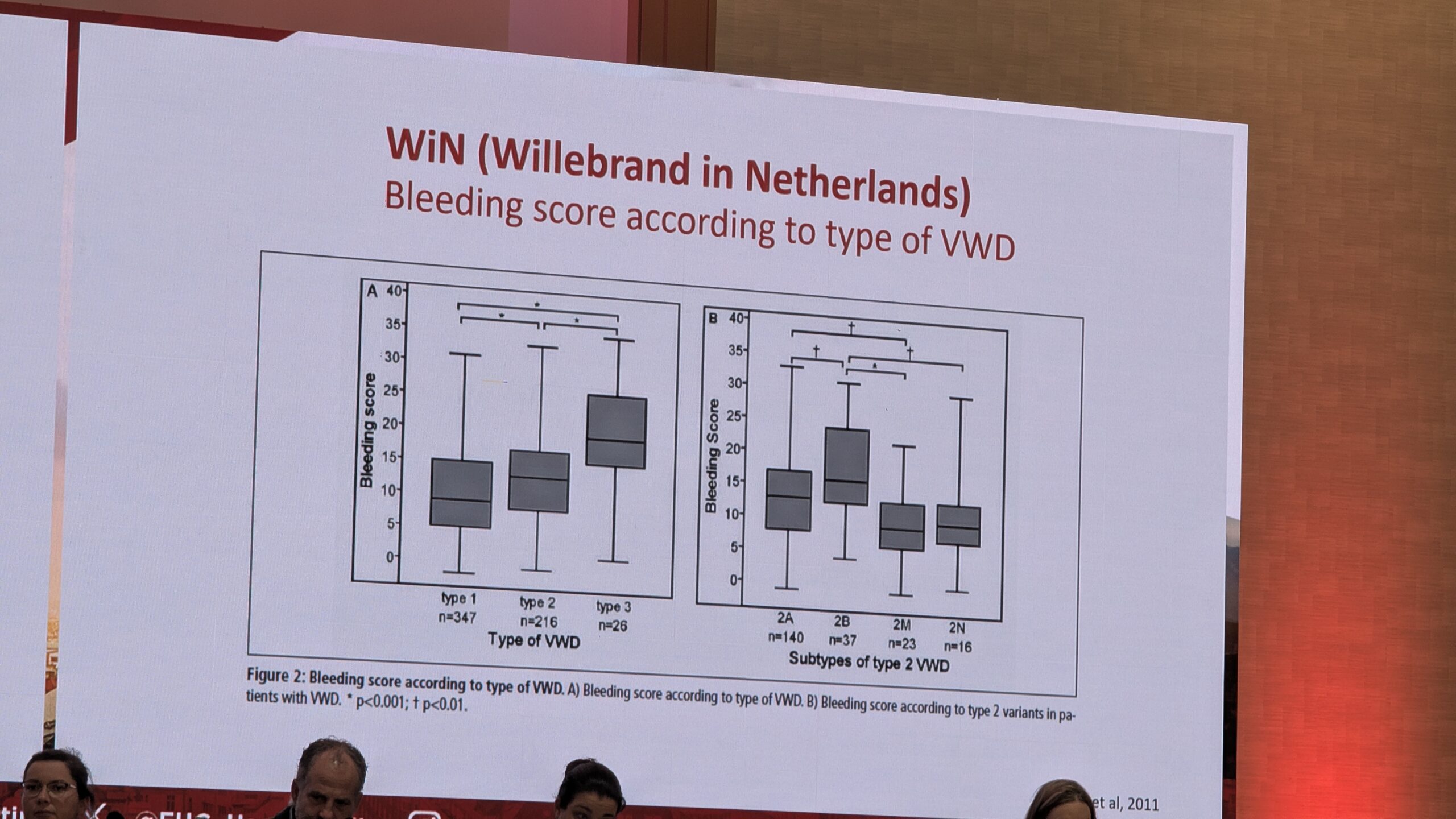
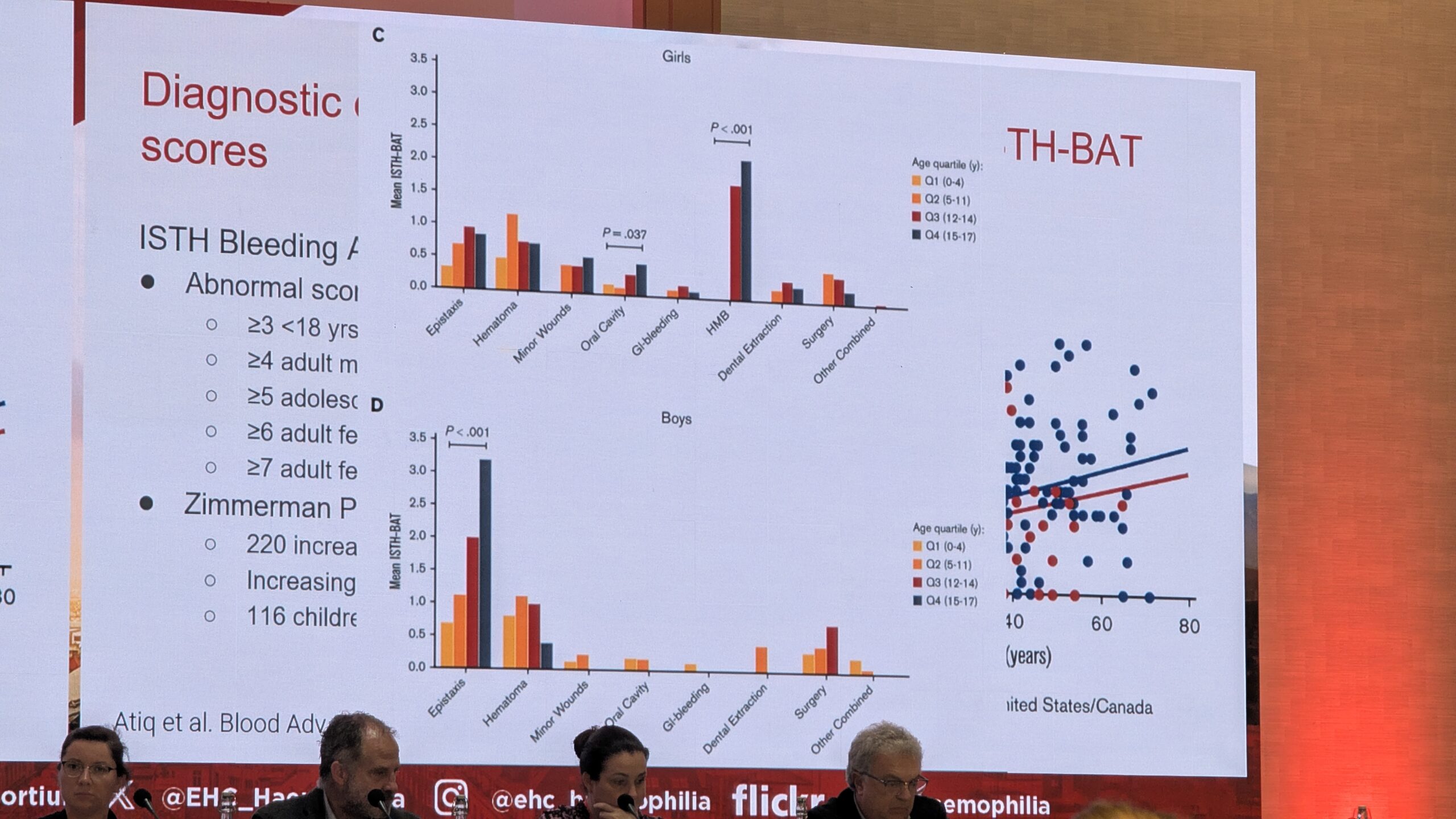
Castaman rõhutas, et verejooksu anamneesi (ajaloo) võtmine on keeruline. Kasutatakse objektiivsemaid hindamisvahendeid, veritsus küsimustikku. Mitmed sümptomid viitavad verejooksuhäire võimalikule diagnoosile. On soovitav kasutada standardiseeritud küsimustikke, näiteks ISTH-BAT (International Society on Thrombosis and Haemostasis – Bleeding Assessment Tool), mis hindab kõiki võimalikke varasemaid sümptomeid. Tulemus, mis naistel kõrgem nr 4-st ja alla kuue meestel, on viide veritsusele ja vajadusele arsti konsultatsiooniks.
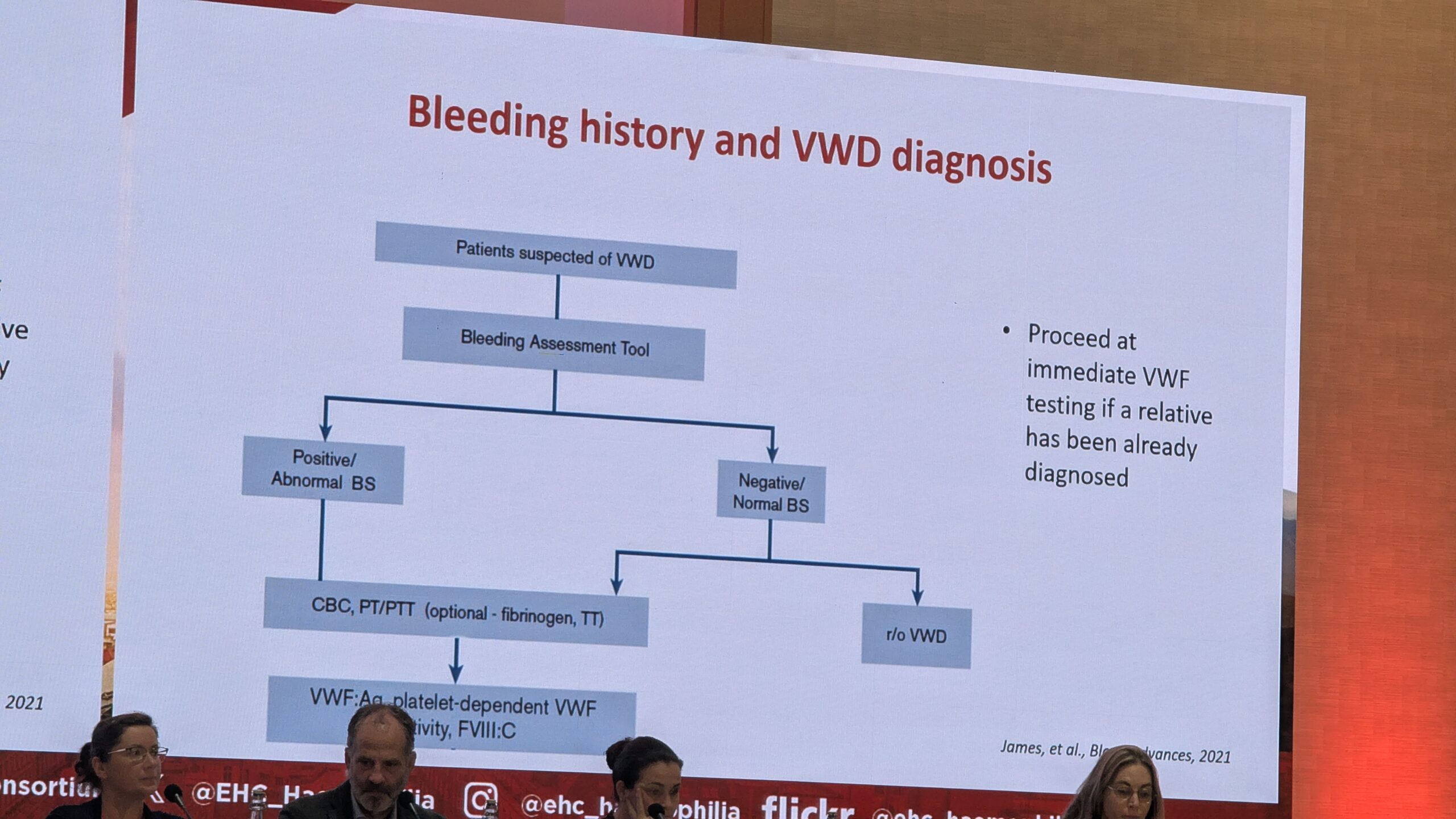
Laboratoorne Hindamine ja Geneetika
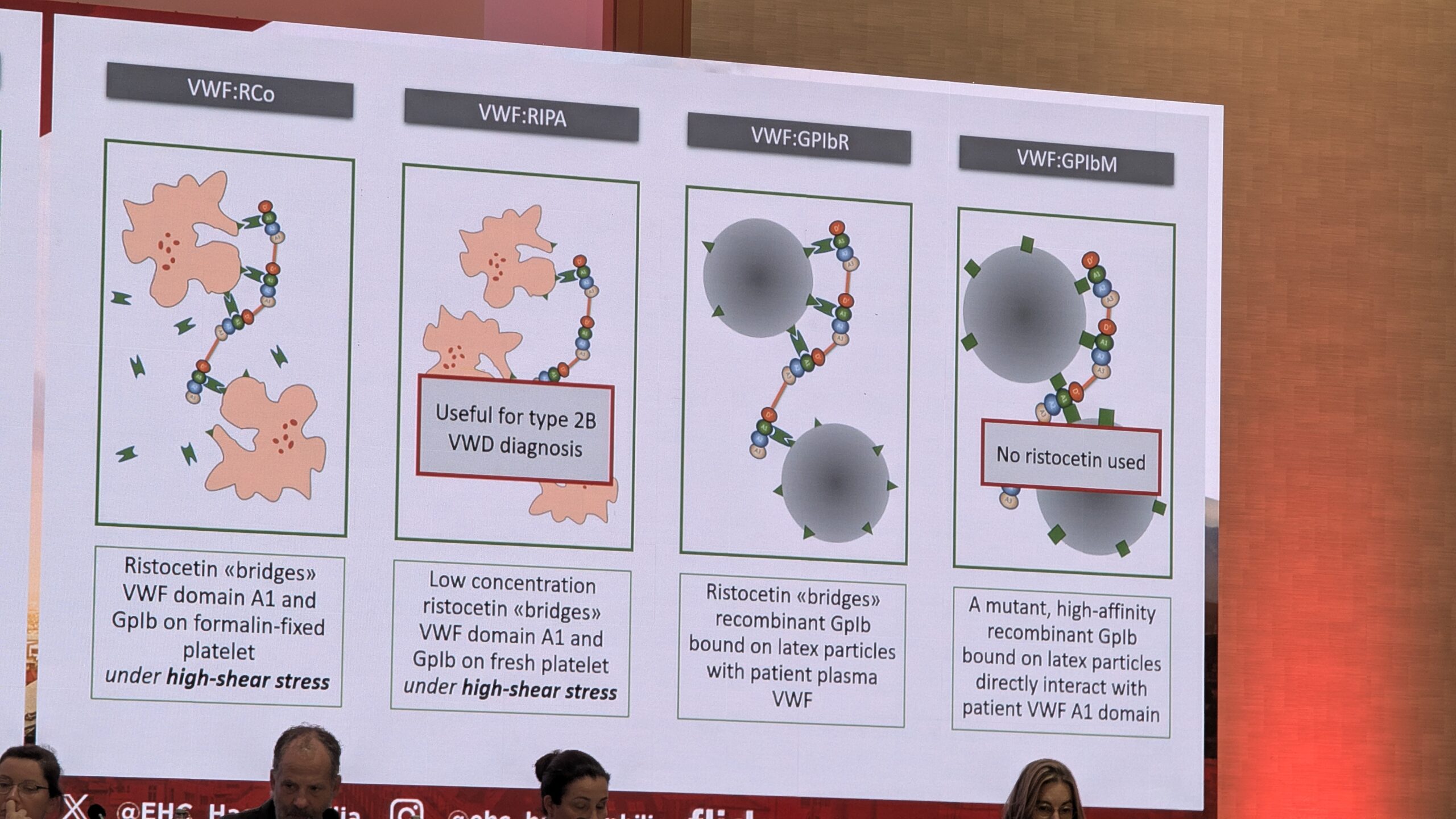
Verejooksu küsimustiku (BAT) järgi saab otsustada esimese taseme sõeluuringu vajaduse üle. Põhitestid hõlmavad protrombiini aega (PT), osalise tromboplastiini aega (APTT), vereliistakute arvu ja VWF aktiivsust. Castaman selgitas, et ükski test ei hõlma VWF-i tegevuse kogu spektrit, kuna faktoril on mitu omadust (seondumine vereliistakutega, FVIII seondumine). Seetõttu soovitas ta kasutada uuemaid VWF aktiivsuse määramise meetodeid, mis on tundlikumad ja kergesti automatiseeritavad, kuigi paljud keskused kasutavad veel ajaloolist ristosetiiniga seotud aktiivsuse testi.
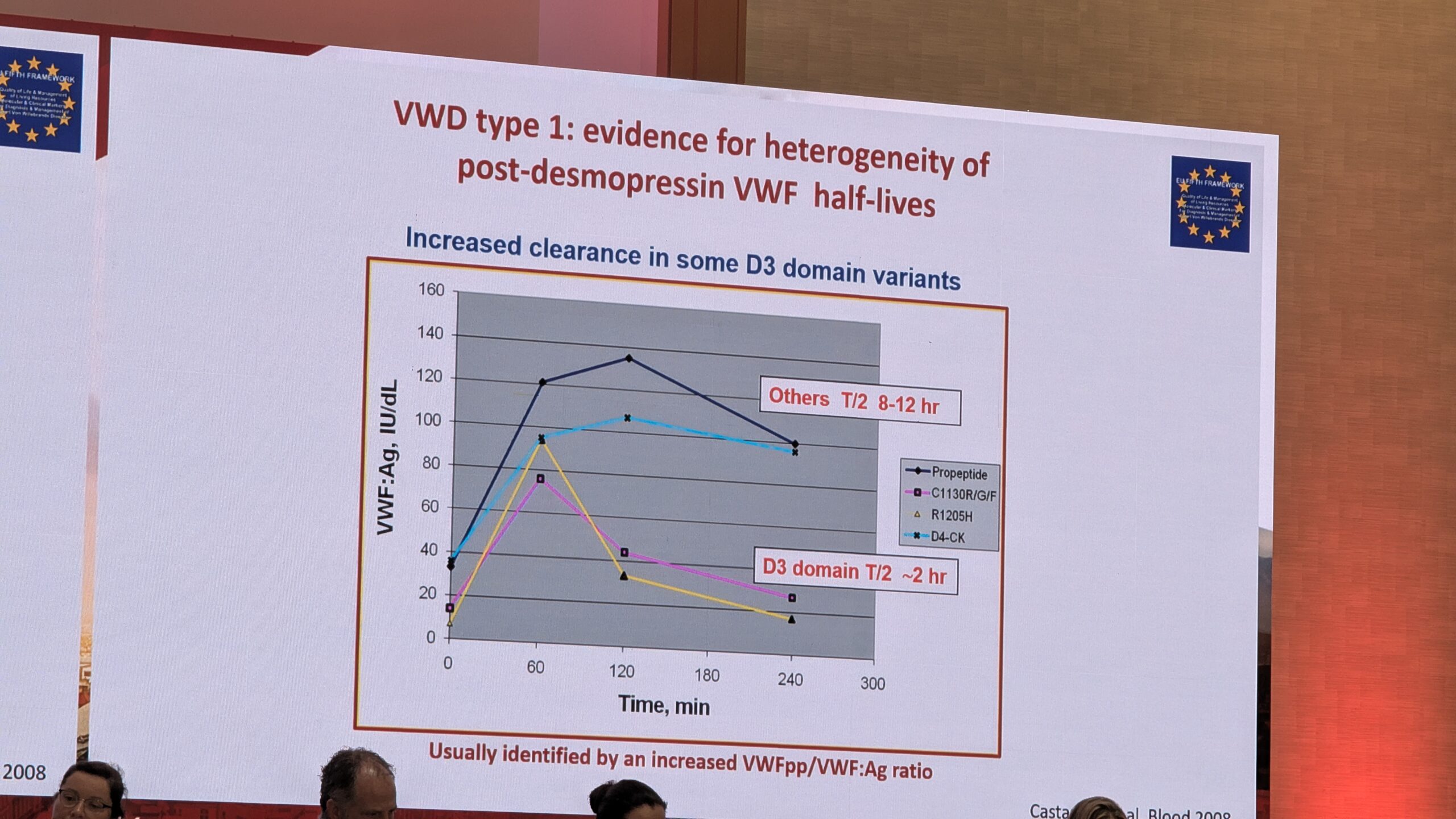
Geneetiline testimine on muutunud järjest olulisemaks, eriti alamliikide (tüüp 2) diagnoosimisel, kus VWF kontsentratsiooni ja aktiivsuse suhe on vähenenud. Geneetiliselt saab eristada näiteks Tüüpi 1 (kvantitatiivne puudulikkus) ja Tüüpi 2 (kvalitatiivne puudulikkus). Samuti aitab geneetika tuvastada haruldasi alamliike nagu Tüüp 2N, mis sarnaneb kliiniliselt hemofiilia A-ga (madal faktor VIII tase). Geneetiline analüüs on eriti väärtuslik peredes, kus on esinenud VWF-vastaseid inhibiitoreid, või VWD tüüp 3. Castaman rõhutas lõpetuseks, et mõlemad, mehed ja naised, on võrdselt mõjutatud, kuigi naistel võib kliiniline pilt olla fertiilses eas raskem.
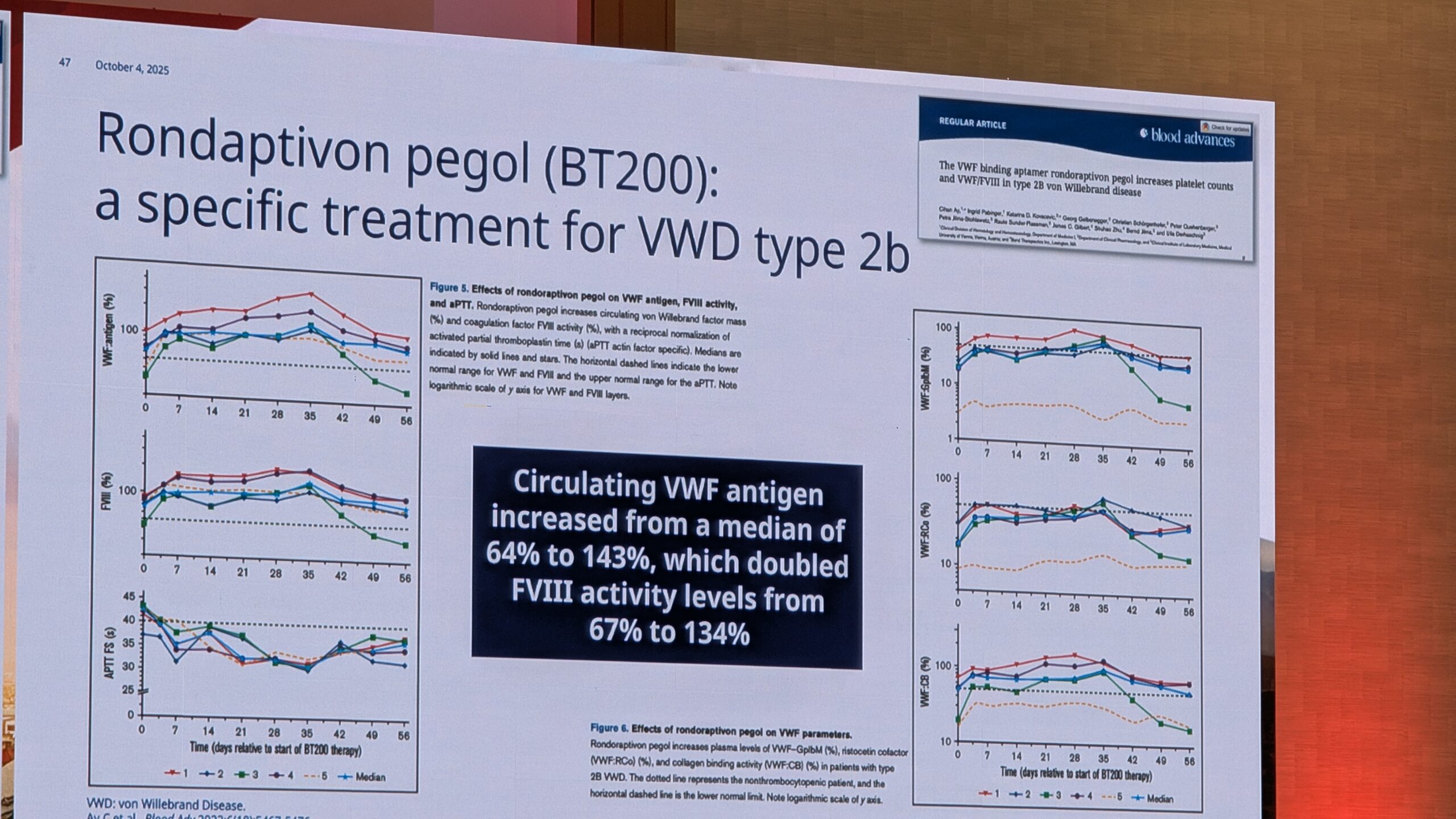
5.3 Eelvaade tulevastesse VWD ravimeetoditesse – Karin van Galen
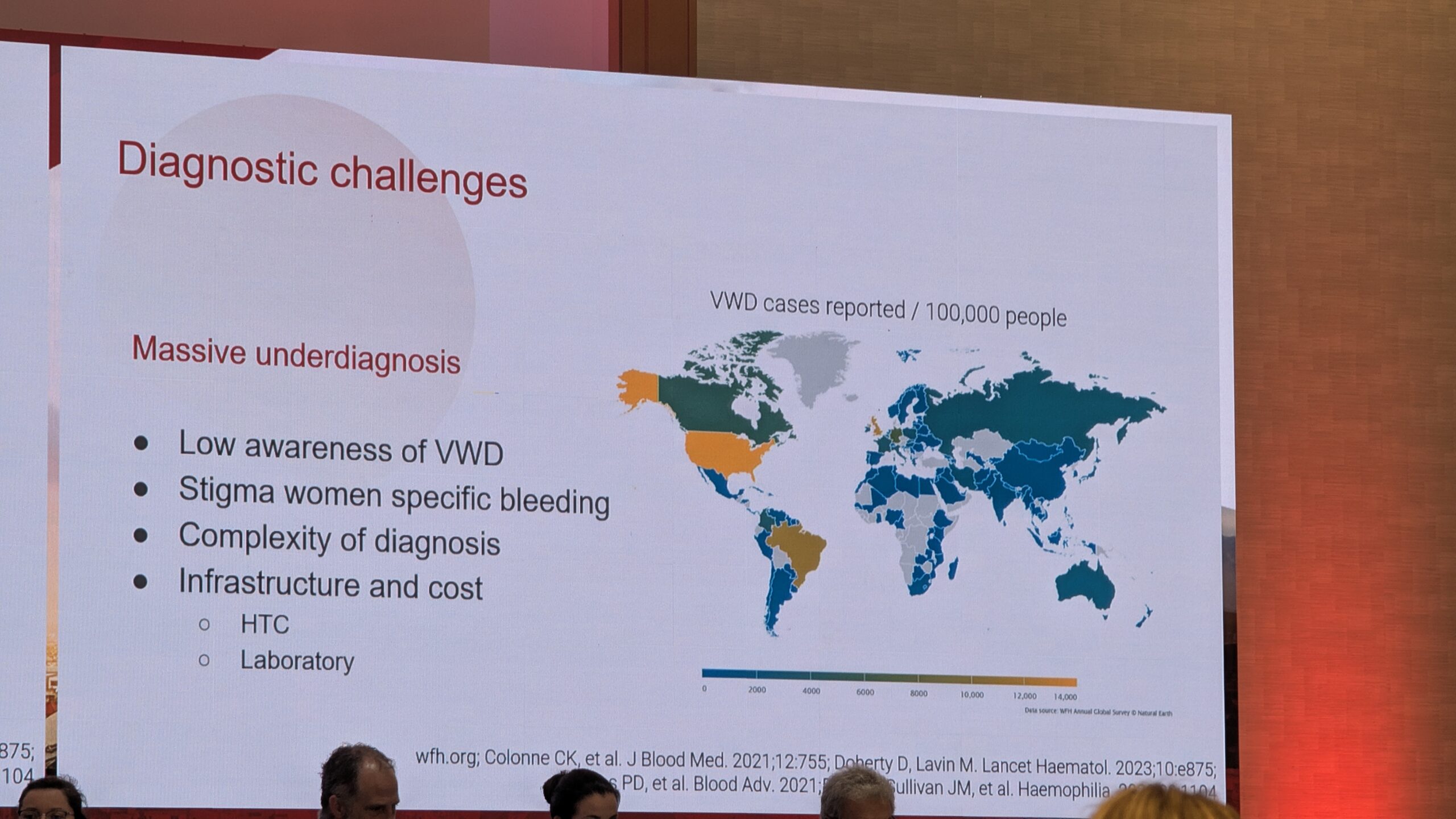
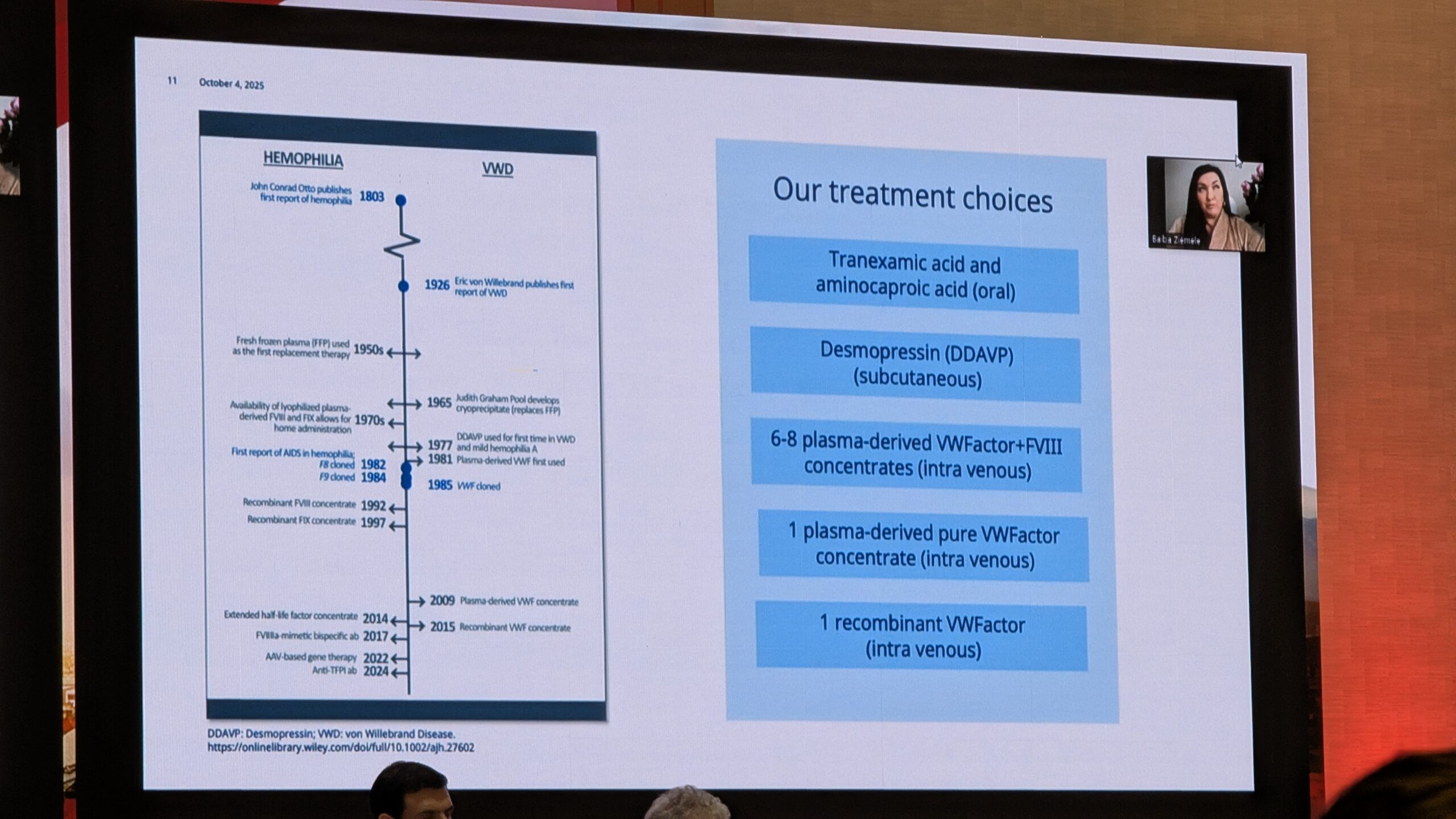
Karin van Galen andis ülevaate VWD ajaloost ja tuleviku ravistrateegiatest. VWD-d kirjeldati esmakordselt 1926. aastal Ålandil ja 1960. aastatel sai kättesaadavaks VWF-i kontsentraat. Tänapäeval on VWD aladiagnoositud, eriti madala teadlikkuse, keerulise diagnostika ja suurte ressursside vajaduse tõttu.
VWD diagnoosi väljakutsed
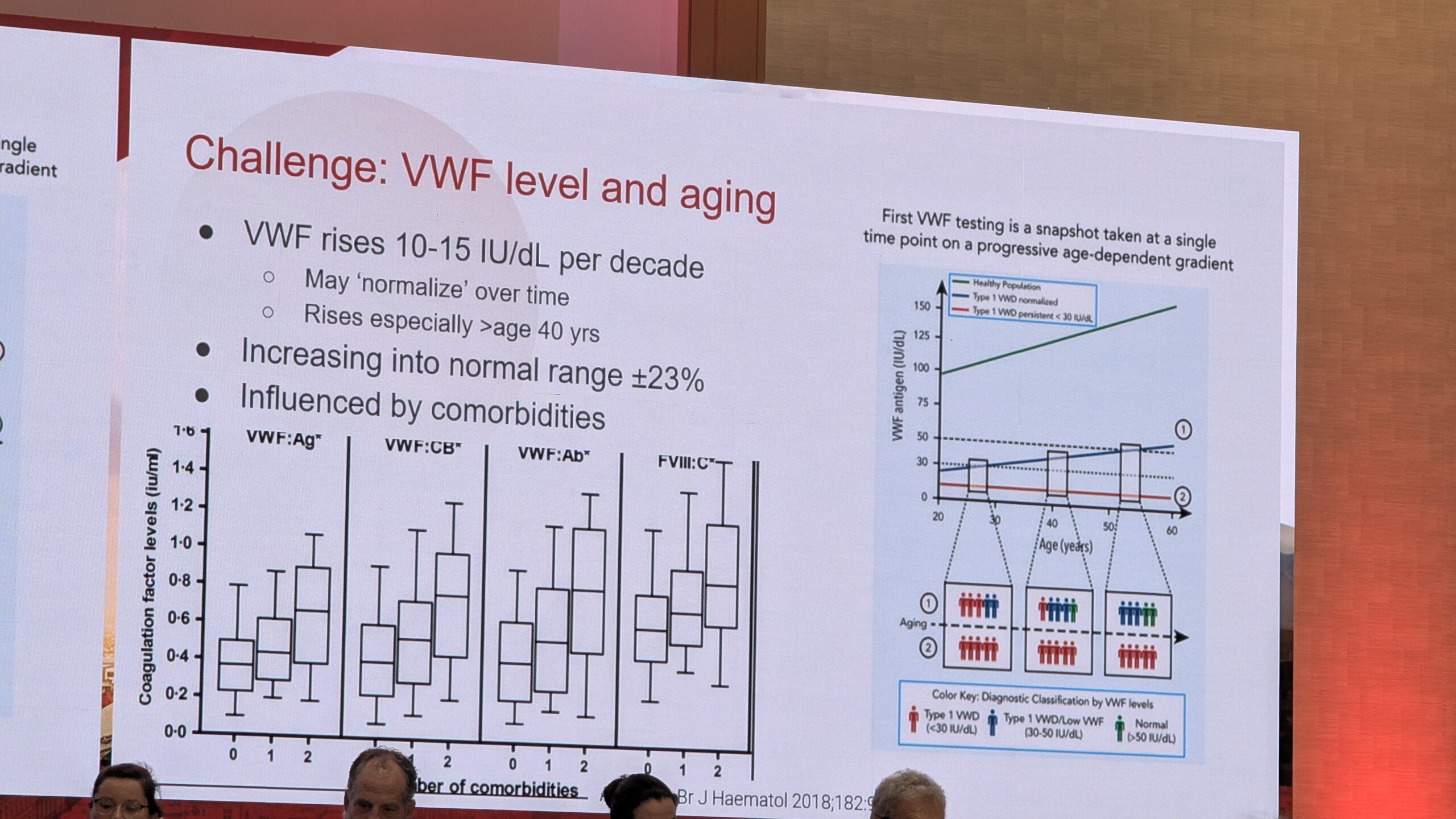
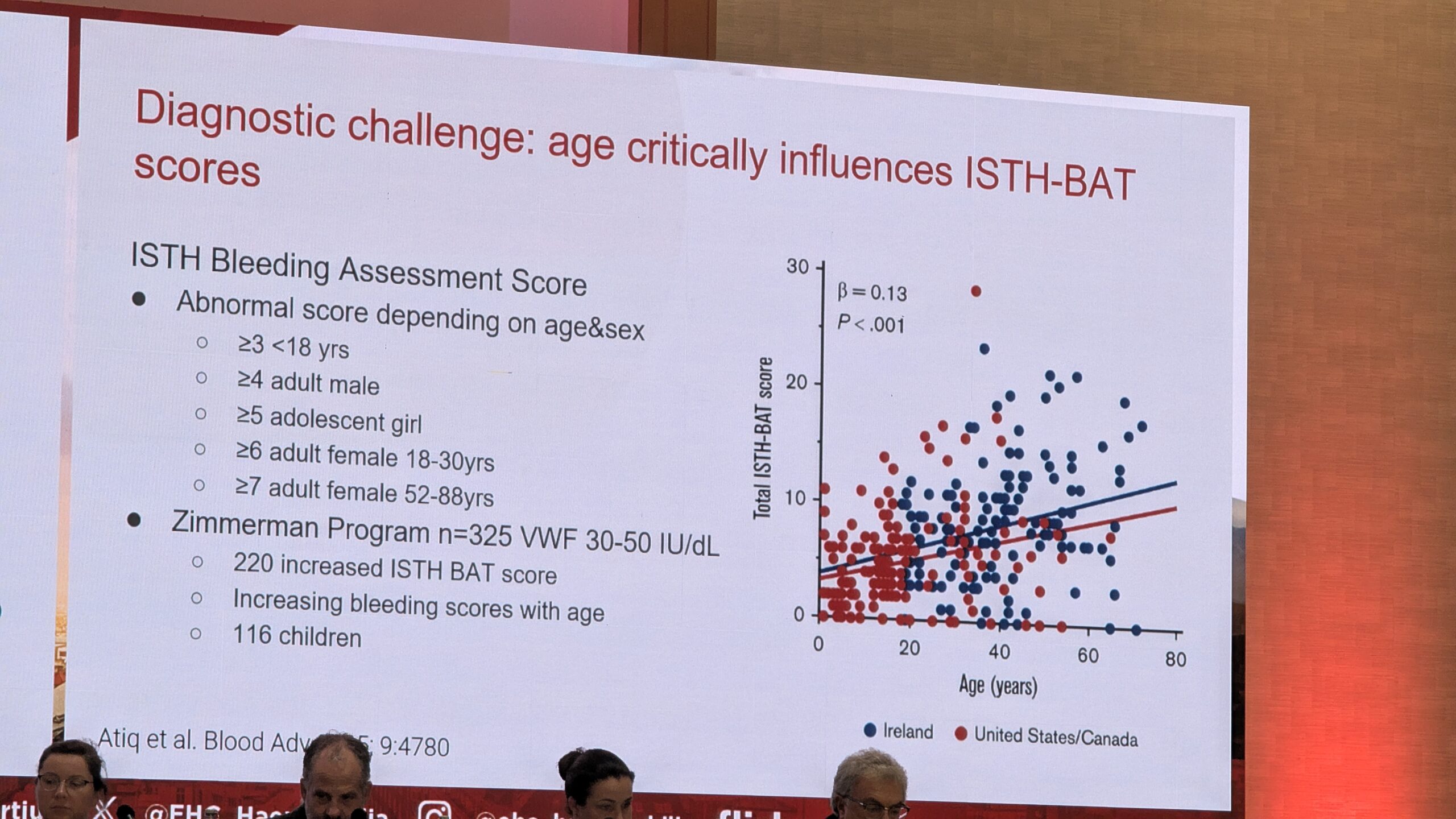
Van Galen selgitas, et VWF tase alla 30 RÜ/dl annab selge diagnoosi. Kuid tase vahemikus 30 ja 50 RÜ/dl on diagnoosimine keerulisem, mis on seotud suurema rauapuuduse ja aneemia riskiga naistel. Samal ajal pakuvad need aga veidi kaitset süvaveenitromboosi eest. VWF tase vanusega tõuseb, mis võib põhjustada hilise diagnoosi või diagnoosi panemise hilinemise. Lisaks mõjutab hindamist patsiendi vanus, sugu, stressitase ja elustiil. Oluline on kasutada soo- ja vanusepõhiseid referentsväärtusi verejooksu hindamisskooride jaoks, näiteks ISTH-BAT skoori, mis näitas, et menstruatsioonid suurendavad verejooksu skoori oluliselt.
Tuleviku ravivõimalused
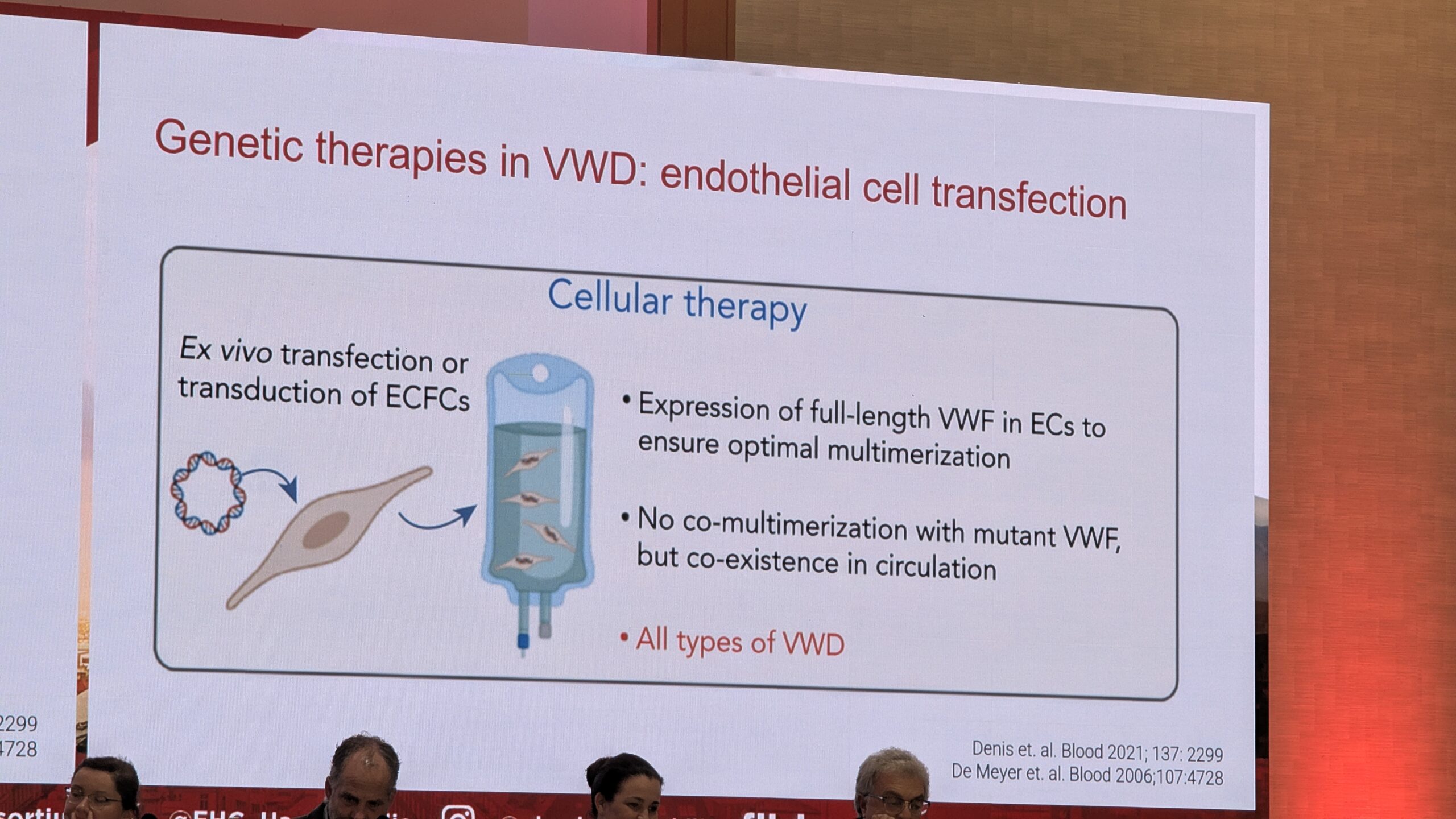
Karin van Galen andis ülevaate VWD ravivõimalustest, mis on alles arenemisjärgus. Tuleviku potentsiaalsed ravimeetodid hõlmavad geeni- ja rakuteraapiat, ravimeid VWF-i puudulikkuse kompenseerimiseks ja VWF taseme tõstmiseks.
- F8 mimeetikumid (FVIII) : Näiteks Emitsizumab (mis jäljendab FVIII aktiivsust) on näidanud head efektiivsust hemofiilia A ja VWF-ga patsientidel, ning sellega on käimas uuringud.
- Antitrombootilised ravimid: Uued uuringud on suunatud antikoagulatsiooni valkude reguleerimisele, näiteks Fitusiran (antitrombiini agonist) ja ained, mis reguleerivad VWF lagunemist. Fitusiran on andnud paljutõotavaid tulemusi, vähendades aastast verejooksude määra (ABR), eriti naistel, kellel on ebanormaalne emaka verejooks.
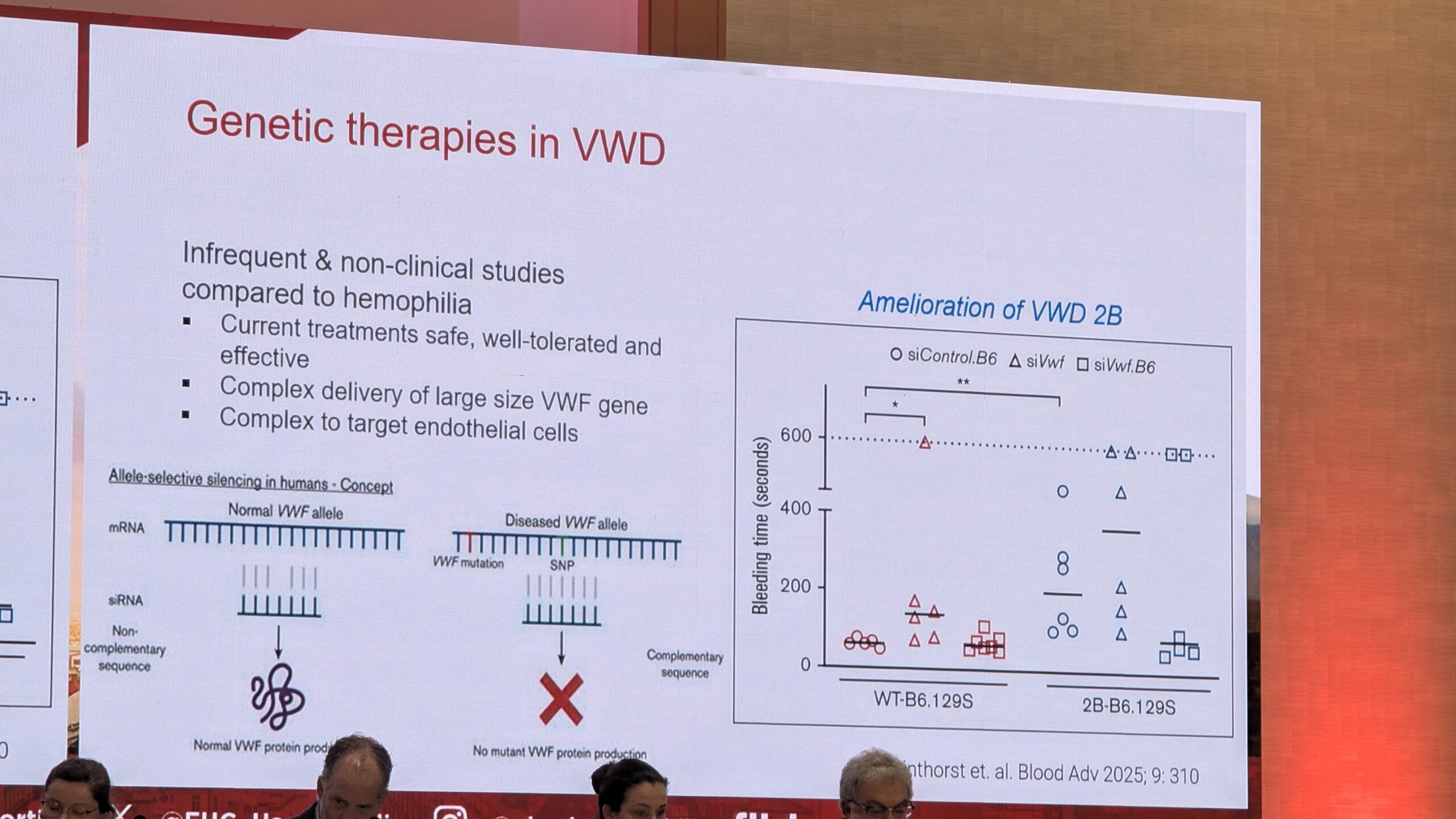
- Geeniteraapia: geeniteraapia VWD raviks oleks ideaalne, kuid uuringuid seni minimaalsed, eriti võrreldes hemofiiliaga. Põhjuseks VWF-i geeni suur suurus ja toime keerukus. Van Galen mainis ka uuenduslikke kontseptsioone, nagu “vaigistav RNA”, et pärssida dominantseid negatiivseid mutatsioone (eriti Tüüp 2B puhul).
Van Galen hoiatas, et hoolimata teaduslikust huvist VWD ravimise parandamise vastu, on endiselt suured puudujäägid ravimite kättesaadavuse ja ebavõrdsuse osas, eriti võrreldes hemofiiliaga. Oluline on tagada, et senised potentsiaalsed ravimeetodid jõuaksid ka patsientideni.
6. 4. sessioon – Haruldaste veritsushäirete keerukuse uurimine: Inhibiitorid, BDUC ja fibrinogeeni defektid
6.1 Fibrinogeeni häirega veritsushaigused ja nende ravimeetodid – Dr. Alessandro Casini
Alessandro Casini alustas ettekannet fibrinogeeni häirete ehk hüübimisfaktori I (faktor I) häirete keerukuse ja väljakutsetega ravi osas. Ta andis lühikese sissejuhatuse nende häirete epidemioloogia, klassifikatsiooni ja diagnoosimise kohta, keskendudes seejärel vähestele tõenduspõhistele andmetele nende patsientide juhtimise kohta.
Klassifikatsioon ja epidemioloogia
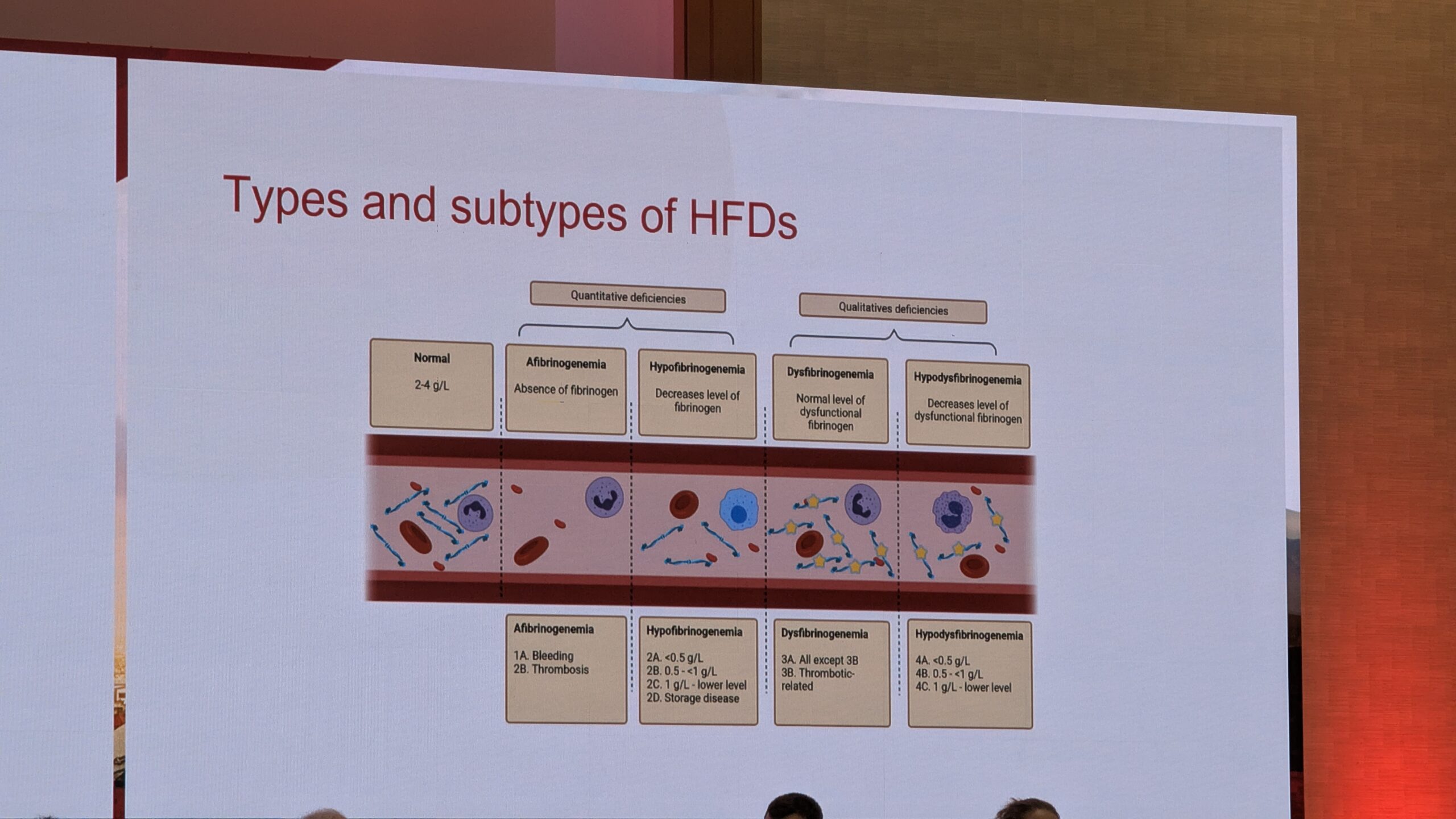
Fibrinogeeni häired jagunevad kvantitatiivseks ja kvalitatiivseks puudulikkuseks.
- Kvantitatiivne puudulikkus:
- Afibrinogeneemia (fibrinogeeni tase veritsuses puudub – või on tuvastamatu).
- Hüpofibrinogeneemia (kontsentratsioon veres on vähenenud, kuid mõõdetav). Hüpofibrinogeneemiat klassifitseeritakse kontsentratsiooni järgi kergeks (1–2 g/L), mõõdukaks (0,5–1 g/L) või raskeks (<0,5 g/L). Kvantitatiivse puudulikkuse puhul on verejooksu fenotüüp tugevalt korrelatsioonis fibrinogeeni kontsentratsiooniga.
- Kvalitatiivne puudulikkus (toime puudus või nõrkus):
- Düsfübrinogeneemia (normaalne fibrinogeeni kontsentratsioon, kuid puudub oodatav toime).
- Hüpodüsfübrinogeneemia (vähenenud kontsentratsioon ja vähenenud toime).
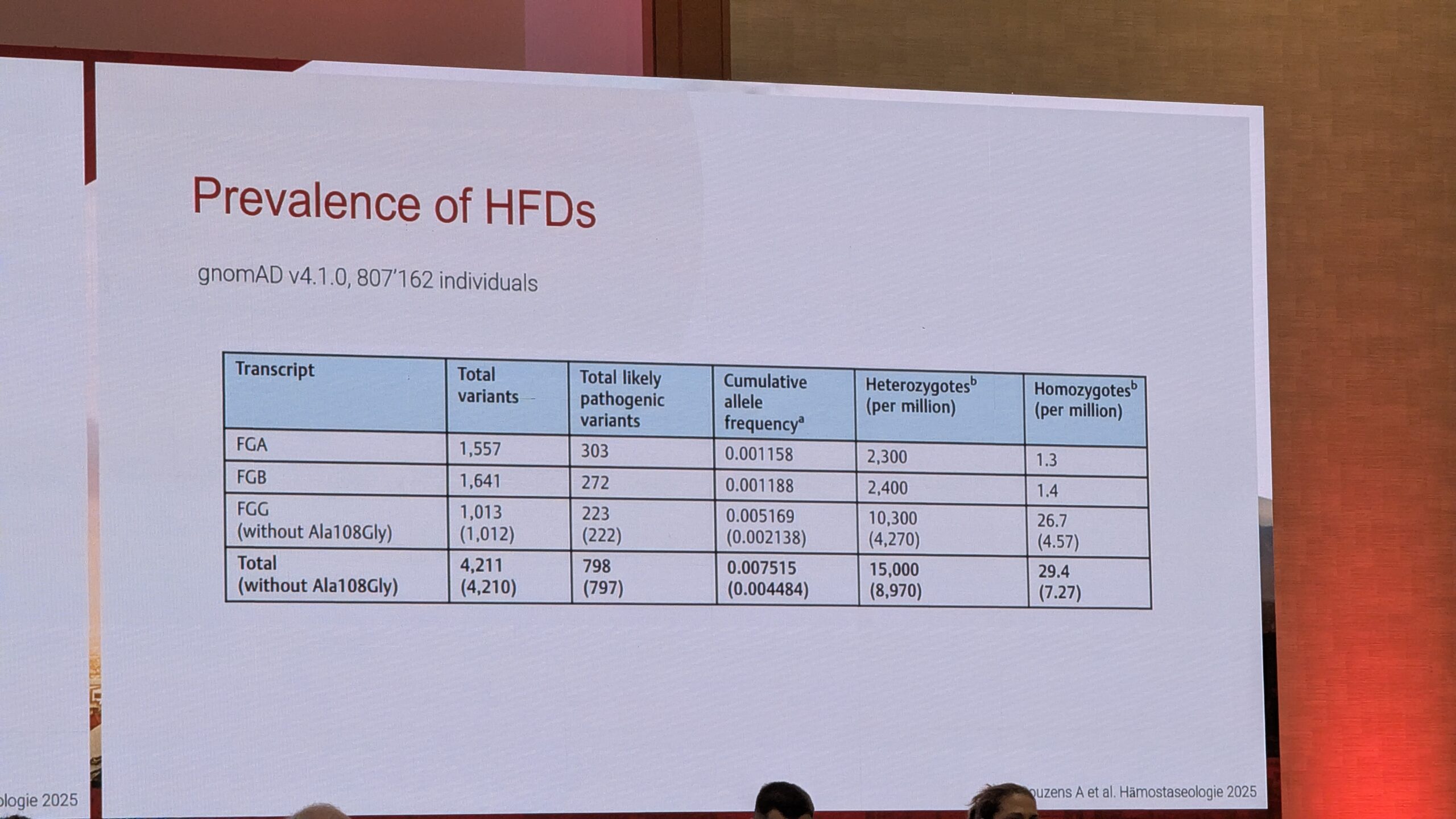
Kõige raskema fibrinogeeni defekti, afibrinogeneemia, hinnanguline levimus on umbes 1 juht 1 miljoni inimese kohta. Hiljutised geneetilised andmed näitavad aga, et VWF-i mutatsioonid võivad olla oodatust levinumad, ulatudes 1:15 000-ni (hüpofibrinogeneemia ja düsfübrinogeneemia koondlevimus).
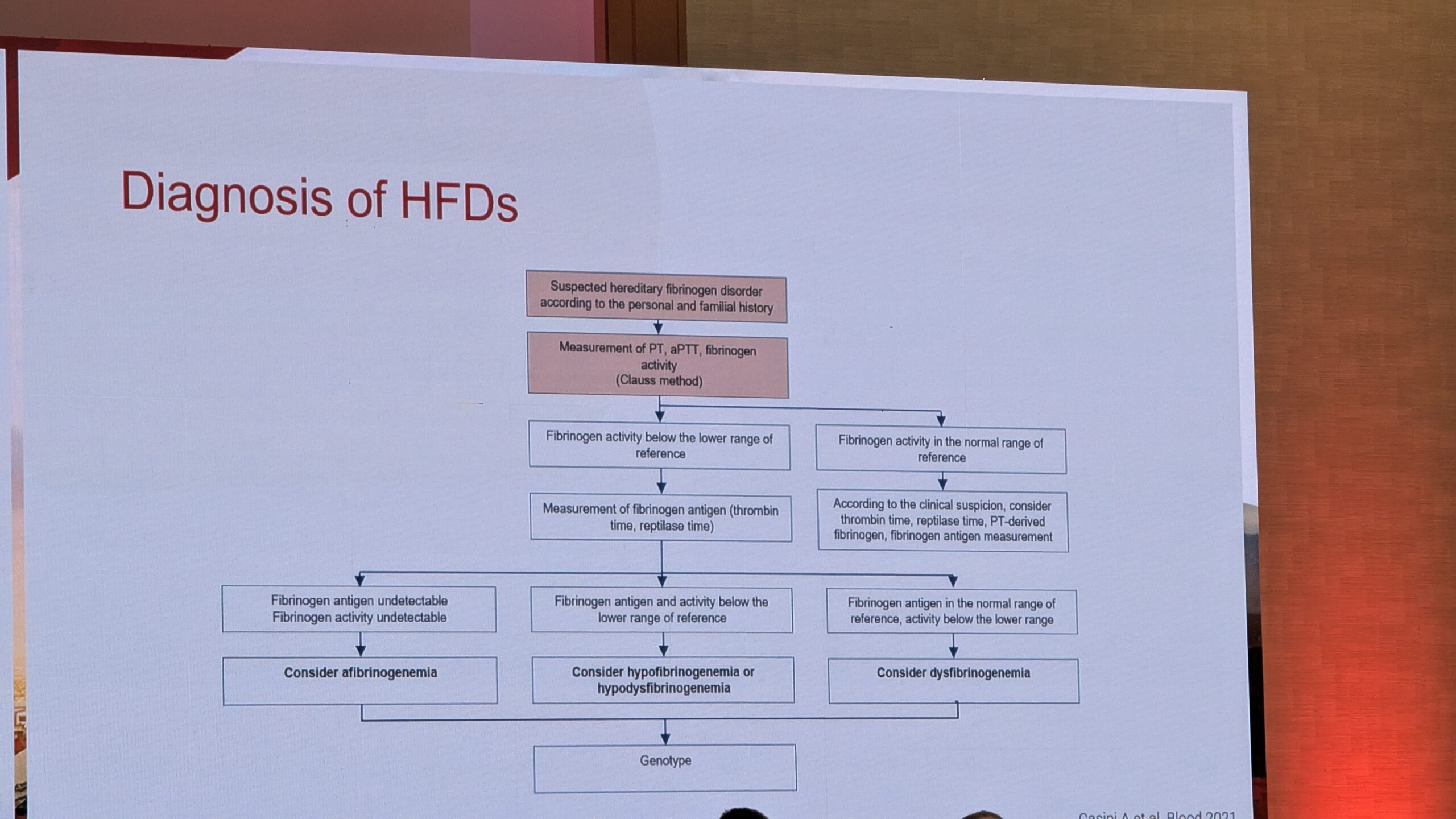
Diagnoosimine ja ravi väljakutsed
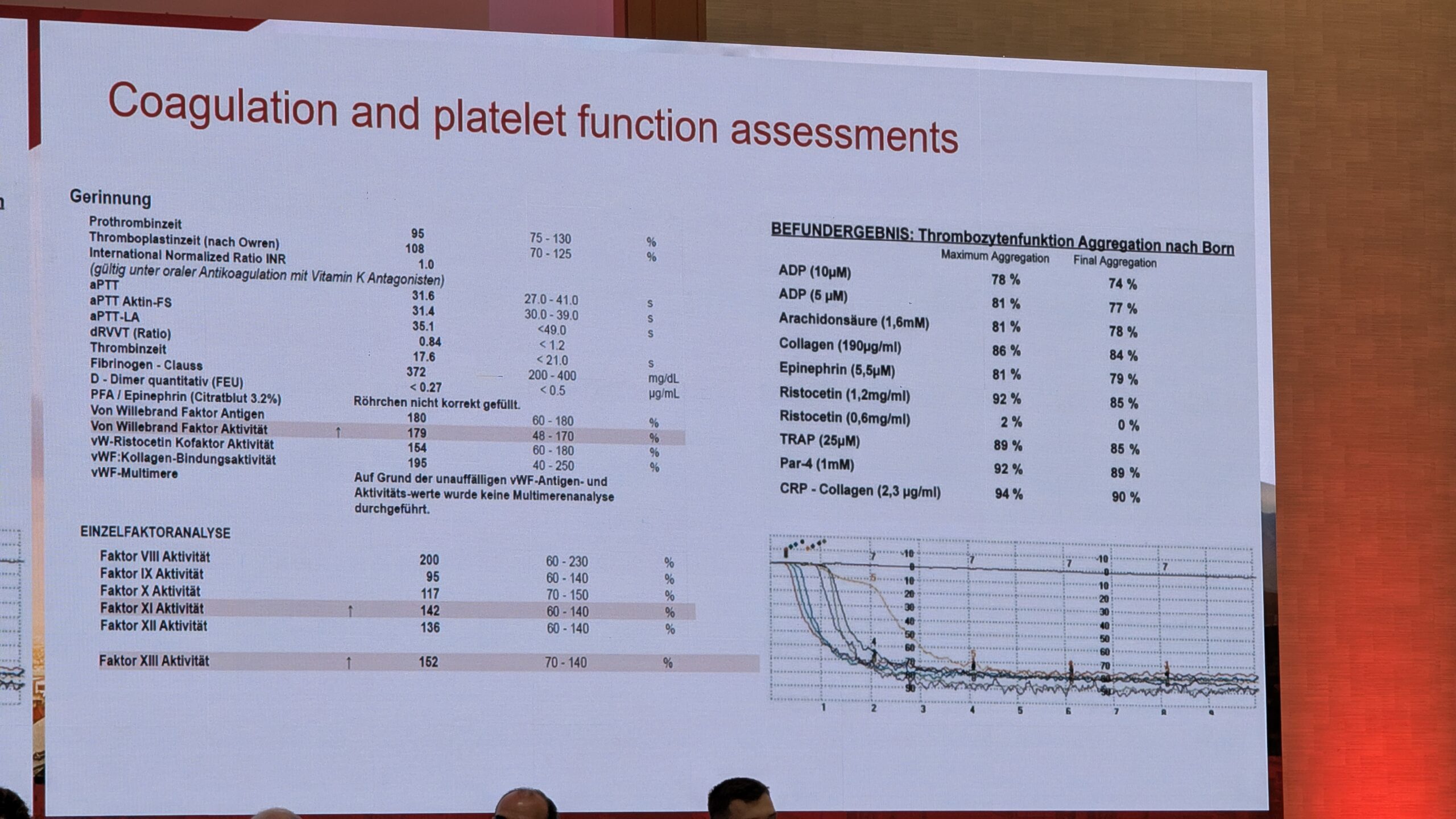
Fibrinogeeni häirete diagnoosimiseks mõõdetakse fibrinogeeni aktiivsust ja antigeeni taset. Kui fibrinogeeni tase on tuvastamatu, diagnoosi hüpotees -afibrinogeneemia. Kui fibrinogeeni antigeen on olemas, kuid aktiivsus on vähenenud, tuleks diagnoosida düsfübrinogeneemiat.
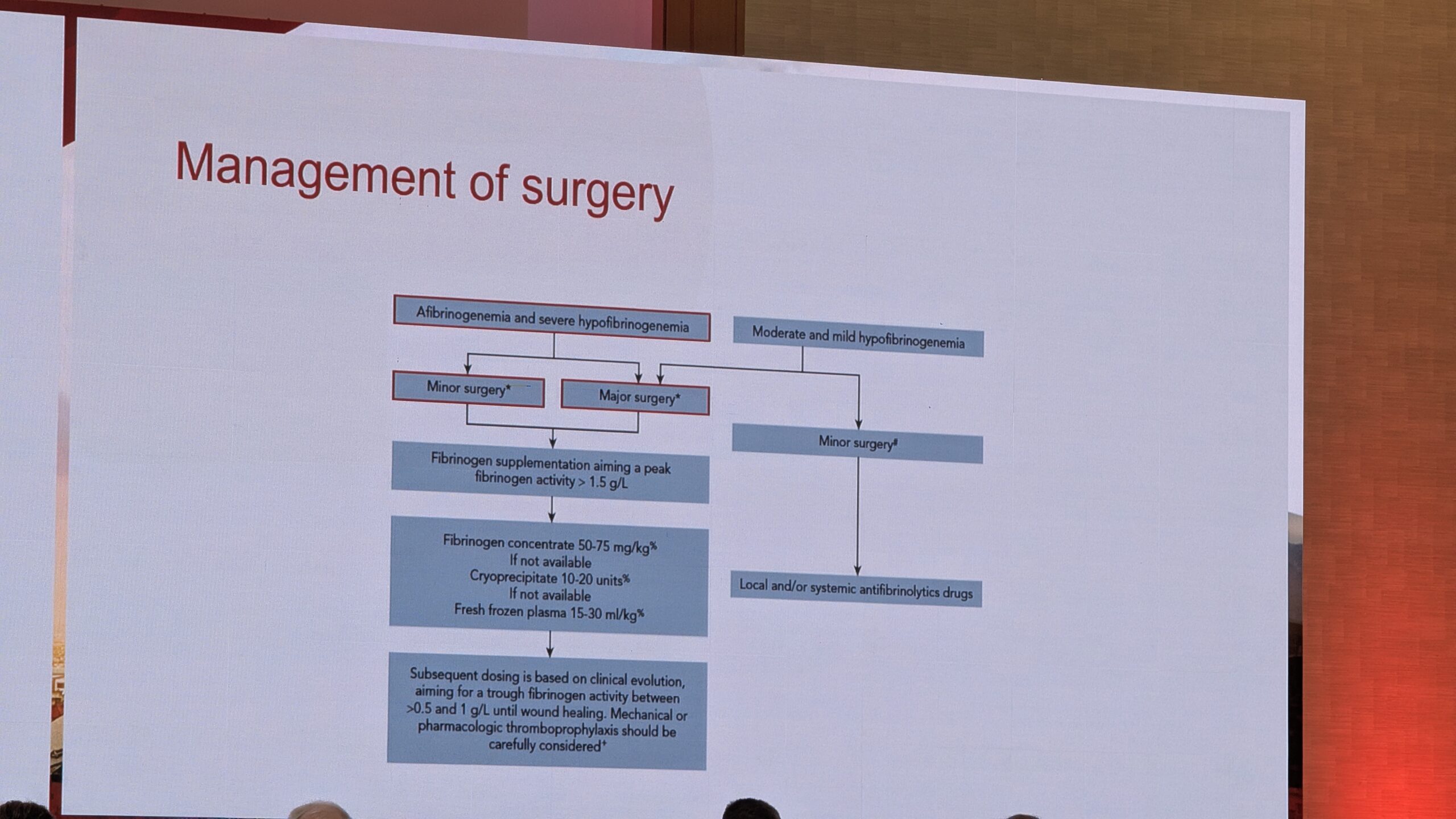
Raviks on parim valik fibrinogeeni kontsentraat. Kontsentraadid (nt RIASTAP/Haemocomplettan, Fibryna ja uus Grifolsi kontsentraat) on saadaval paljudes riikides. Alternatiivide hulka kuuluvad krüopretsipitaat (eriti Põhja-Ameerikas) ja värskelt külmutatud plasma. Fibrinogeeni kontsentraat on parim valik mitmel põhjusel: teadaolev kontsentratsioon igas viaalis võimaldab täpselt annustada, väiksemat kogust ja kiiremat infusiooni ning sellega kaasneb madal nakkus- ja allergiliste reaktsioonide risk.
Profülaktika ja patsientide KVALITEET
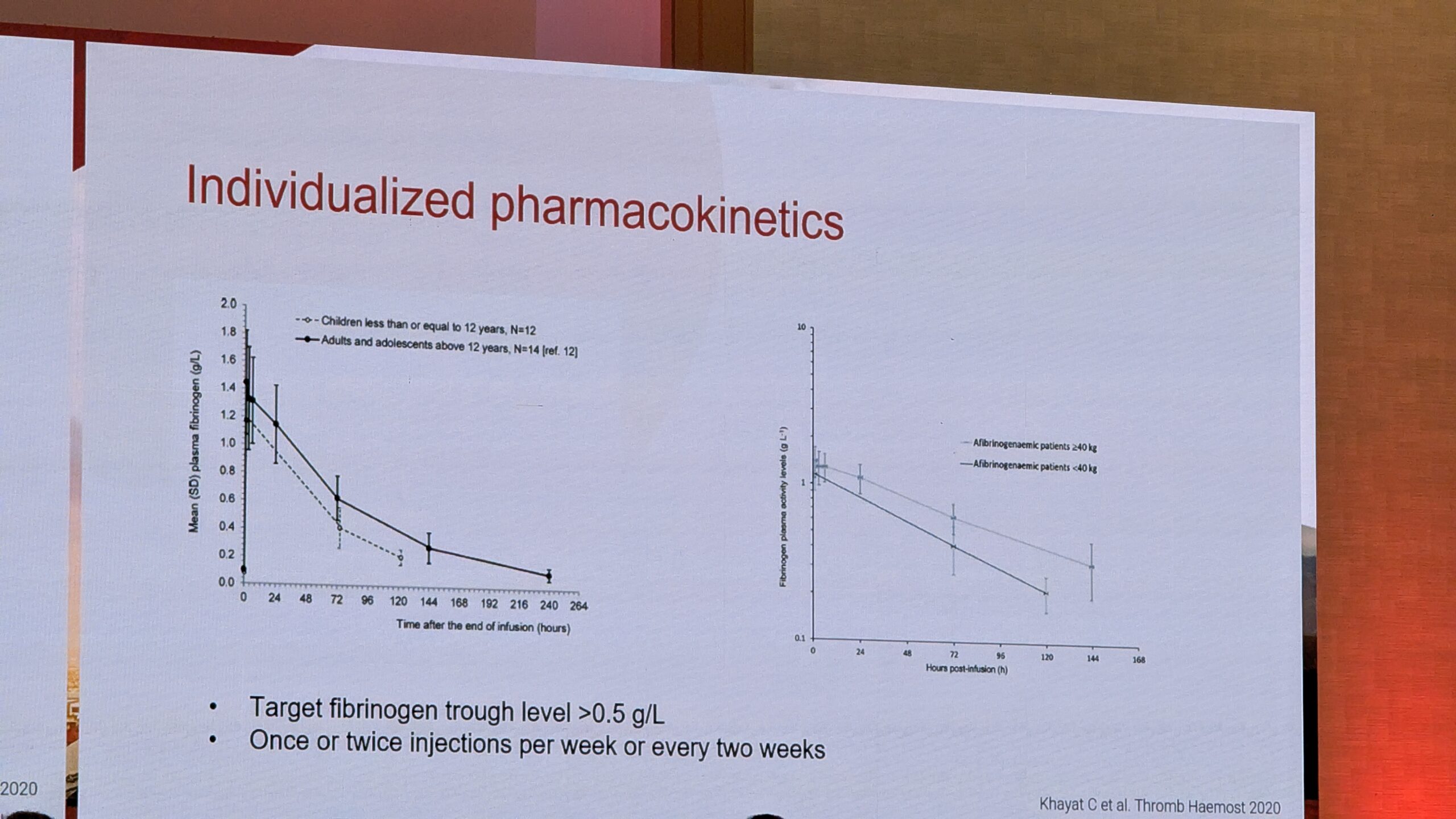
Siiani ei ole piisavalt andmeid, mis toetaksid profülaktilist ravi. Konsensus on siiski alustada profülaktikat kergete, korduvate verejooksude või raske fenotüübi korral. Profülaktiline ravi on oluline ka seetõttu, et raskete fibrinogeeni defektidega patsientidel on suurem oht intrakraniaalsele verejooksule (ajuveritsusele). Profülaktika puhul on oluline arvestada patsiendi farmakokineetikat, kuna esineb erinevusi. Fibrinogeeni poolväärtusaeg on umbes neli päeva, mis lubab soovitada annustamist kord nädalas, eesmärgiga hoida tase üle 0,5 g/L.
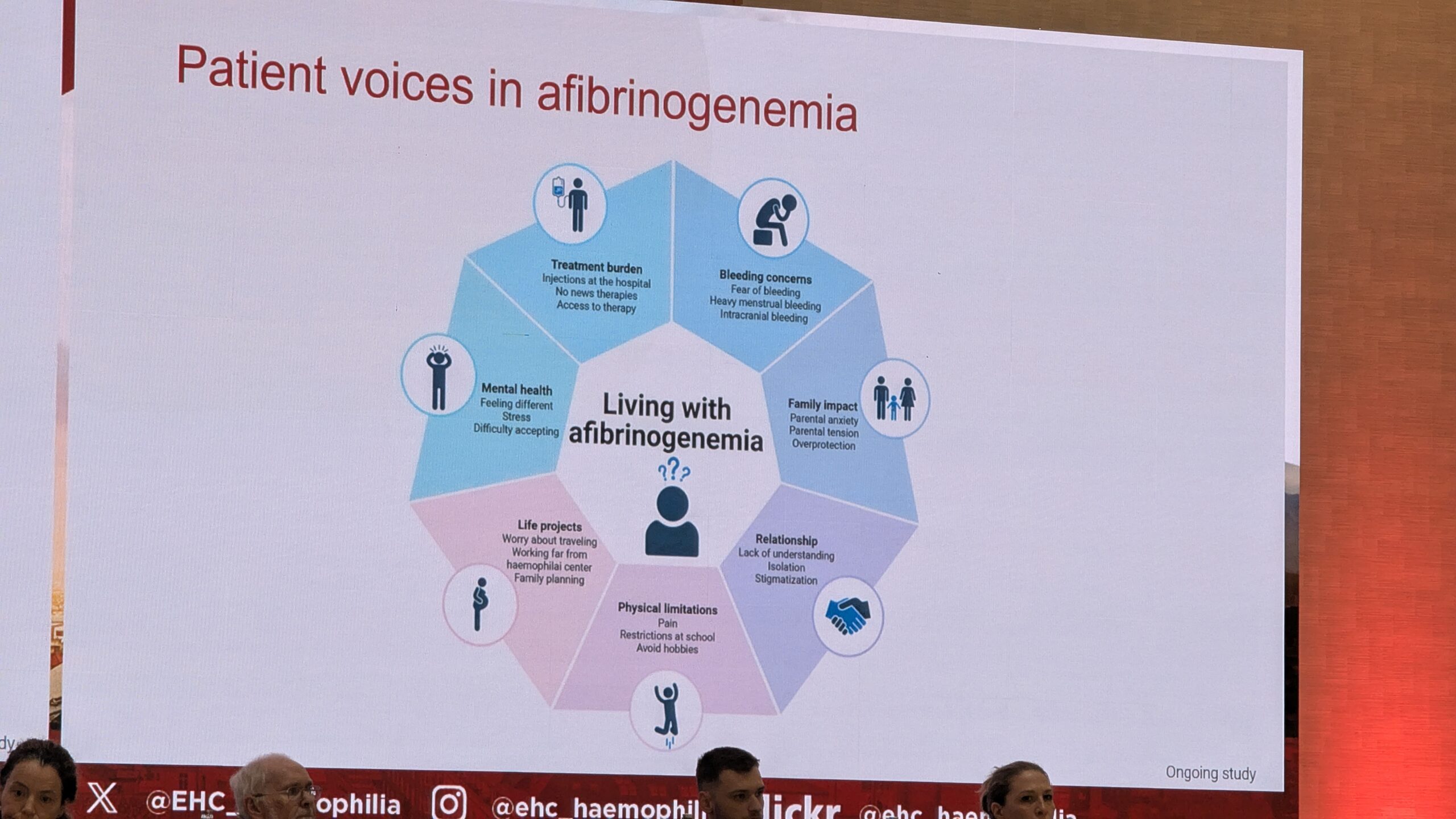
Profülaktiline fibrinogeeni infusioon mõjub patsientidele positiivselt, säilitades elukvaliteedi (HR-QoL). Uuringus näidati patsientidel, kes said fibrinogeeni kontsentraati krüopretsipitaadi asemel, elukvaliteedi paranemist. Samuti oli elukvaliteet kõrgem patsientidel, kes tegid infusioone kodus, võrreldes nendega, kes pidid seda saama haiglas. Elukvaliteeti mõjutavad negatiivselt mitmed tegurid, sealhulgas intrakraniaalse verejooksu hirm, kartus haiglavisiitide ees, füüsilise tegevuse piirangud (valu ja puudumine koolis/tööl) ning ravikoormus (nii infusioonid kui ka juurdepääs ravile).
6.2 Hemofiilia B inhibiitoritega: kas see on endiselt tähelepanuta jäetud rühm? – Dominik Cepic
Dominik Cepic ettekandes oli teemaks haruldane patsientide rühm – inhibiitoritega hemofiilia B patsiendid. Ta alustas sissejuhatust et see on sageli unustatud hemofiilia “alamliik”, kuna on nii harudlane. Ta tõdes, et hemofiilia A saab kogu tähelepanu, seal on rohkem patsiente, ravimeid ja uuringuid, mistõttu hemofiilia B, eriti inhibiitoritega, jääb haruldaseks alamliigiks, kus patsiente sellegi poolest kimbutavad piirangud.
Isiklik lugu ja sotsiaalne mõju
Cepic rõhutas, et statistika taga on alati inimene. Enne uue uuringuravi algust ligi kaheksa aastat tagasi ei suutnud ta normaalselt toimida, oli pidevalt haiglas ja tal esines veritsusi, mis ei peatunud. Ta tunnistas, et tol ajal ei oleks ta isegi mõelnud kogukonna tegevustes osalemisele.
Kuigi hemofiilia B inhibiitoritega on haruldane, on siingi oma probleemid. Olukord on viimase 20 aasta jooksul märkimisväärselt paranenud, kuid ta usub, et saab veelgi paremini. Patsientide ravivalikuid on vähe– Cepic kasutas aastaid sama tüüpi ravimit veritsuste peatamiseks, mida ta sai sünnist saadik.
Teadlikkuse ja eestkostetöö vajadus
Dominik Cepic rõhutas kogukonna tugeva eestkostetöö (advocacy) vajalikkust. Paljudel tema noortel sõpradel selle haigusega, mille raviga on tekkinud inhibiitorid on sarnaseid või isegi raskemaid lugusid. Kuna nende rühm on nii väike, ei pruugi isegi väiksemate linnade arstid hemofiilia B-st inhibiitoritega kuulnud olla. Seetõttu patsiendid seisavad silmitsi olukordadega, kus neid kardetakse ravida, isegi kui neil on õiged ravimid kaasas.
Ta viitas kogukonna toetuse olulisusele, kus noorel hemofiiliaga lapsel, kellel olid rasked ajuveritsused, aidati leida ja annetustega vajalik ravim. Cepic väljendas rõõmu, et saab hetkel uuringus osaledes uuringu ravi ja, et on tulemas uued, elu muutvate raviviisid. Loodab tulevaste suukaudselt manustatavate ravimite ning geeniteraapia progressi üle. Teavitustöö on protsess, mis viib lõpuks innovatsioonini. Rõhutas, et me peame alati naasma algtõdede juurde: verejooksud, elukvaliteet, vaimse tervise kvaliteet ja eestkostetöö.
Temale esitatud Patsientide elukvaliteedi küsimusele vastas ta, et kõige kallimaks muutuvad ravimid tervisele, mida saab kas liiga hilja, liiga vähe või üldse mitte. Ebapiisav ravi põhjustab pöördumatut liigesekahjustust ja pikaajalisi probleeme, mis on ühiskonnale kulukamad, kuna patsient ei saa olla funktsionaalne.
6.3 Füsioterapeudi vaatenurk – Melanie Bladen
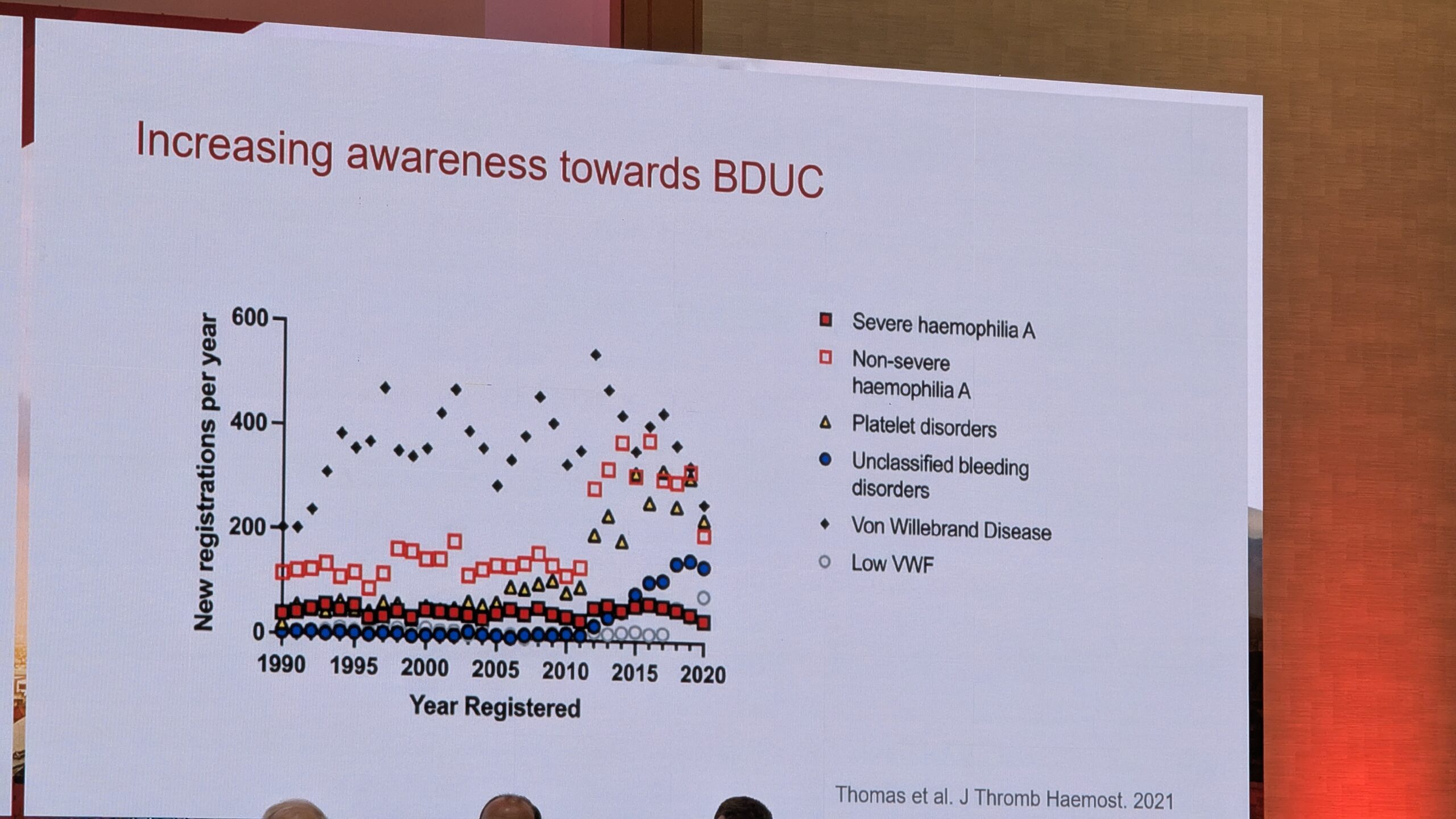
Johanna Gebhart tutvustas patsientide rühma- teadmata põhjusega veritseja- BDUC (ingl. Bleeding Disorder of Unknown Cause). Austira kliinikud tunnistavad oma “kliinilist ignorantsust” nende patsientide suhtes, kelle verejooksuhäiret ei suudeta täpselt selgitada. Kuid nad väärivad uurimist ja ravi.
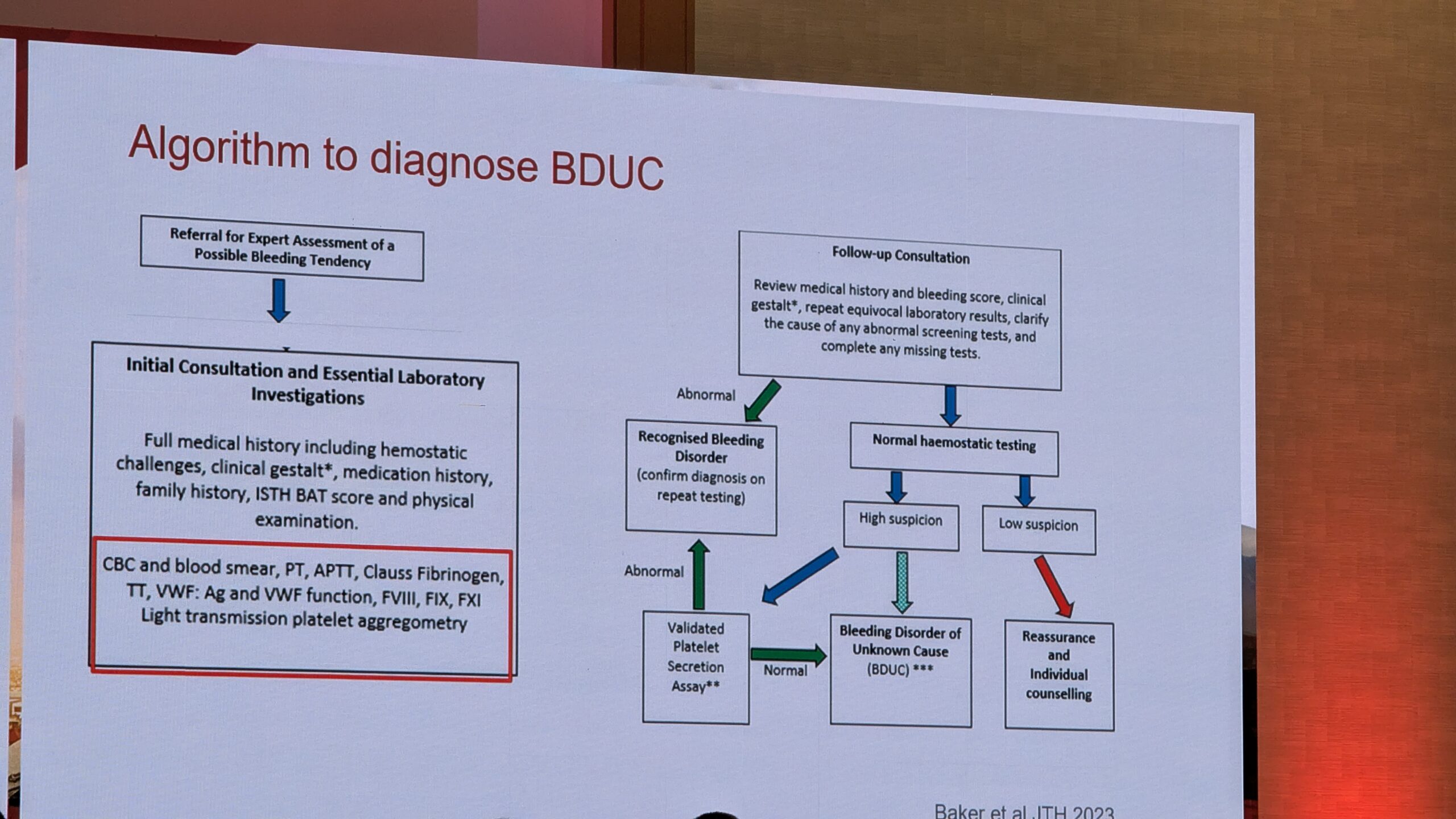
BDUC rühma kliiniline pilt ja diagnoos
BDUC on välistamise diagnoos, mis defineeriti 2024. aastal standardiseeritud uuringutega. See diagnoositakse, kui hoolimata tugevat kliinilisest kahtlusest verejooksuhäirele on kõik põhjalikud diagnostilised testid (nt hüübimisfaktorid 8, 9, 11, Von Willebrandi faktori testid ja vereliistakute funktsiooni testid) normi piires.
Tüüpiline BDUC patsient, dr. Gebhart sõnul on 30-aastane naine, kellel on eluaegne kerge kuni mõõdukas verejooksule kalduvus. Selle hulka kuuluvad sünnitusjärgsed verejooksud, pikenenud menstruatsiooniverejooksud ja suurenenud verevalumid väikeste vigastuste korral.
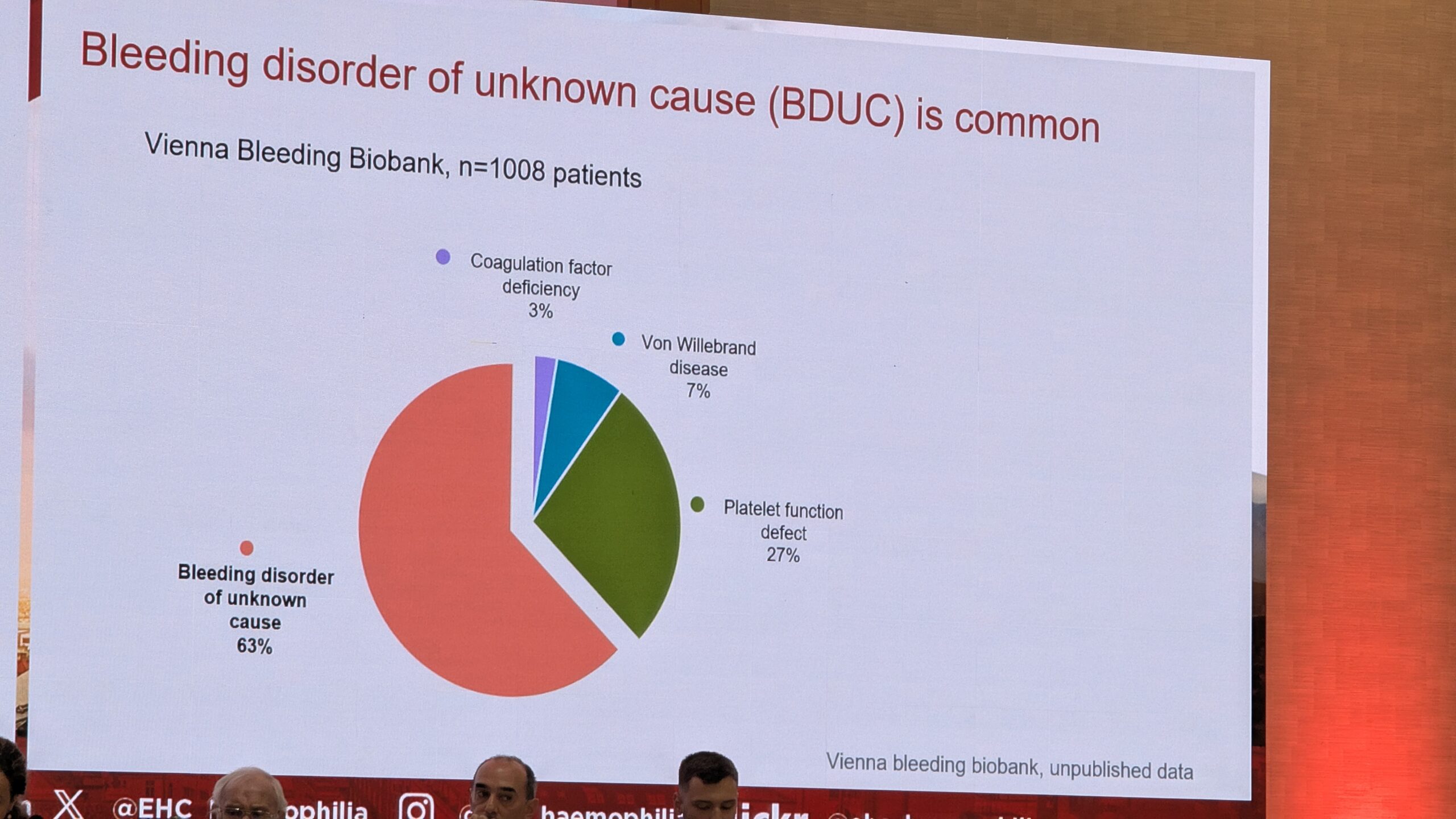
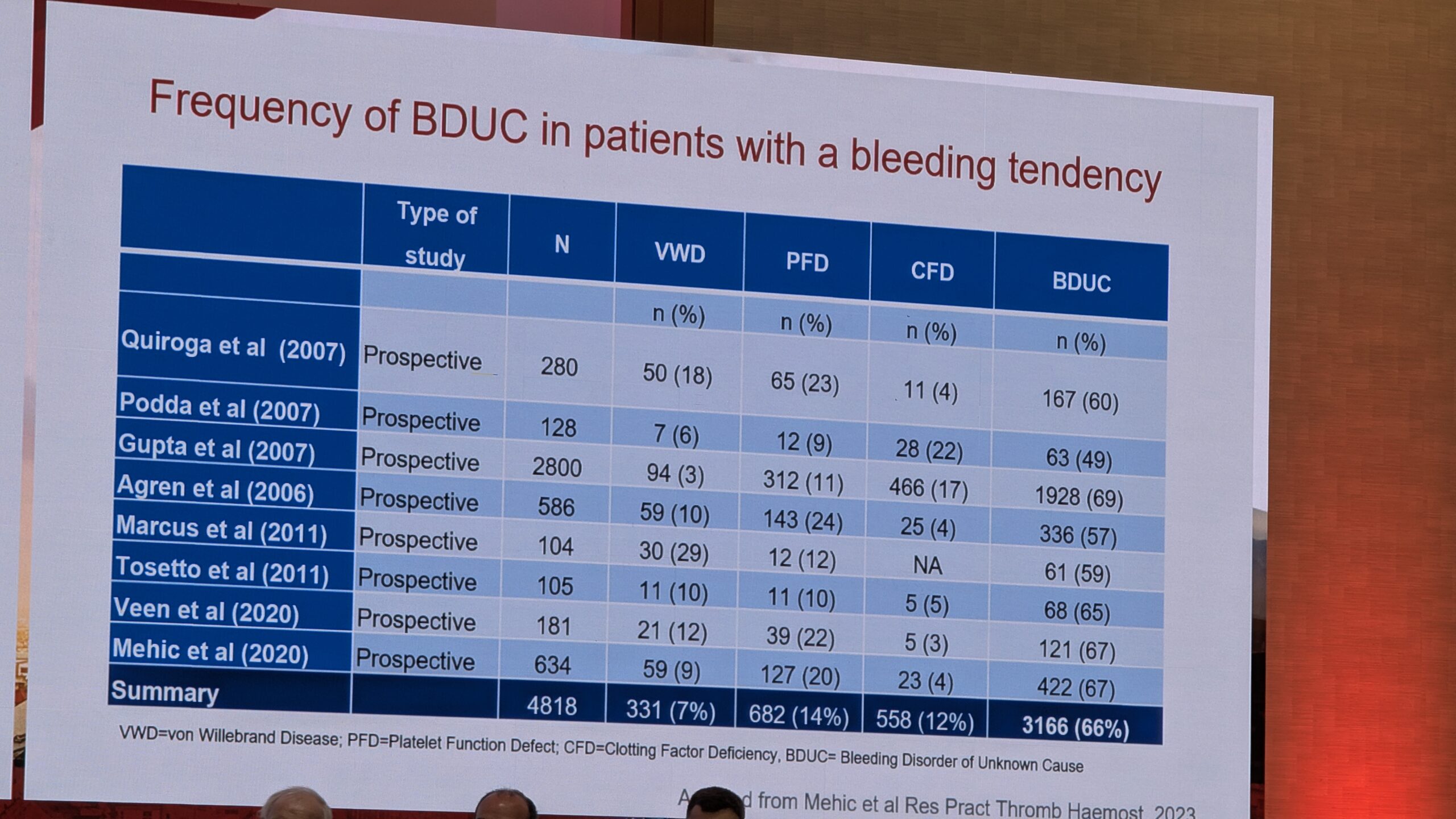
Levimus ja fenotüüp
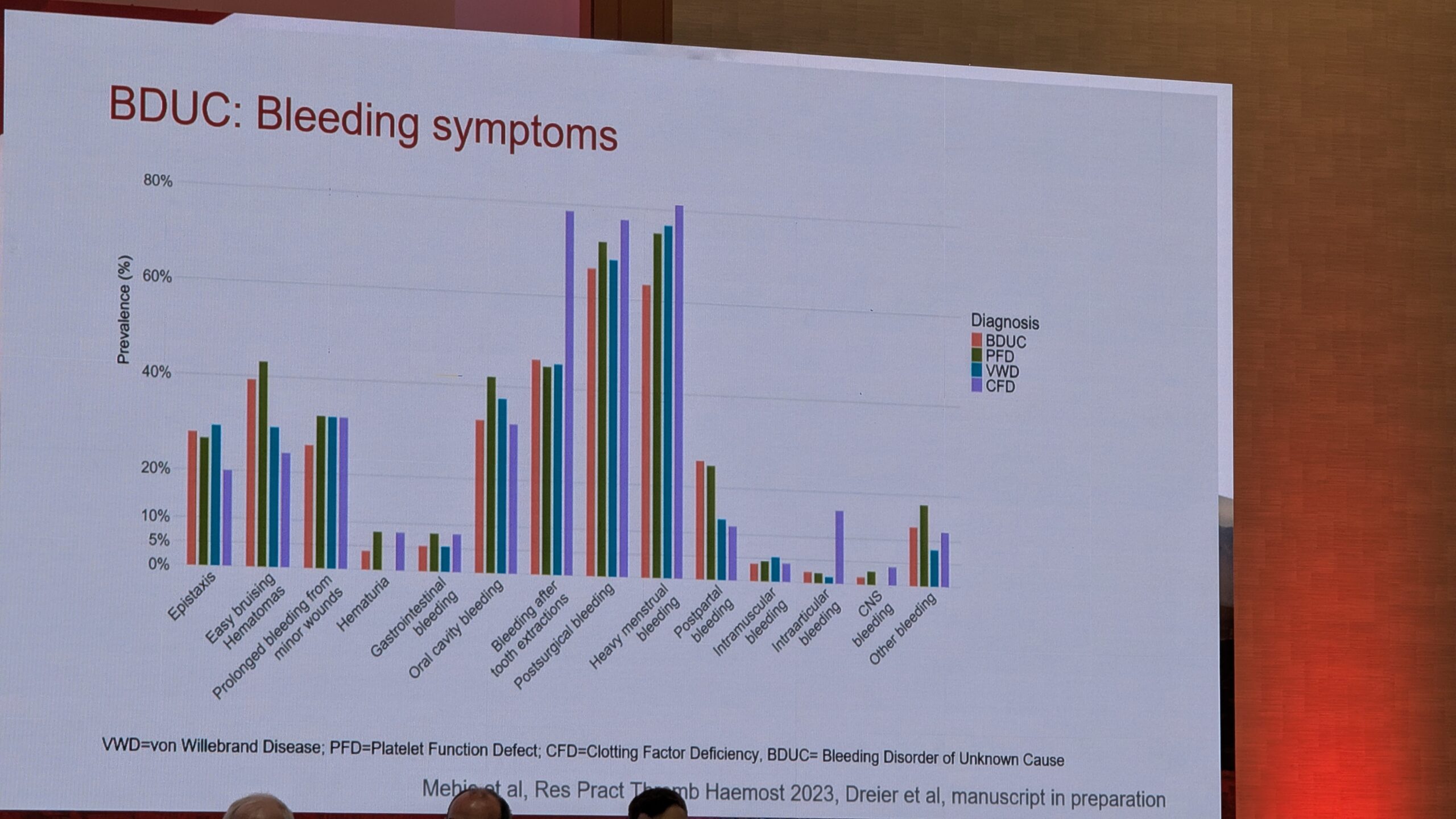
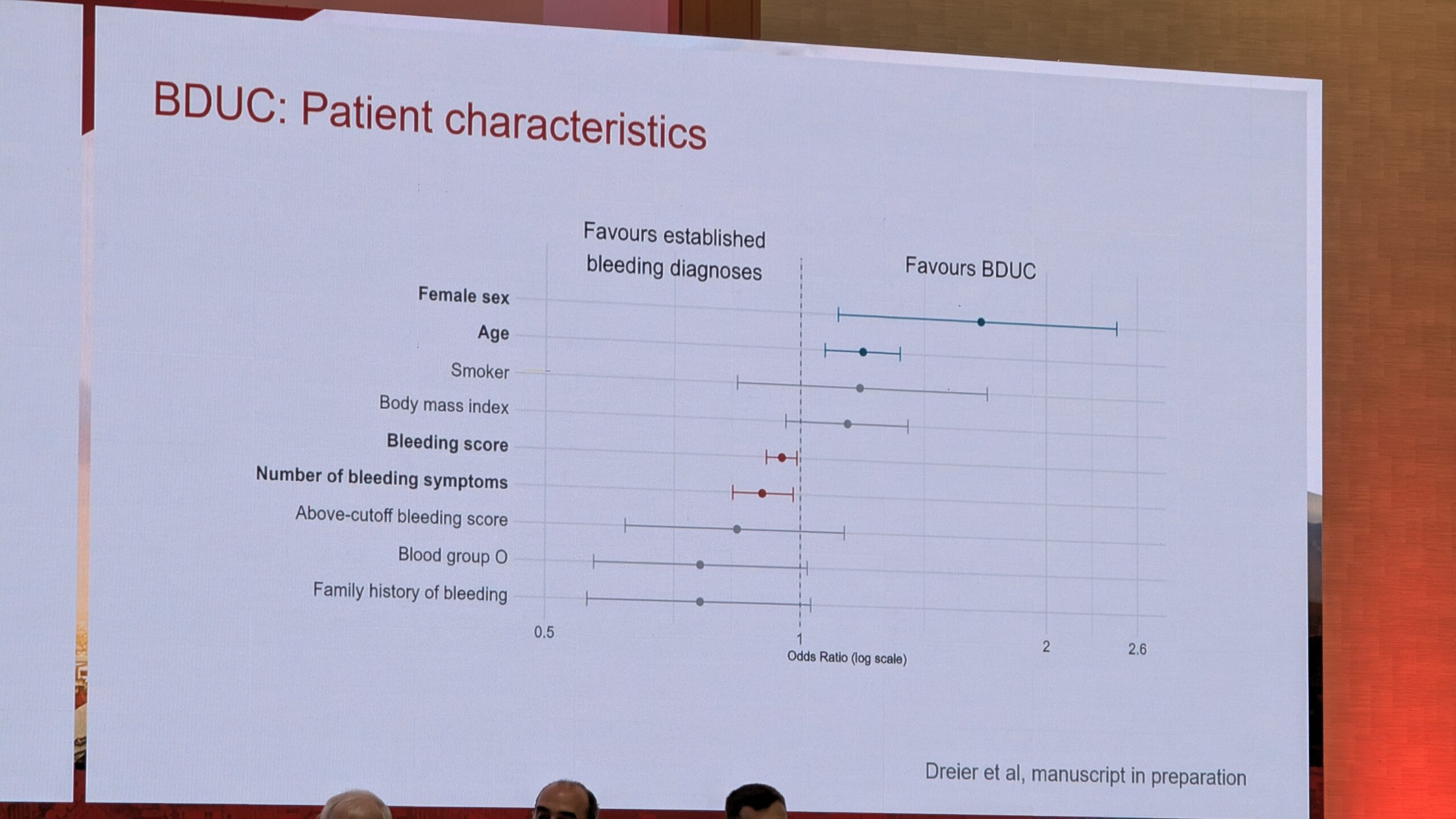
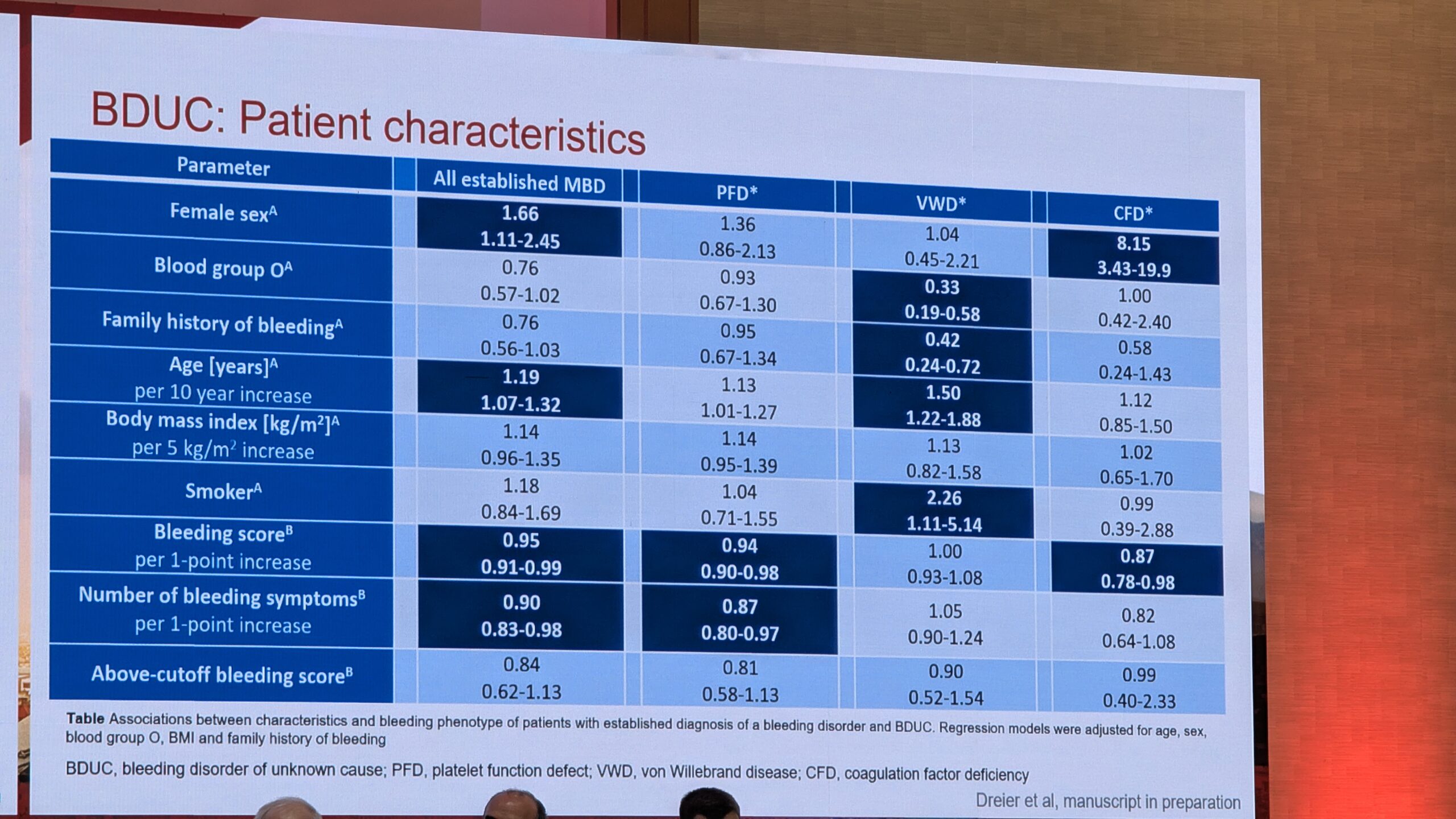
Uuringute põhjal on BDUC levinud: kahel kolmandikul patsientidest, kes pöördusid verejooksu kalduvuse tõttu kliinikutesse ilma eelneva diagnoosita, tuvastati BDUC, kui võimalikud veritsuspõhjused välistati. BDUC patsientide kliiniline fenotüüp on sarnane teiste kergete või mõõdukate verejooksuhäiretega, nagu Von Willebrandi tõbi (tüüp 1) või vereliistakute funktsioonihäired. Nendel patsientidel esinevad sageli kergesti tekkivad verevalumid ja limaskestade verejooksud (nt ninaveritsused). BDUC patsientide hulgas on sagedamini naisi ja nad on nooremad kui teiste diagnoositud verejooksuhäiretega patsiendid.
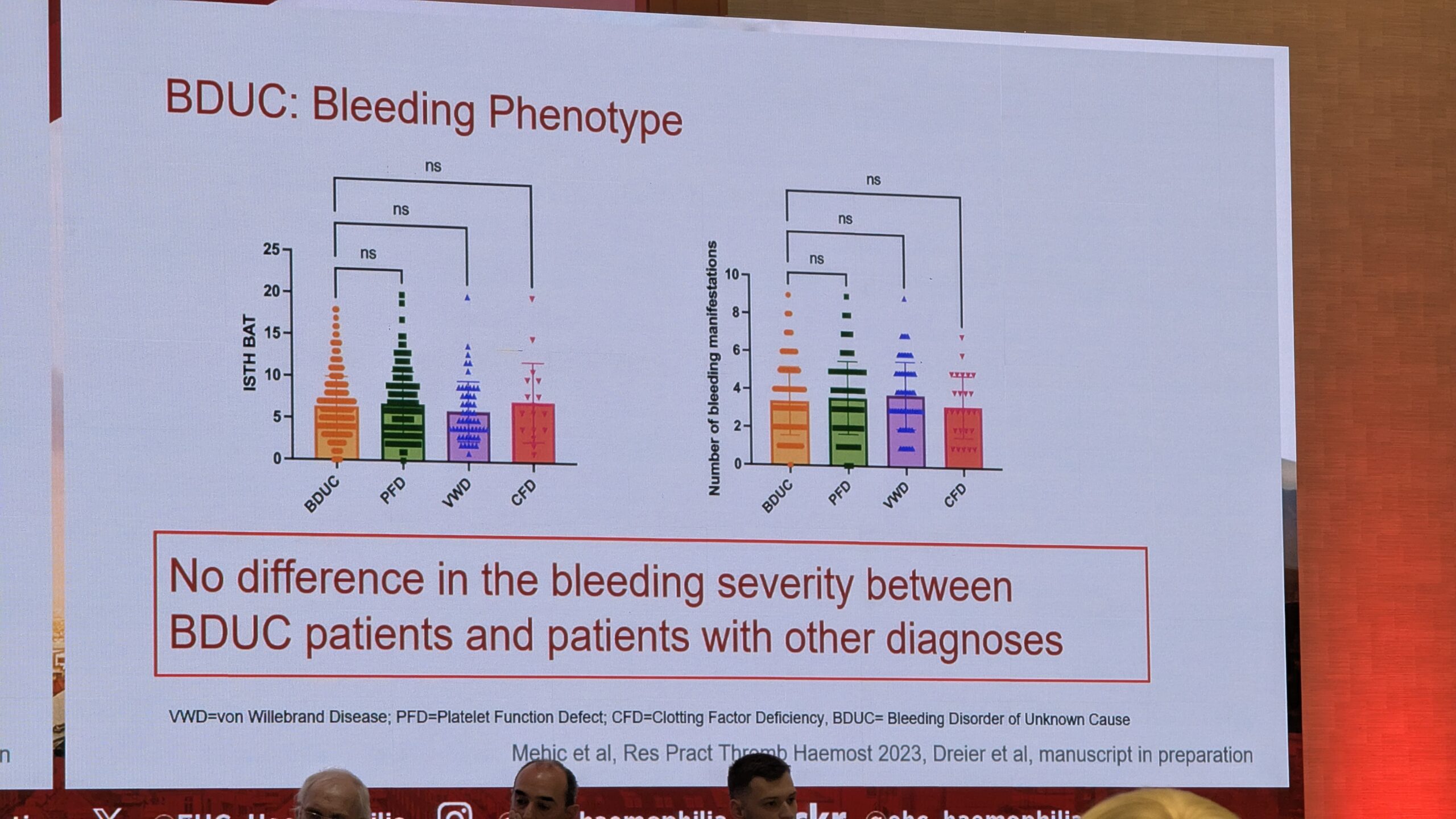
Patofüsioloogia, elukvaliteet ja ravi
Hoolimata sellest, et BDUC on välistamise diagnoos, leiti, et nendel patsientidel esineb hemostaasi (nt trombi genereerimise, viskoelastse testimise ja plasma hüübimise) kõrvalekaldeid võrreldes tervete kontrollrühmadega. Siiski on nende verejooksu mehhanismid endiselt suures osas tundmatud.
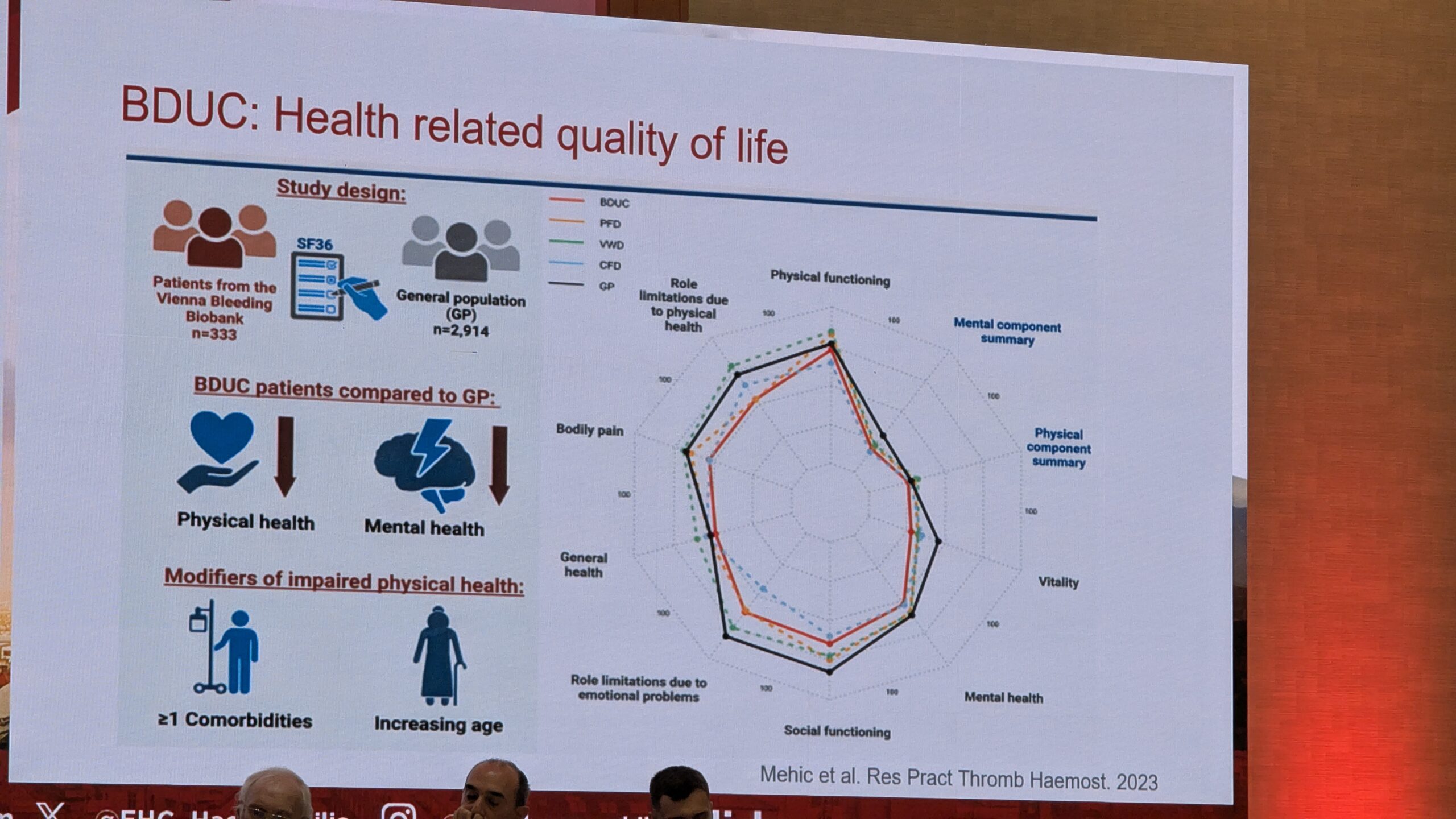
BDUC-ga patsientide elukvaliteet on halvenenud võrreldes üldpopulatsiooniga ning on samaväärne teiste verejooksuhäiretega patsientidega. See rõhutab vajadust tegeleda nende seisundiga, kuna see mõjutab tugevalt patsientide elu.
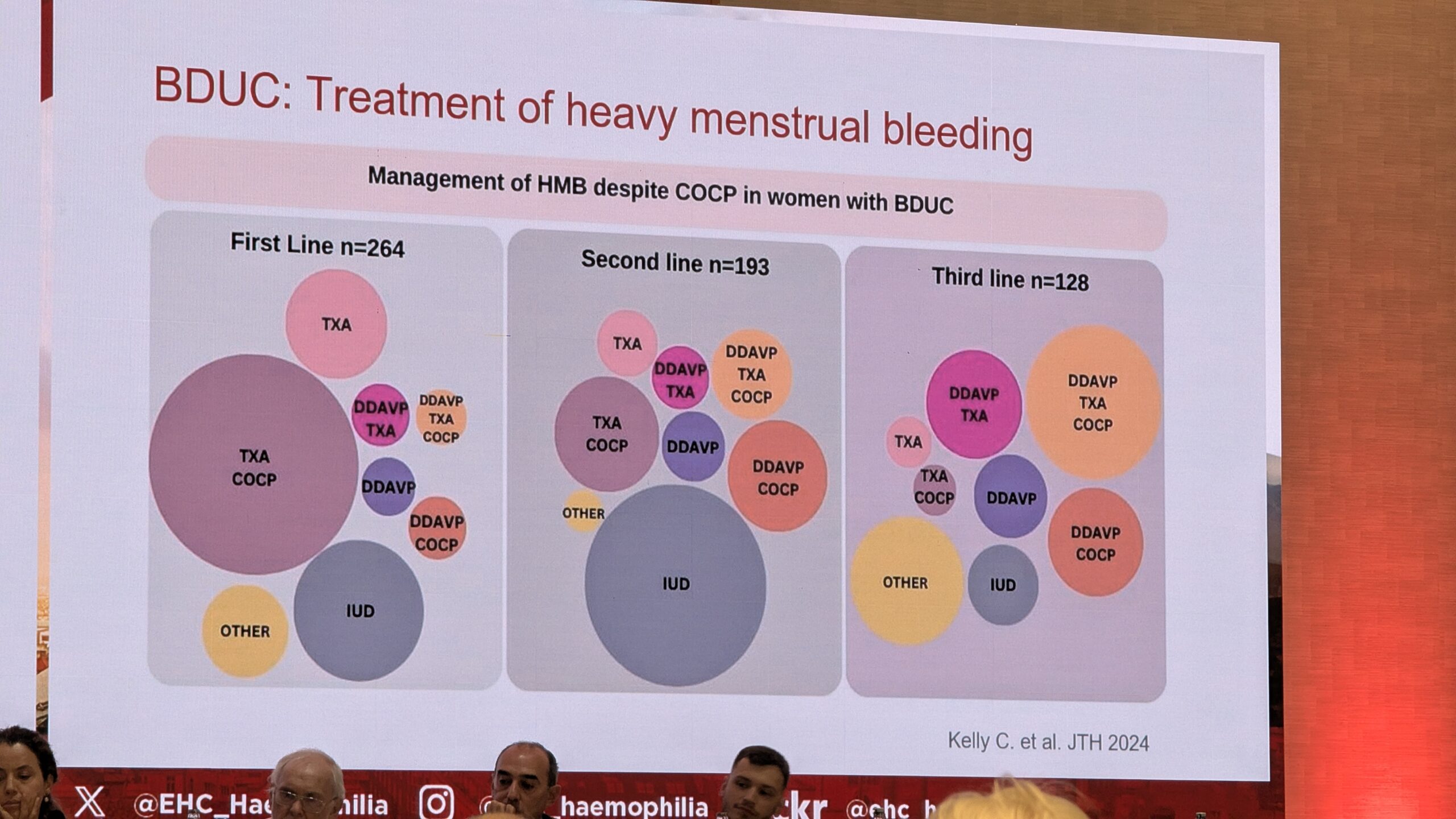
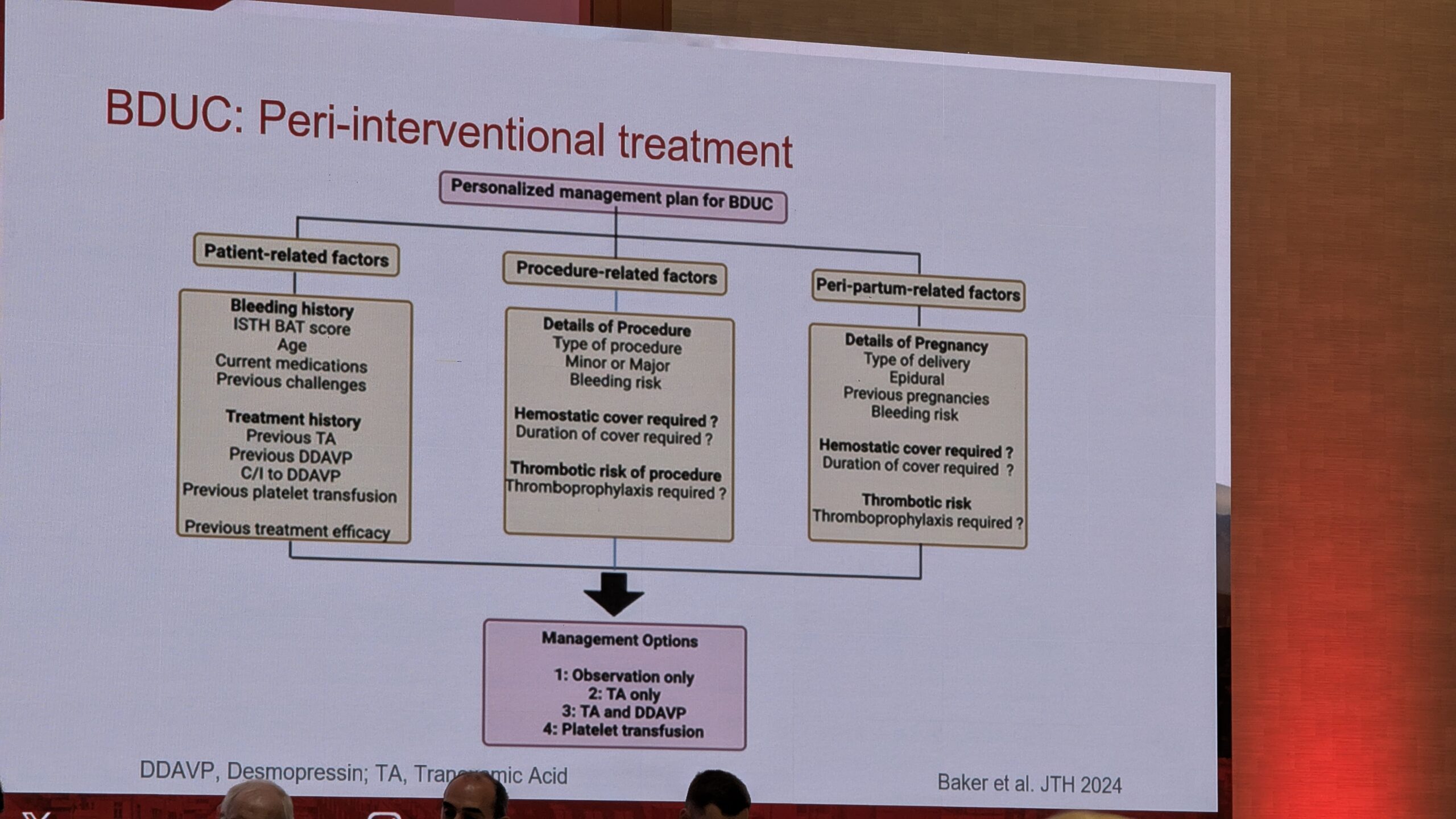
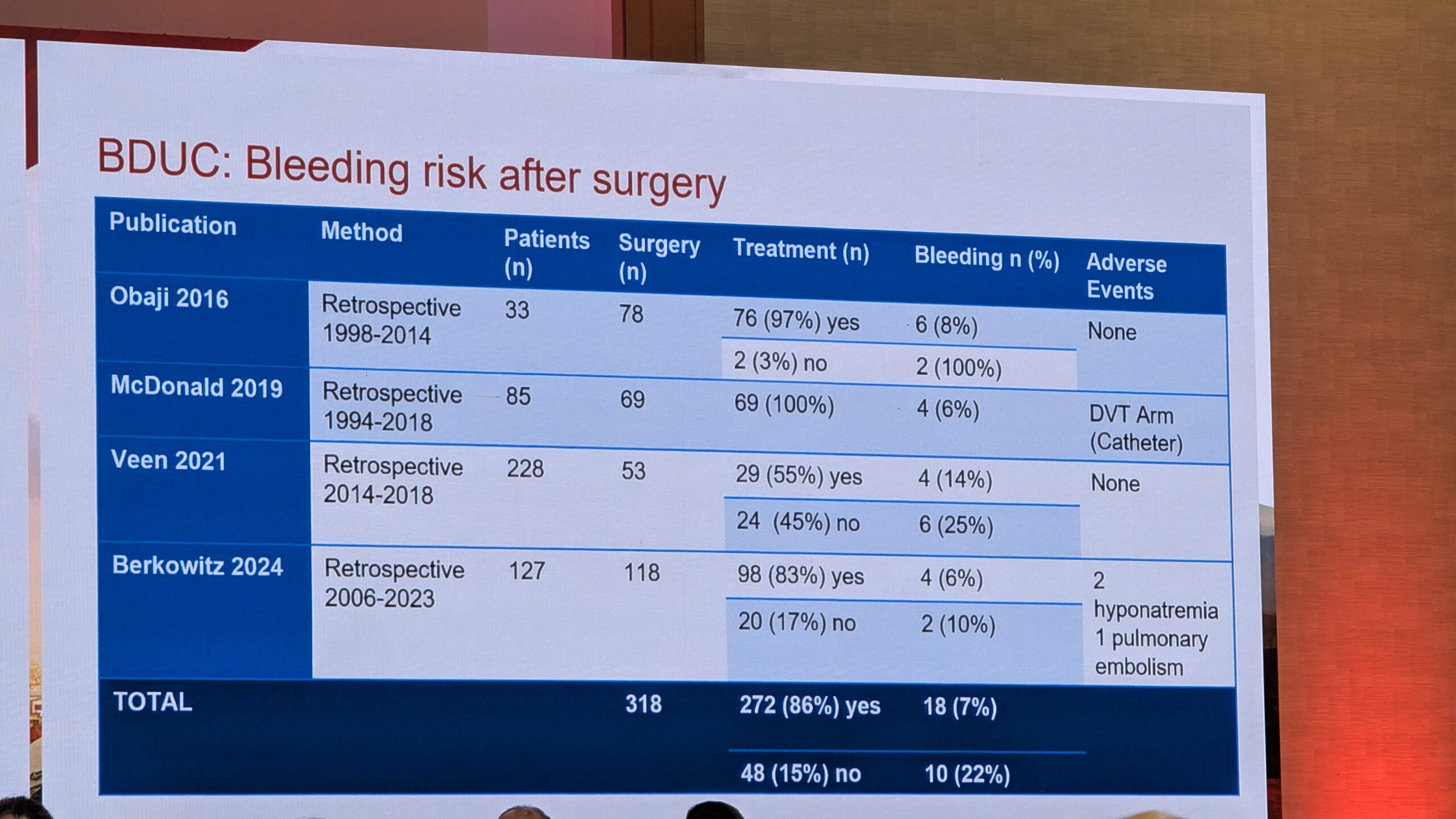
Ravivalikud on piiratud ja andmeid on vähe. Valikuks on hormonaalseid kontratseptiive (naistel), desmopressiini (DDAVP) ja traneksaamhapet (antifibrinolüütikum). Kirurgiliste protseduuride ja sünnituste puhul on verejooksu risk oluline. Näiteks sünnituse järgselt esines verejooks 30% ravitud BDUC patsientidest ja üle pooltel ravimata patsientidest, mis näitab, et isegi ravi korral on BDUC rühm endiselt kõrge riskiga.
Traneksaamhape (TEA) BDUC ravi peamise osana
Põhiline ravivalik BDUC korral on trankesaamhape. Üks hambaarst-ekspert rõhutas, et see on sageli peamine ravim ja kahjuks ei ole see ei ole paljudes riikides kättesaadav. See on oluline hammaste eemaldamisel, mis on ka nende patsientide sageli esimene verejooksu episood elus.
Dr. Gebhart ütles kokkuvõtteks et BDUC on levinud, kerge kuni mõõduka verejooksu kalduvusega haigus, mille mehhanismid on teadmata ja mille raviks on piiratud valikud. Pidas oluliseks seda patsiendide rühma uurida ja neile ravijuhendid välja töötada.
7. 5. sessioon – SLAM-sessioon
7.1 Ortopeedia edusammud: liigeseasendusest kõhrekoe konstrueerimiseni – Dr. Gianluigi Pasta
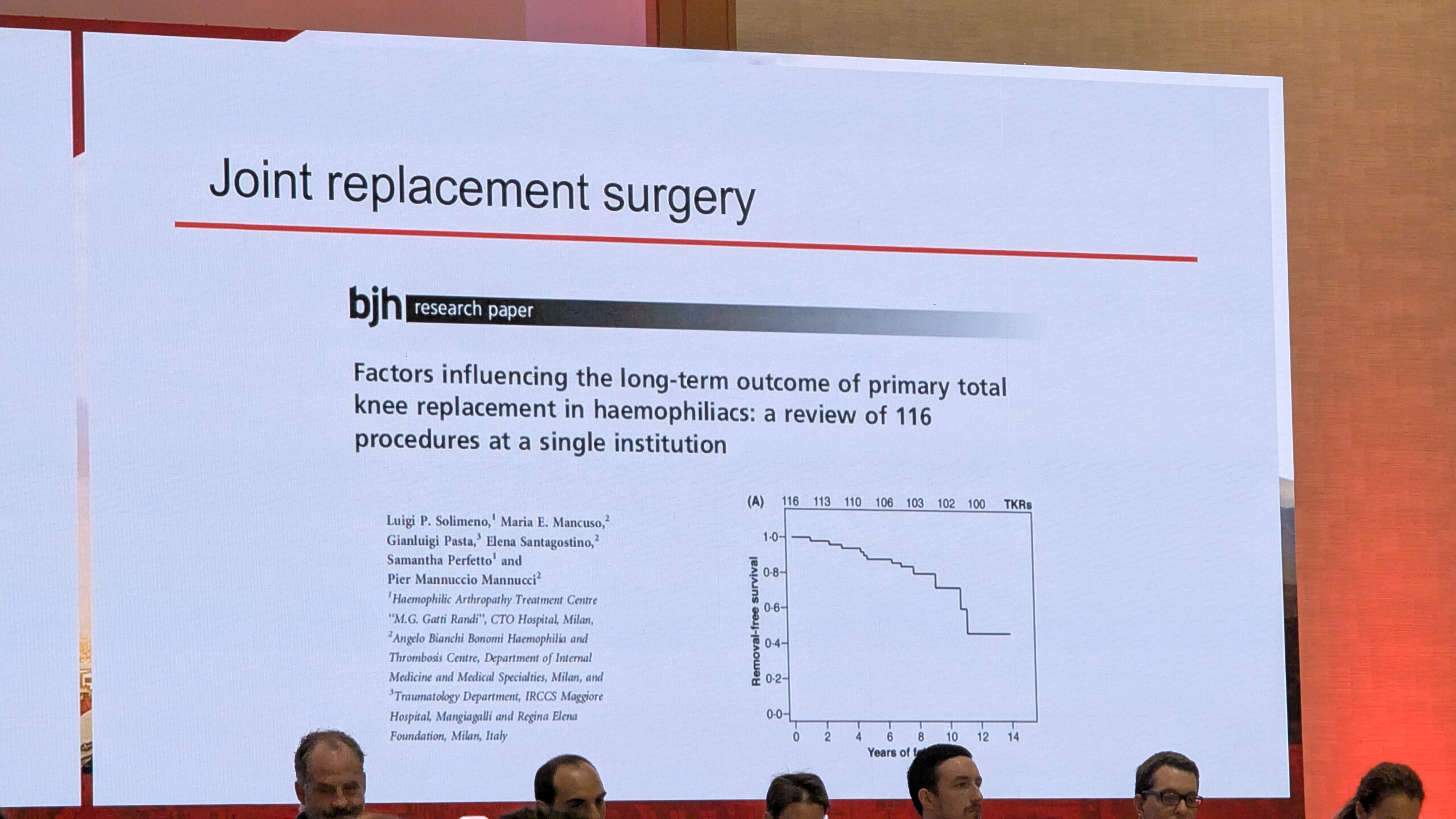
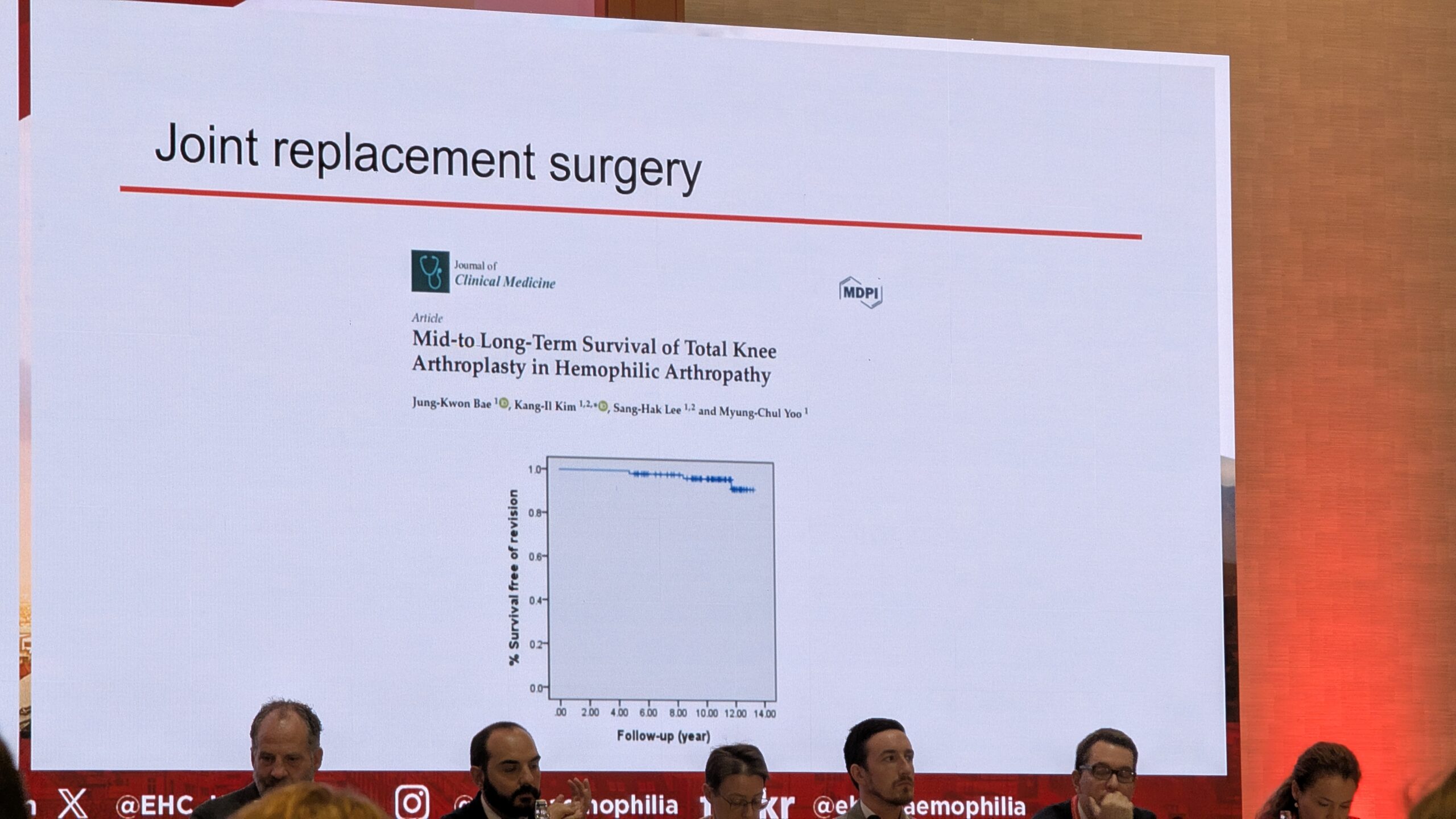
Dr. Gianluigi Pasta rõhutas, et ortopeedias on tehtud suuri edusamme, eriti põlveliigese asenduse valdkonnas. Põlveliigese asendus on ohutu ja efektiivne protseduur hemofiiliaga inimestele, mida kinnitavad ka Maailma Hemofiilia Föderatsiooni (WFH) soovitused. Aastate jooksul on paranenud elulemuskõverad.
Põlveliigese asenduses on head tulemused
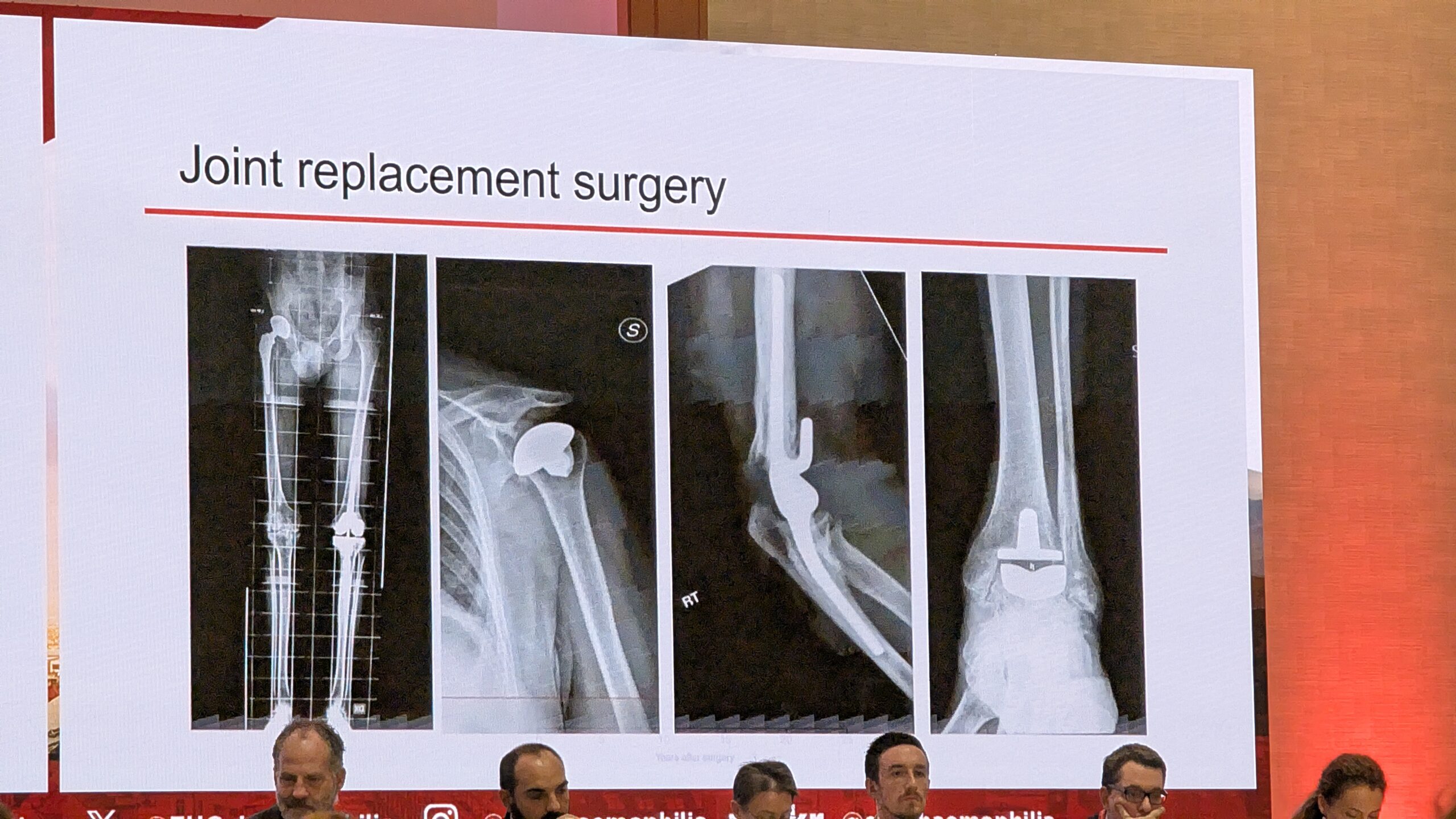
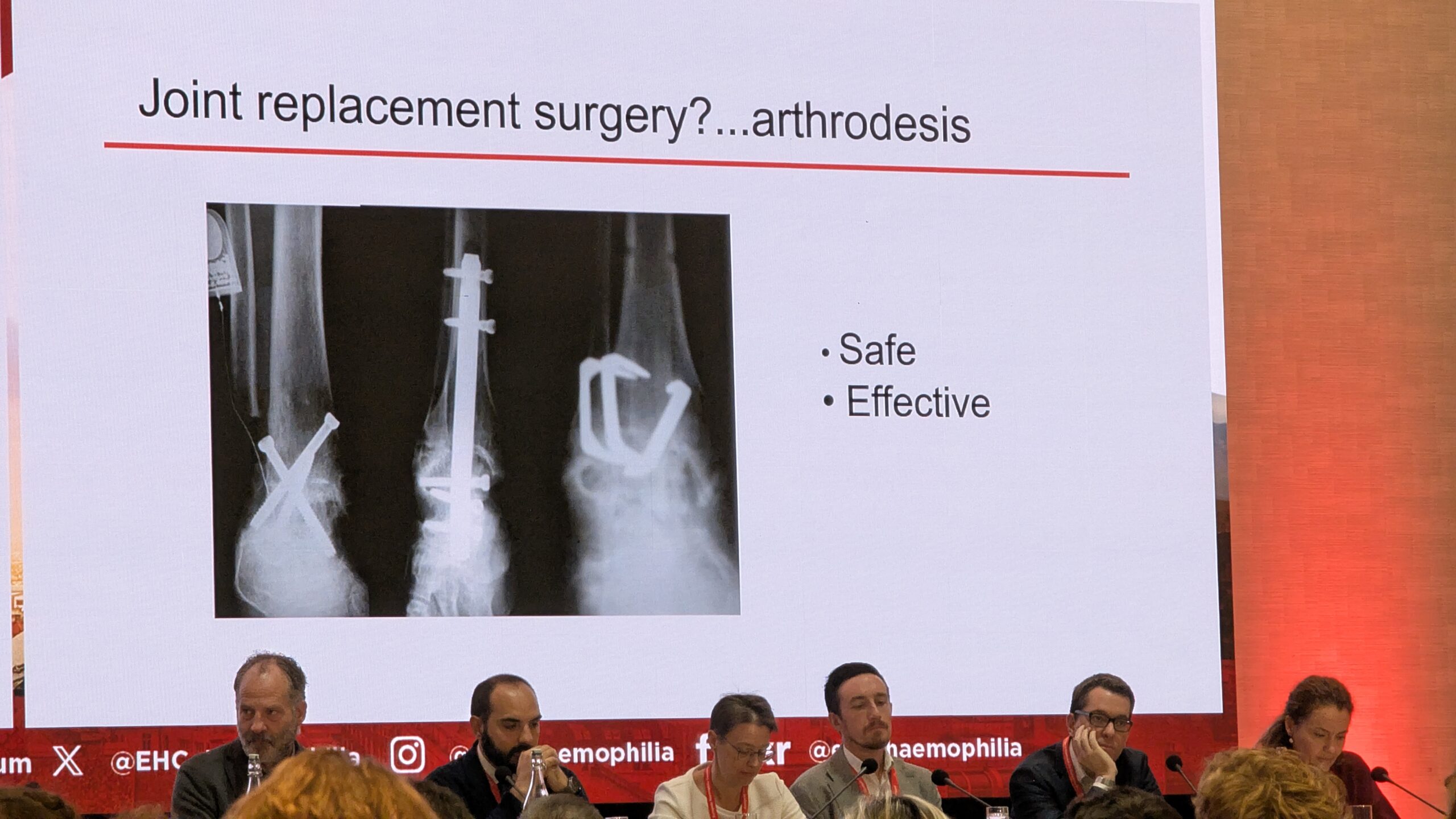
Kahjuks see ei laiene aga sama eduga teistele liigestele. Näiteks puusaliigese asendusel ei ole sama rahuldavaid tulemusi kui põlveliigese asendusel. Eriti keeruline on olukord hüppeliigese asendusoperatsiooniga. Paljud kirurgid eelistavad hemofiiliaga inimeste puhul pahkluu asendusoperatsioonile pigem pahkluu artrodeesi (liigese jäigastamine), kuna varasemate andmete põhjal on sellel protseduuril paremad tulemused. Dr. Pasta aga tunnistas, et viimase kümne aasta jooksul on pahkluu kirurgias tehtud märkimisväärseid edusamme materjalide, kirurgilise tehnika ja kogemuste osas ning tulemused on julgustavad pahkluu asenduse jätkamiseks.
Tehnoloogia ja regeneratiivne meditsiin
Tulevik toob ortopeedilistesse operatsioonidesse tehnoloogilist abi, nagu näiteks robotkirurgia. Oluline on parandada implantaadi elulemust (survival of the implant), kuid hemofiilia valdkonnas peetakse veelgi tähtsamaks leida lahendusi infektsiooni määra vähendamiseks pärast liigese asendamist.
Dr. Pasta käsitles ka regeneratiivse meditsiini (nt kõhre inseneeria) valdkonda, märkides, et see on meditsiiniringkondades ja isegi igapäevastes vestlustes kuum teema. Siiski on hemofiilia artropaatia (liigesehaiguse) regeneratiivne ravi keeruline ja piiratud. Praegu on regeneratiivne meditsiin kättesaadav kroonilise põletiku raviks liigestes, mitte niivõrd kõhredefektide raviks. Eesmärk on ravida sinoviiti (liigesepõletikku) ja seda tagasi pöörata mitte ainult reumatoloogilise raviga, vaid ka muude vahenditega. Näiteks uuritakse, kuidas näiteks trombotsüütiderikas plasma (PRP) võiks ravida kroonilist sünoviiti. Dr. Pasta rõhutas, et tulevikus peaks ortopeediline strateegia liikuma asendamiselt liigese säilitamise suunas, ehkki elukvaliteedi parandamine on kirurgide peamine eesmärk. Meeskonna töö tagab ortopeedilise protseduuri edukuse.
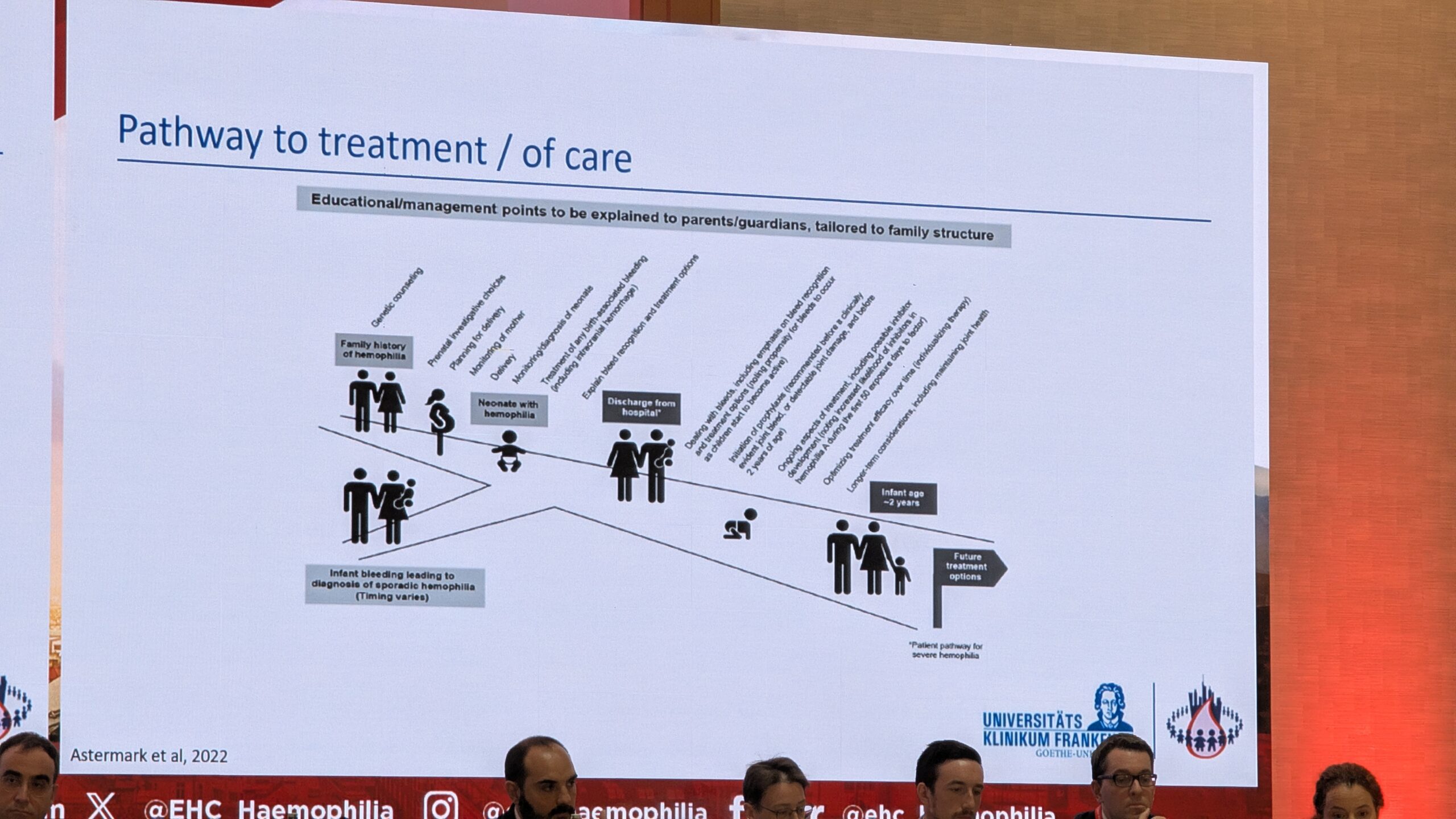
7.2 Millal ja kuidas alustada profülaktikat varem ravimata patsientidel? – Dr. Christoph Königs
Dr. Christoph Königs käsitles kriitilist küsimust: millal ja kuidas alustada profülaktikat varem ravimata patsientidel (PUPs), nentides, et selle kohta on kahjuks vähe tõenduspõhist teavet. Olemasolevad andmed põhinevad asendusravimitel, mida paljudes riikides enam ei kasutata, kuna need on üle kümne aasta vanad. See tekitab dilemma: kas tugineda vanematele andmetele või kasutada kaasaegset ravi.
Vajadus varajase konsultatsiooniga
Dr. Königs rõhutas, vanemate psühholoogilise nõustamise alustamisega kohe diagnoosimise hetkel. Hemofiilia diagnoos on perele šokk, mis tabab neid kui ootamatu “veoauto”. Eriti neid peresid, kus hemofiiliat ei ole varem esinenud. Nad seisavad silmitsi kahtlustustega oma lapse väärkohtlemises. See on suur draama. Tema kogemuse kohaselt on alguses info vanematel raskesti vastuvõetav. Seetõttu on tähtis keskenduda lihtsale teadmisele: lapsel on haigus, mis ei kao.
Profülaktika ajaline valik
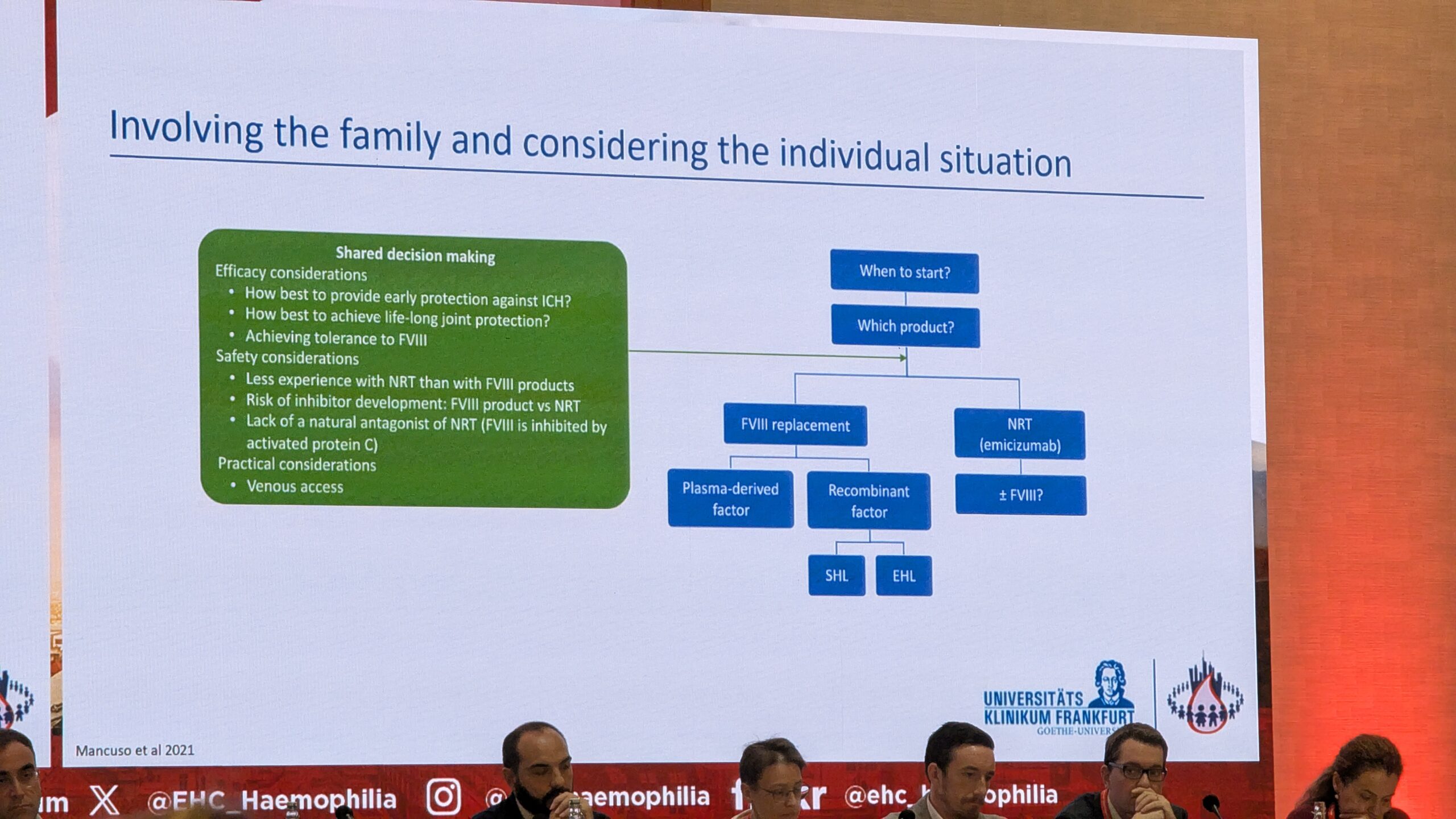
Dr. Königs toonitas, et raviotsused, eriti profülaktika alustamine, tuleb teha koos perekonnaga. Meil ei ole ühte „parimat ravi“ kõigile. Koos planeerimine on oluline, et ravi sobiks perele ja lapsele, sest see annab parima tulemuse.
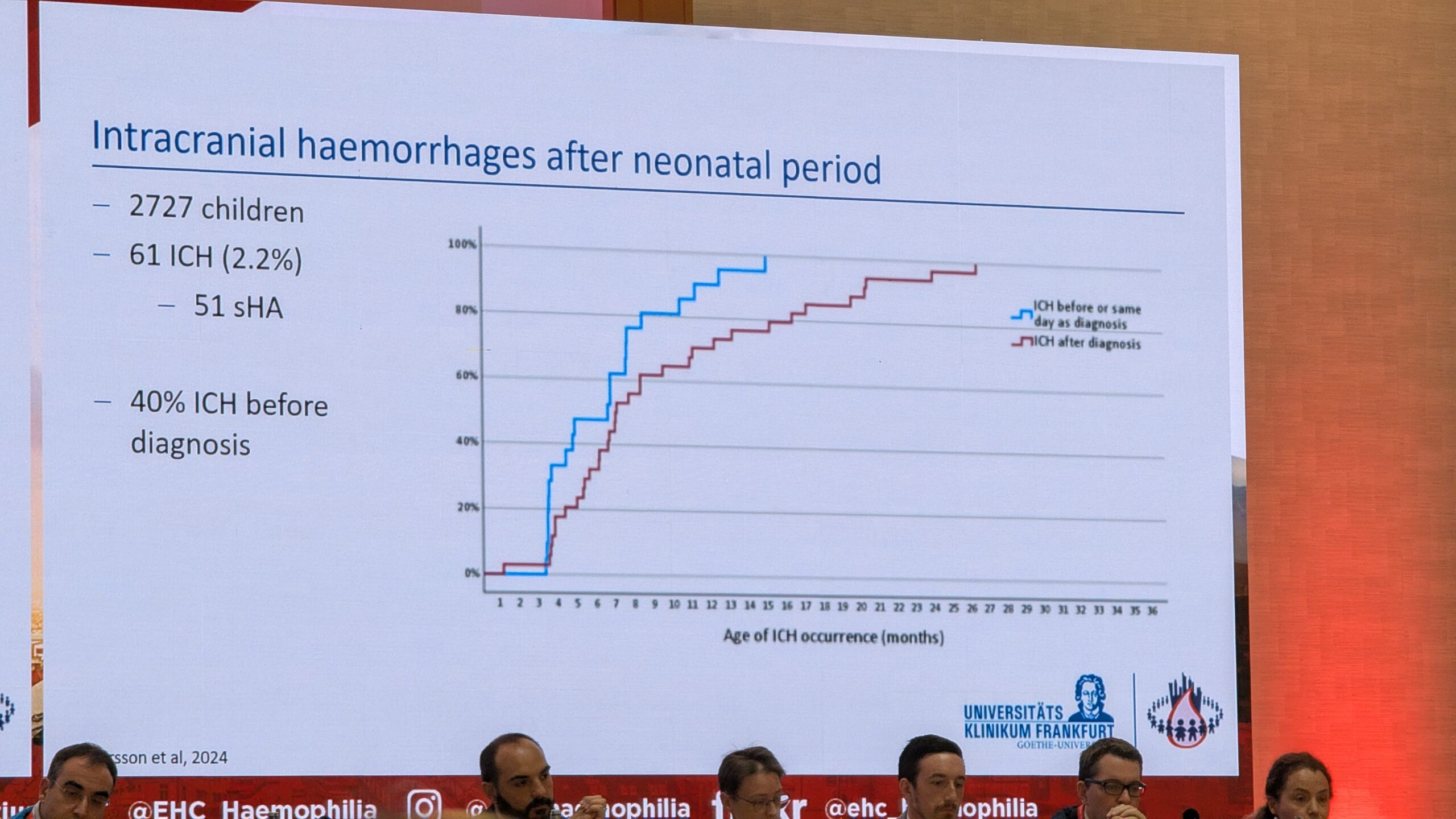
Vaatamata sellele, et enamik varem ravimata patsientide (PUP) verejookse on juba aset leidnud 12. elukuuks, alustatakse profülaktikat tihti alles selles vanuses. Königs sõnul on eesmärk alustada nii vara kui võimalik, et vältida just neid varaseid verejookse. Profülaktika peab olema:
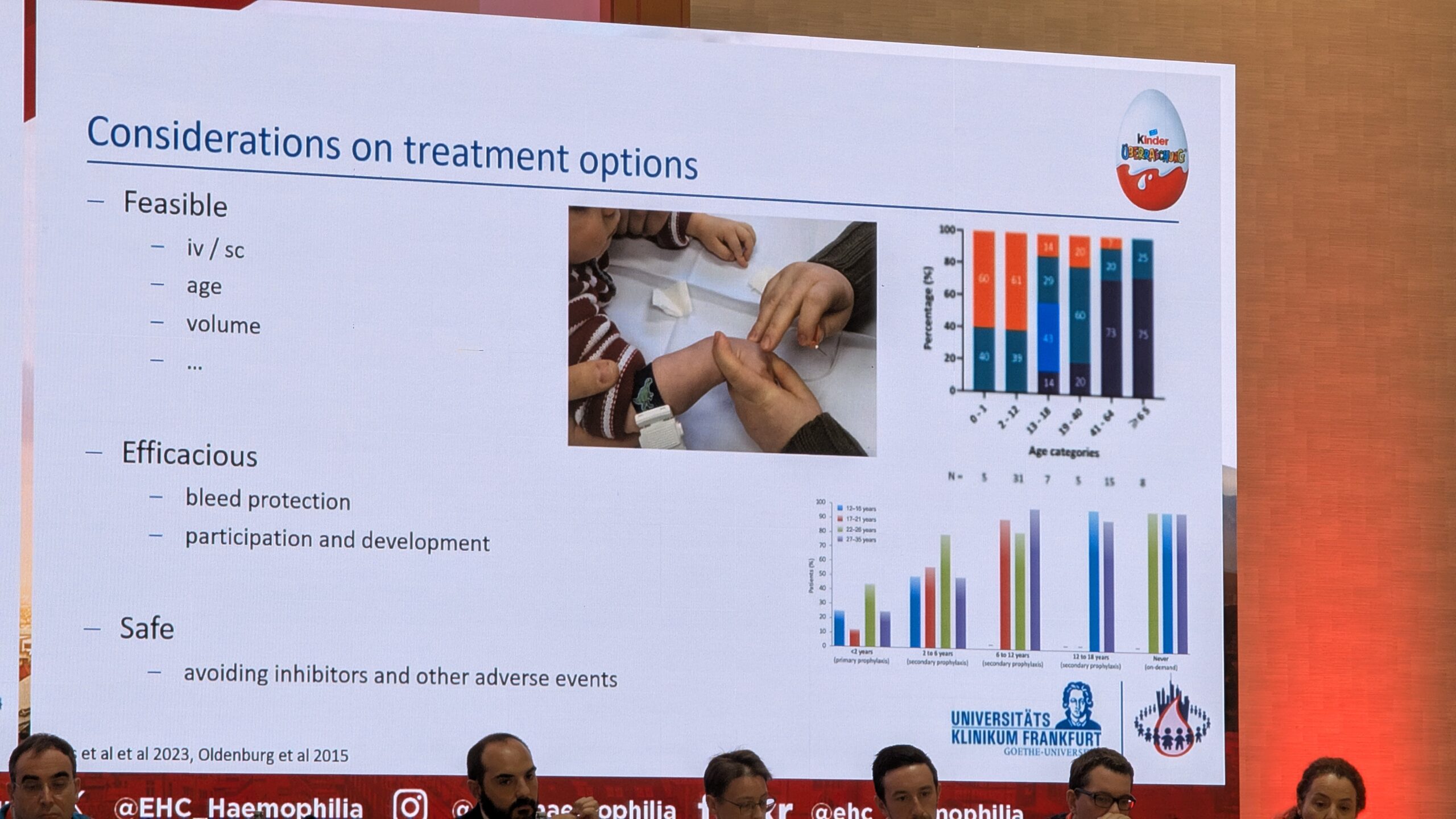
- Teostatav: arvestama vanust, manustamis mahtu ja pere olukorda (nt kas õde saab süstida).
- Efektiivne: peab olema hea ja aitama lapsel ohutult osaleda arengutegevustes, vältida kõrvaltoimeid ja inhibiitorite teket.
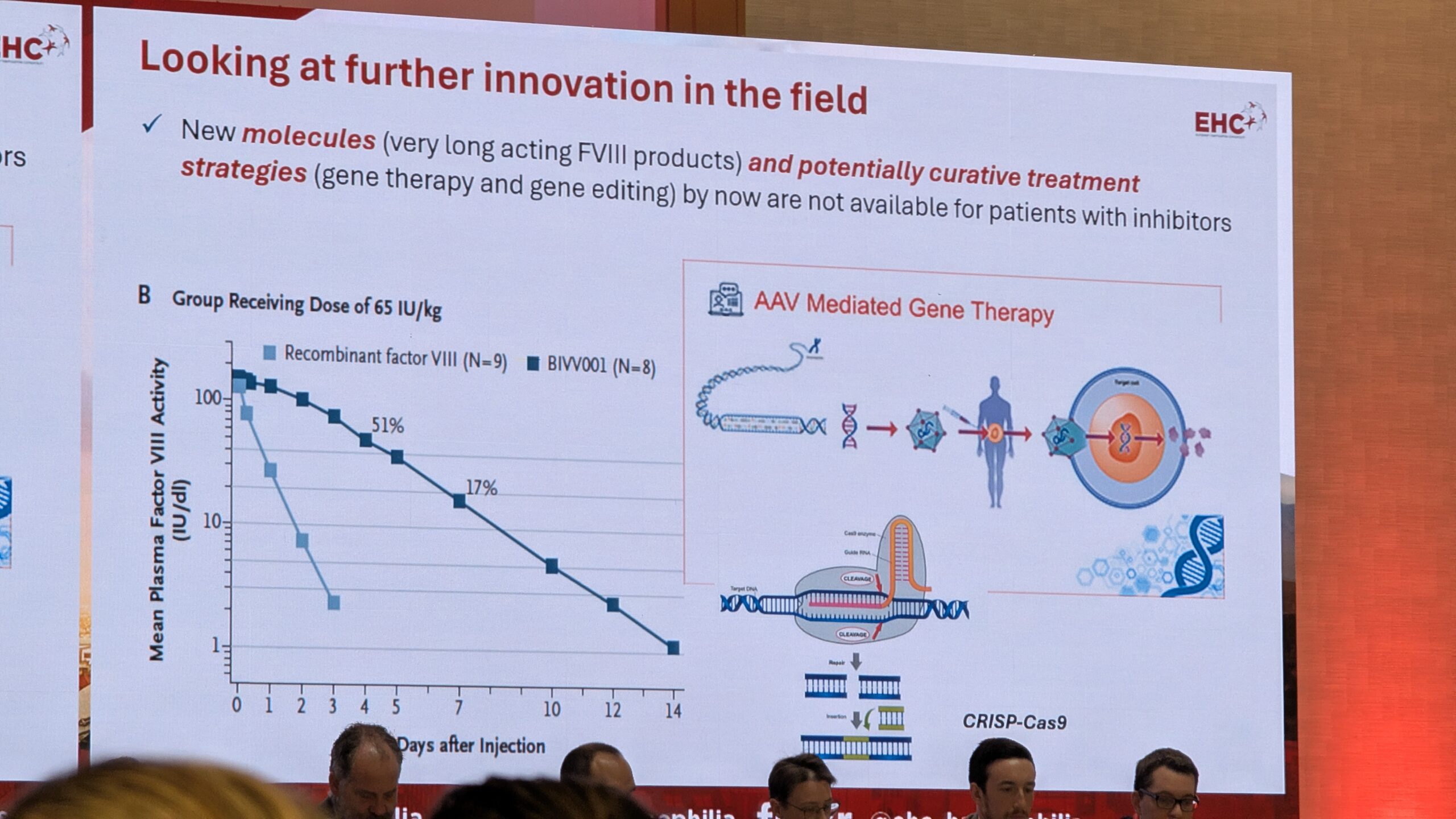
Arvestades tänapäevaseid ravivõimalusi (nagu näiteks pika poolväärtusajaga tooted ja Emitsizumab), on patsientidel palju erinevaid valikuid, kuigi mõned uued ravimeetodid (nt mitte-asendusravi) pole PUP-idele hetkel veel kättesaadavad.
7.3 Geeniteraapia: reaalse maailma kogemused EL-i patsienditeekonnalt – Dario Di Minno
Dario Di Minno jagas ülevaate Euroopa Liidu patsientide geeniteraapia reaalsest kogemusest, rõhutades, et patsientide psühholoogiline ettevalmistus on sama oluline kui kliiniline protseduur.
Patsiendi teekond ja ootused
Geeniteraapia teekond (patient journey) koosneb viiest etapist. Di Minno keskendus esimesele, sõelumise (screening) etapile, mis on kriitilise tähtsusega. Lisaks kliinilistele aspektidele (nt vanus, varasemate inhibiitorite puudumine) on esmatähtis psühholoogiline keel, sealhulgas patsiendi hirmud, ootused ja motivatsioon.
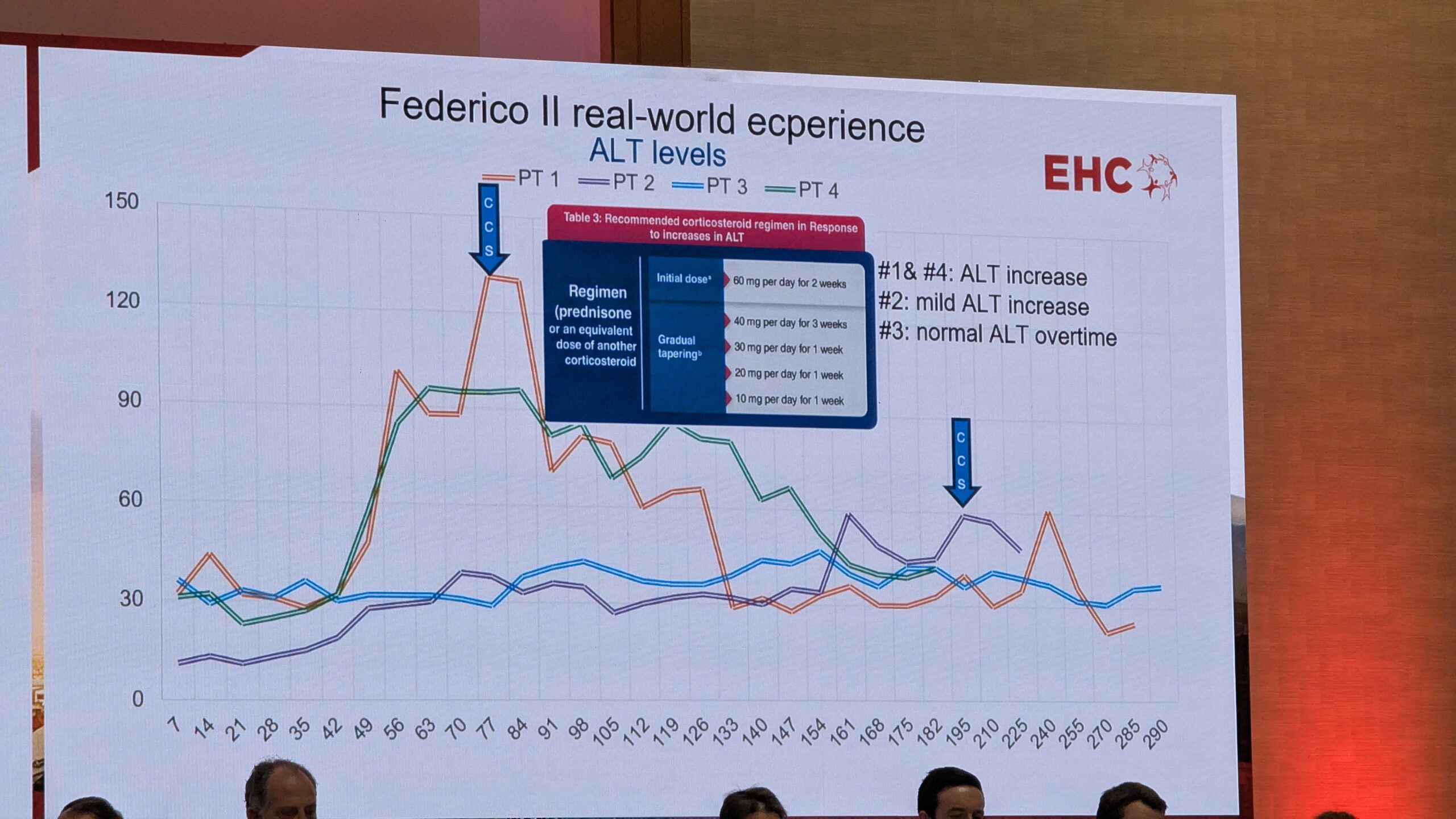
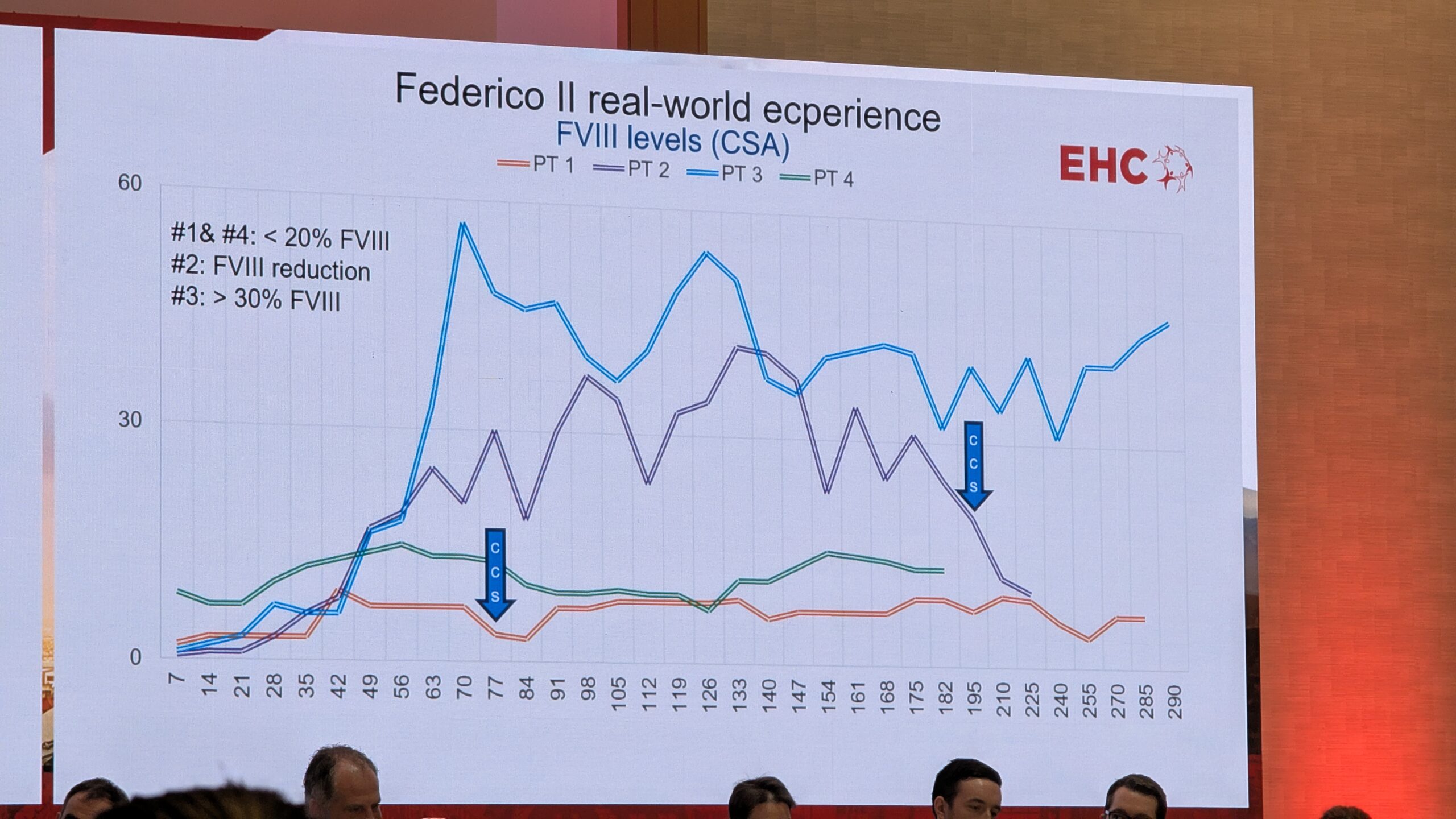
Patsientide peamine ootus geeniteraapialt oli vabadus verejooksudest ja vabadus profülaktikast. Samal ajal kardeti pikaajalisi muresid, nagu püsiva efekti kadumine (missing effect), maksafunktsiooni halvenemine (increase in ALT) ja pahaloomulised kasvajad (malignancy).
Kliiniline kogemus ja mured
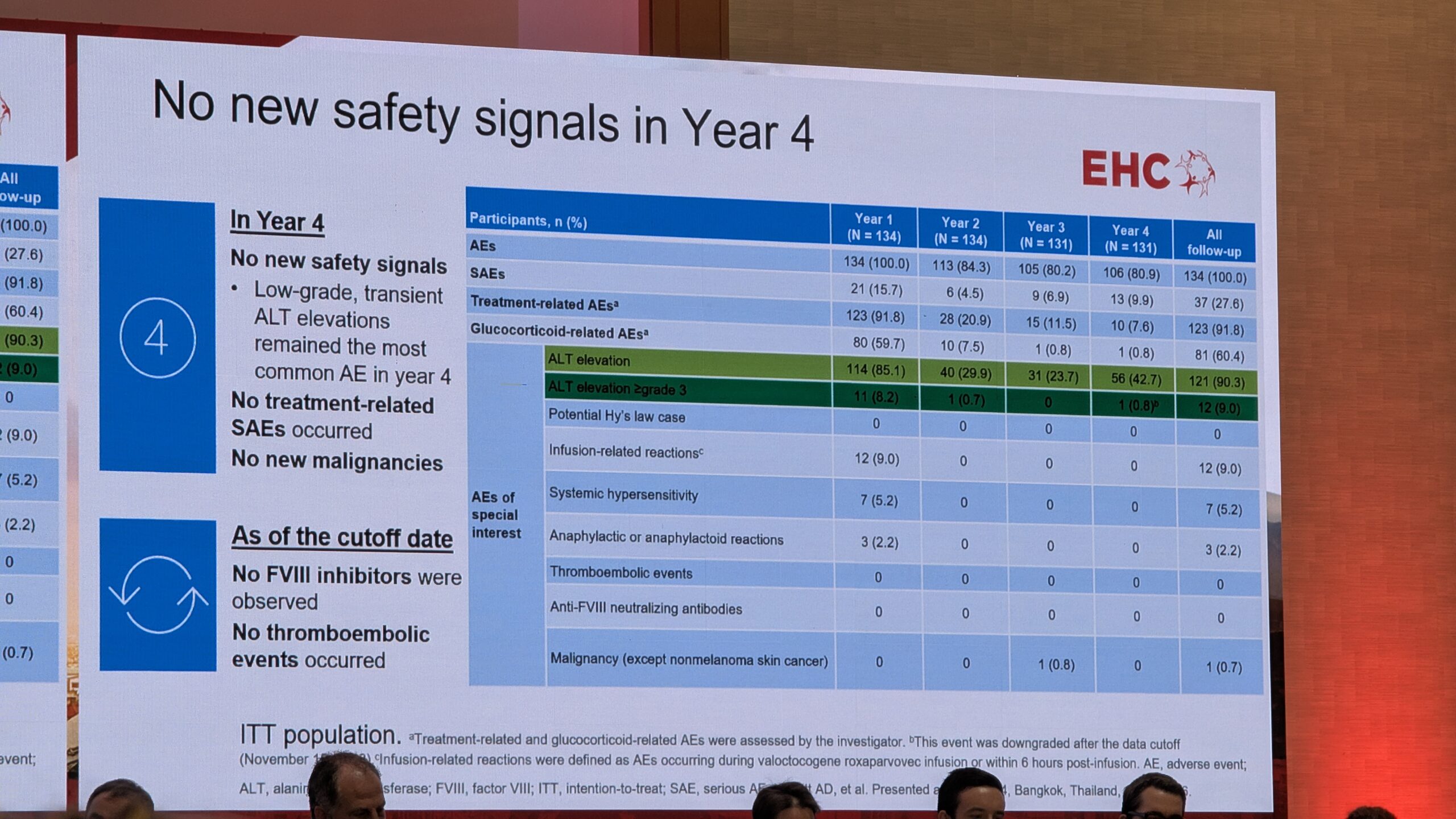
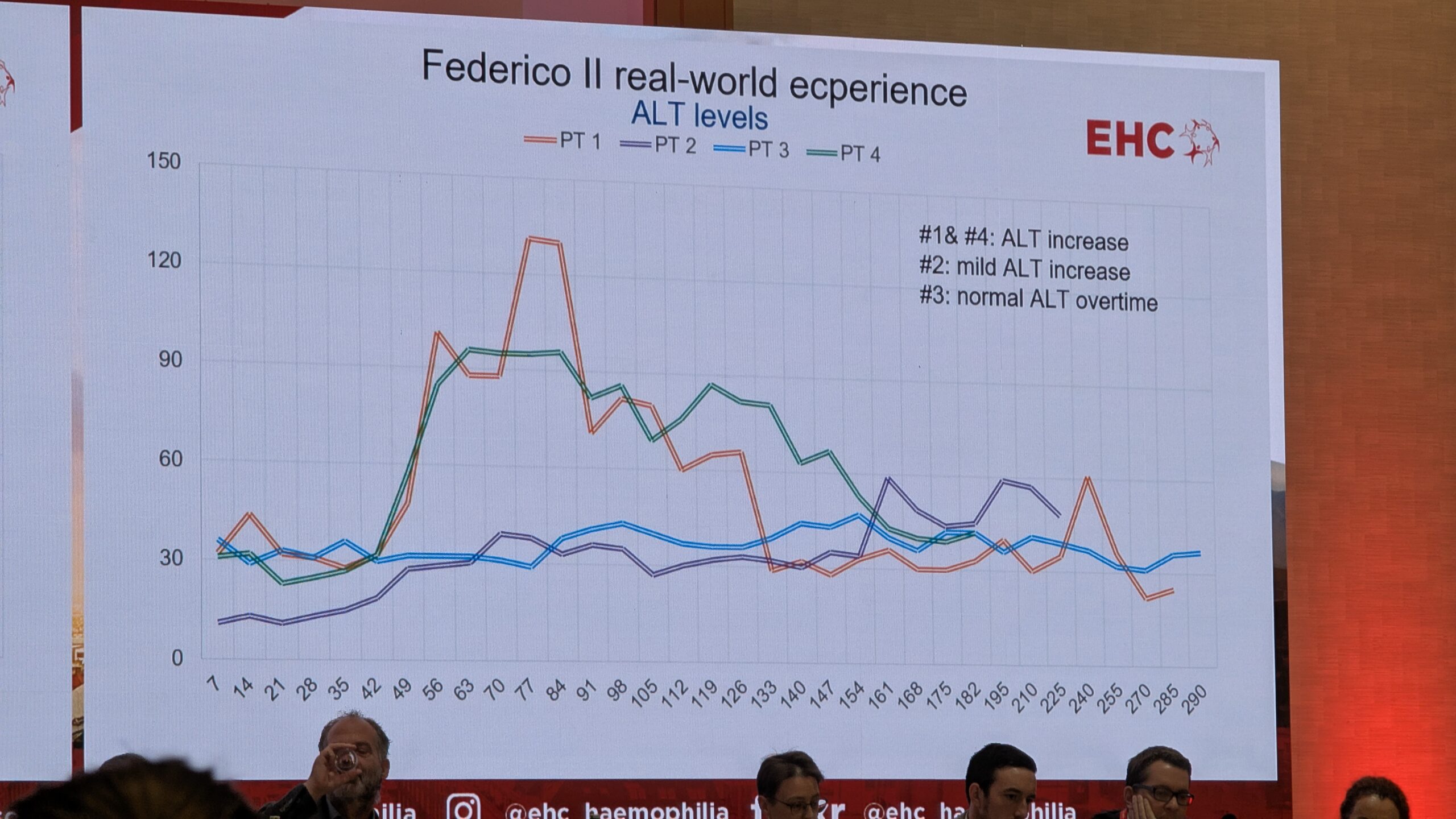
Kliiniliselt on geeniteraapia kõige keerulisem osa rangelt jälgitav jälgimisperiood (strict follow-up), mis on eriti intensiivne esimese kuue kuu jooksul (nädalased vere- ja kliinilised kontrollid). Kõige sagedamini teatatud kõrvaltoime oli ALAT (maksatestid) taseme tõus. Umbes 10% juhtudest esines 3. astme ALAT taseme tõusu, mille puhul kasutati kortikosteroide.
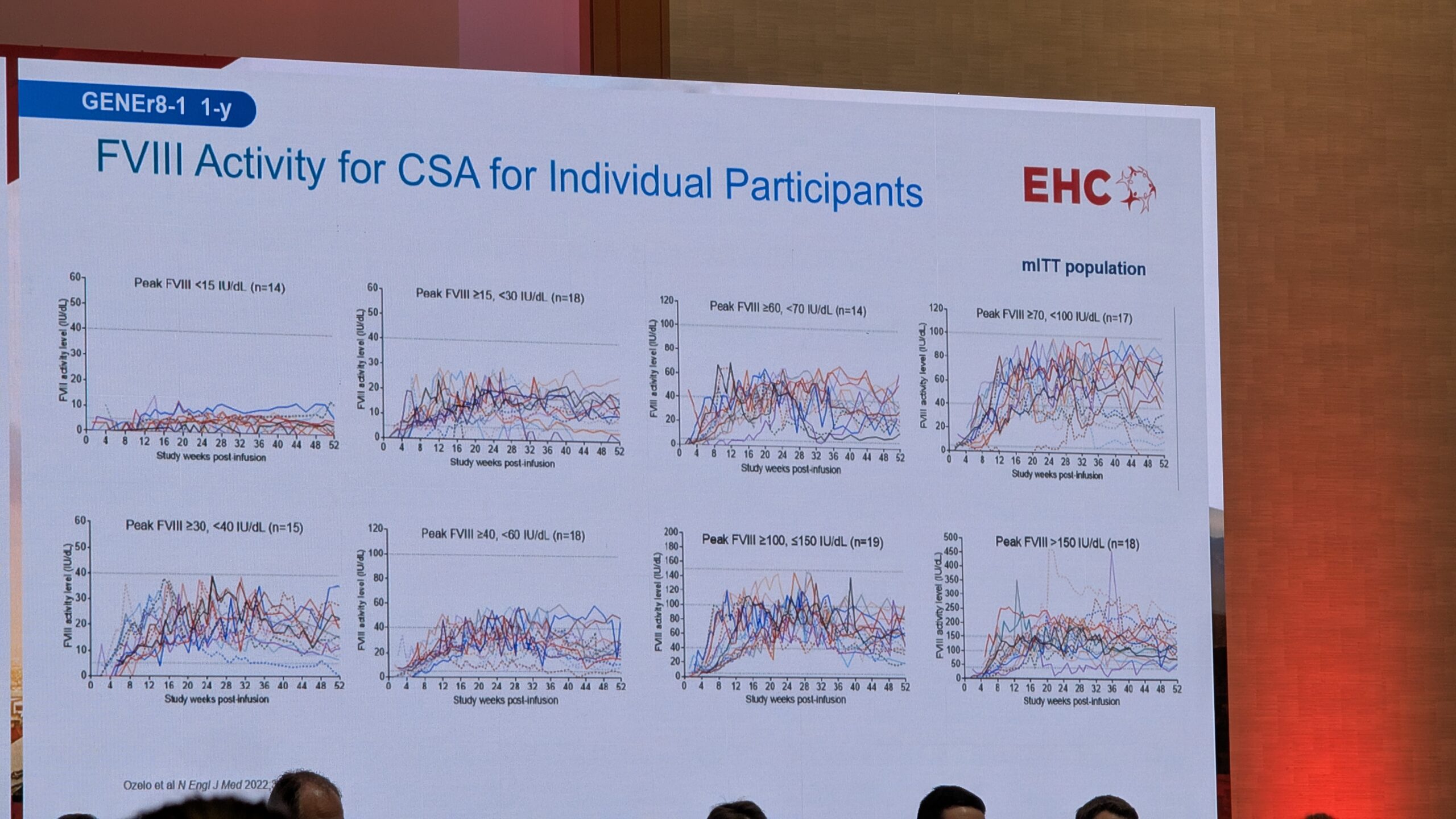
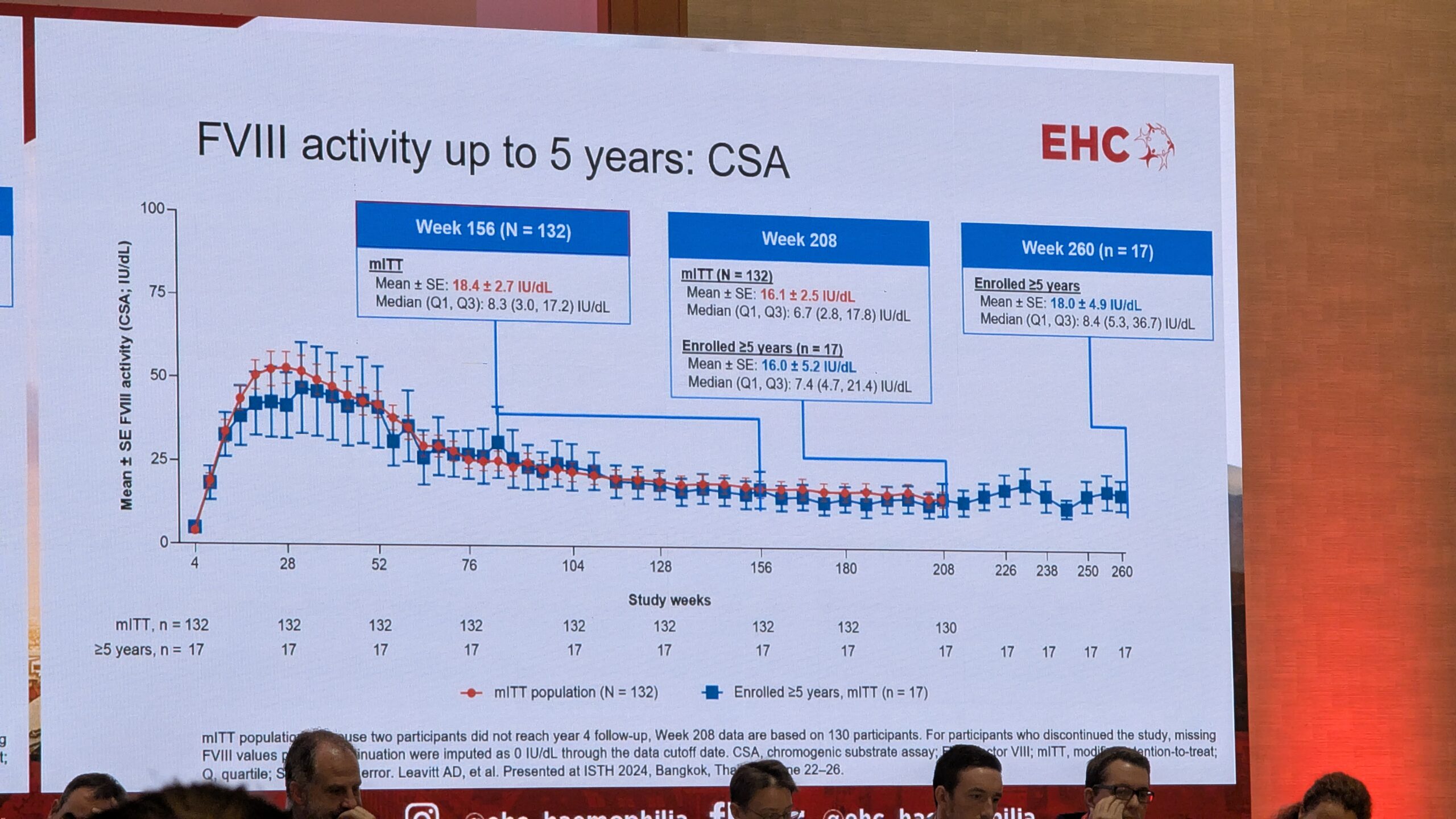
Faktori VIII ekspressiooni osas täheldati alguses langust (decay), mis oli ootuspärane. Kõige olulisem oli aga stabiilne ja püsiv ekspressioon aja jooksul. Hetkel on maksimaalne jälgimisaeg seitsme aastani ulatuv, kuid eeldused on ekspressiooni stabiilsuseks kahe aasta jooksul. Üks patsient, keda Di Minno näitas, oli pärast geeniteraapiat saanud mitu traumat, sh autoõnnetuse, ja vajas vaid ühel korral faktori infusiooni, rõhutades, et enamikel juhtudel on patsiendid pärast ravi lõpetanud profülaktika ja ei ole vajanud täiendavaid faktori infusioone. See on üks geeniteraapia kõige olulisemaid tulemusi.
7.4 Valu leevendamine verejooksu häirete korral – Nathalie Roussel
Nathalie Roussel keskendus valuravi väljakutsetele, purustades levinud väärarusaamu hemofiiliaga inimeste valu hindamise kohta.
Valed arusaamad valu osas
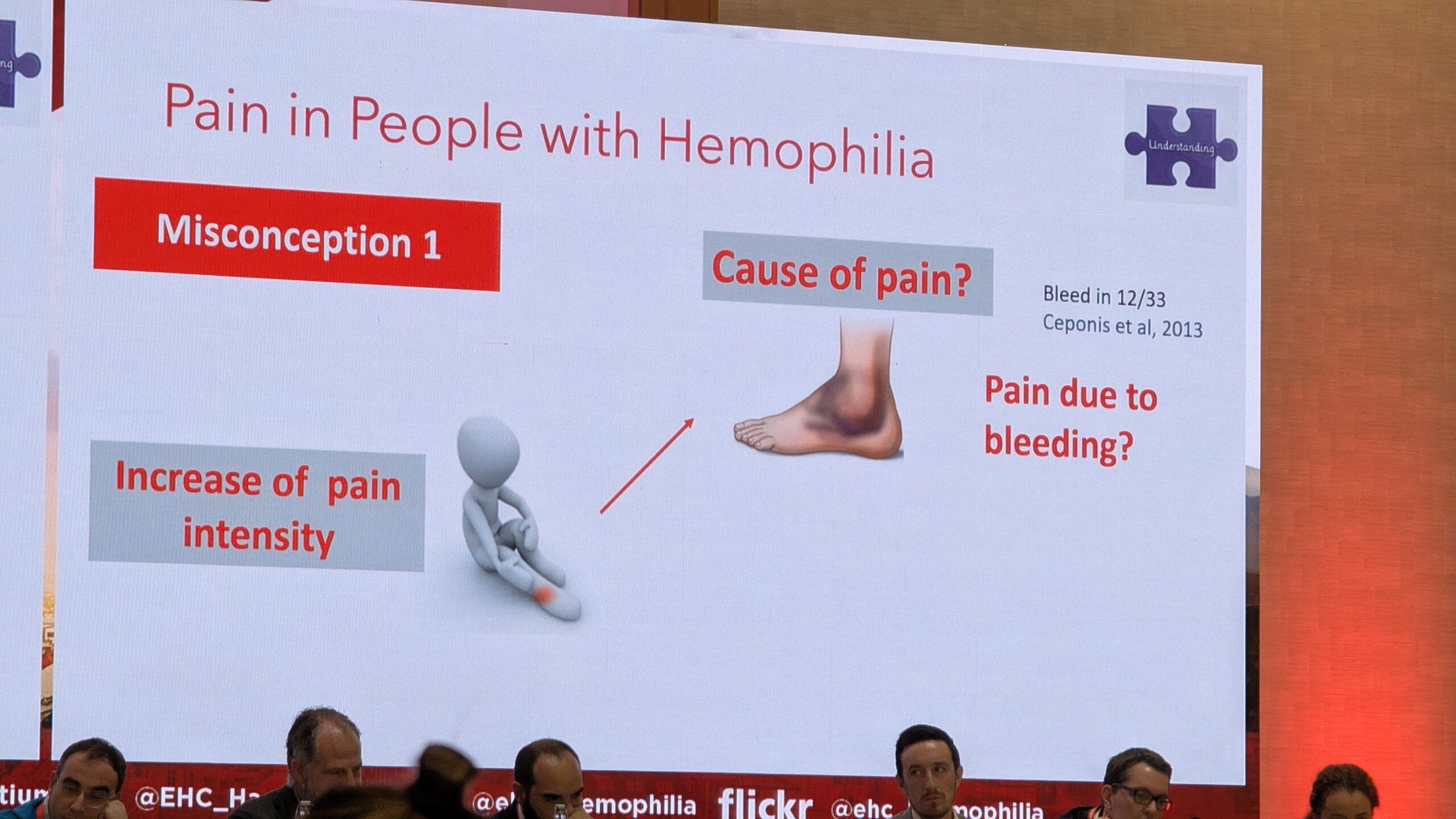
Roussel tõi esile kaks peamist väärarusaama:
- Äkiline valu intensiivsuse tõus on täpne näitaja akuutsest verejooksust (bleed). Uuringud näitavad, et vaid kolmandikku kahtlustatavatest verejooksudest kinnitati verejooksudena. Valu intensiivsus kõigub ka kroonilise liigesehaiguse korral iga päev.
- Valu seletub täielikult struktuursete liigesekahjustustega. Uuringud rohkem kui 100 patsiendiga näitasid, et liigesekahjustuse (liigese seisundi skoori, nt Hemophilia Joint Health Score – HJHS) ja valu intensiivsuse vahel puudus oluline korrelatsioon.
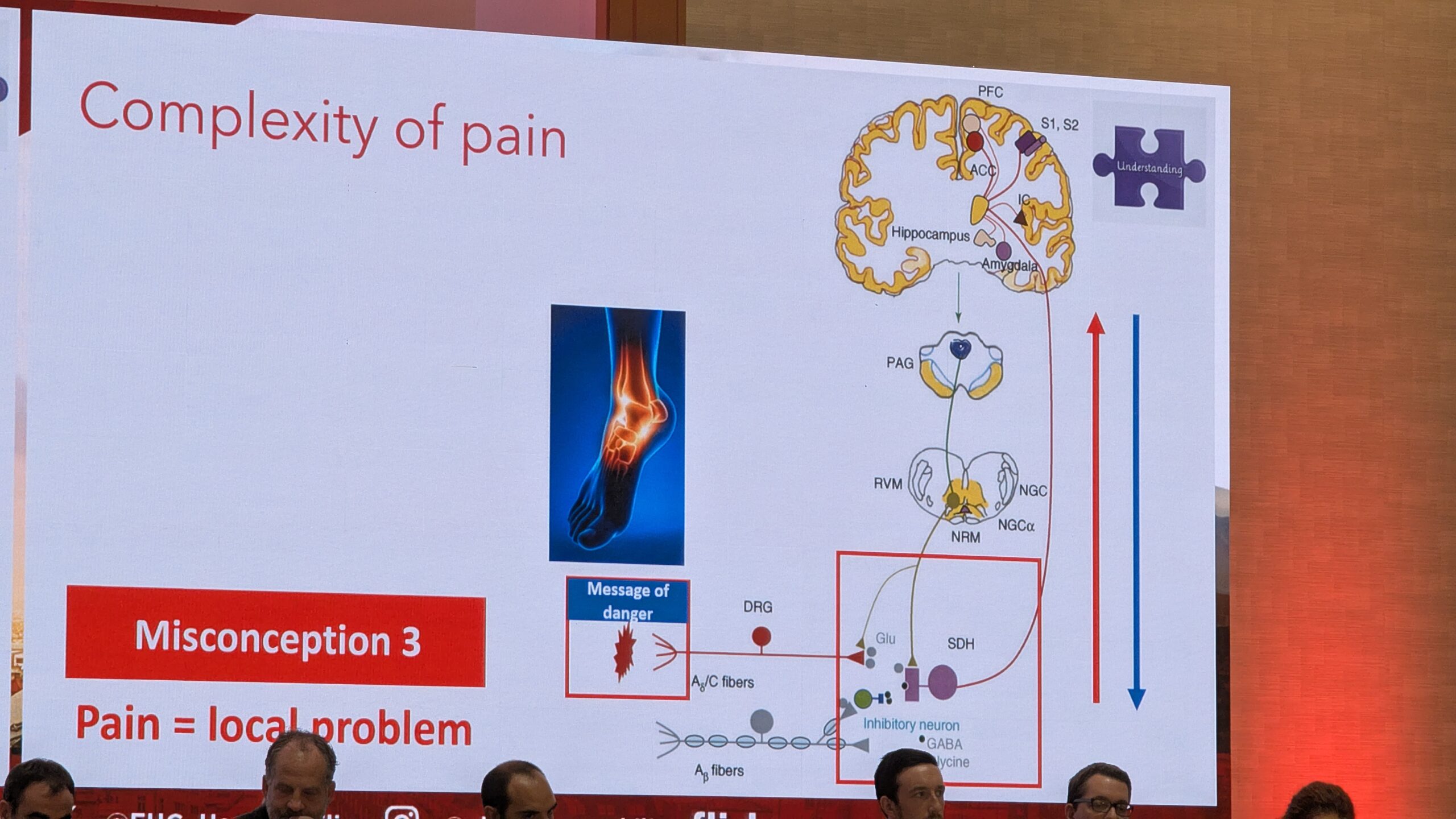
Valu on keskne probleem
Kuna valu ei ole ainult lokaalne probleem, vaid seda interpreteerib aju (stimulus läheb ajju ja aju tõlgendab seda), on kroonilise valu puhul tegemist keskse närvisüsteemi düsfunktsiooniga, eriti valu kontrolli süsteemis. See düsfunktsioon on sarnane teiste krooniliste valuhäiretega (nt alaseljavalu, kaelavalu, põlve artroos) ja seda on võimalik muuta.
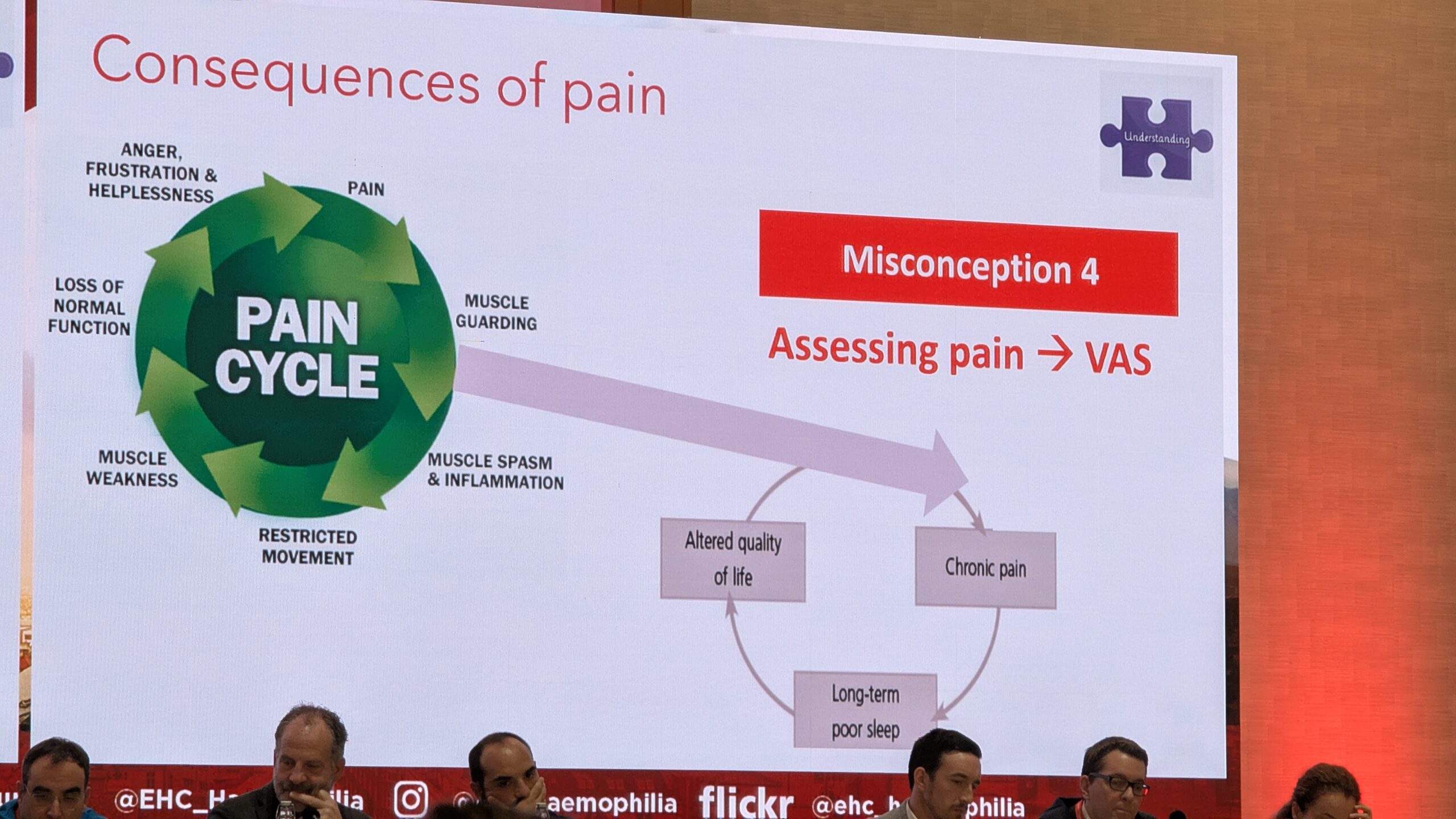
Biopsühhosotsiaalne hindamine ja ravi
Valu ei saa hinnata ainult visuaalse analoogskaalaga (VAS), mis on ainult “kiirfoto ühest hetkest”. Valuravi vajab laia biopsühhosotsiaalset hindamist. See hõlmab bioloogilisi tegureid (liigese seisund, ligipääs ravile), psühholoogilisi tegureid (hirm verejooksude ees, stress) ja sotsiaalseid tegureid. Kuna valu on multifaktoriaalne, peab ka ravijuhtimine olema multimodaalne.
Roussel, olles füsioterapeut, rõhutas füüsilise tegevuse ja harjutuste olulisust. Harjutused ei paranda ainult funktsiooni, vaid aktiveerivad ka aju poolt juhitavat allapoole suunduvat valu kontrolli süsteemi. Valuravi on meeskonnatöö, mis nõuab multidistsiplinaarset lähenemist. Oluline on usaldus patsiendi ja tervishoiutöötaja vahel.
7.5 Vananev aju hemofiilia korral – William McKeown
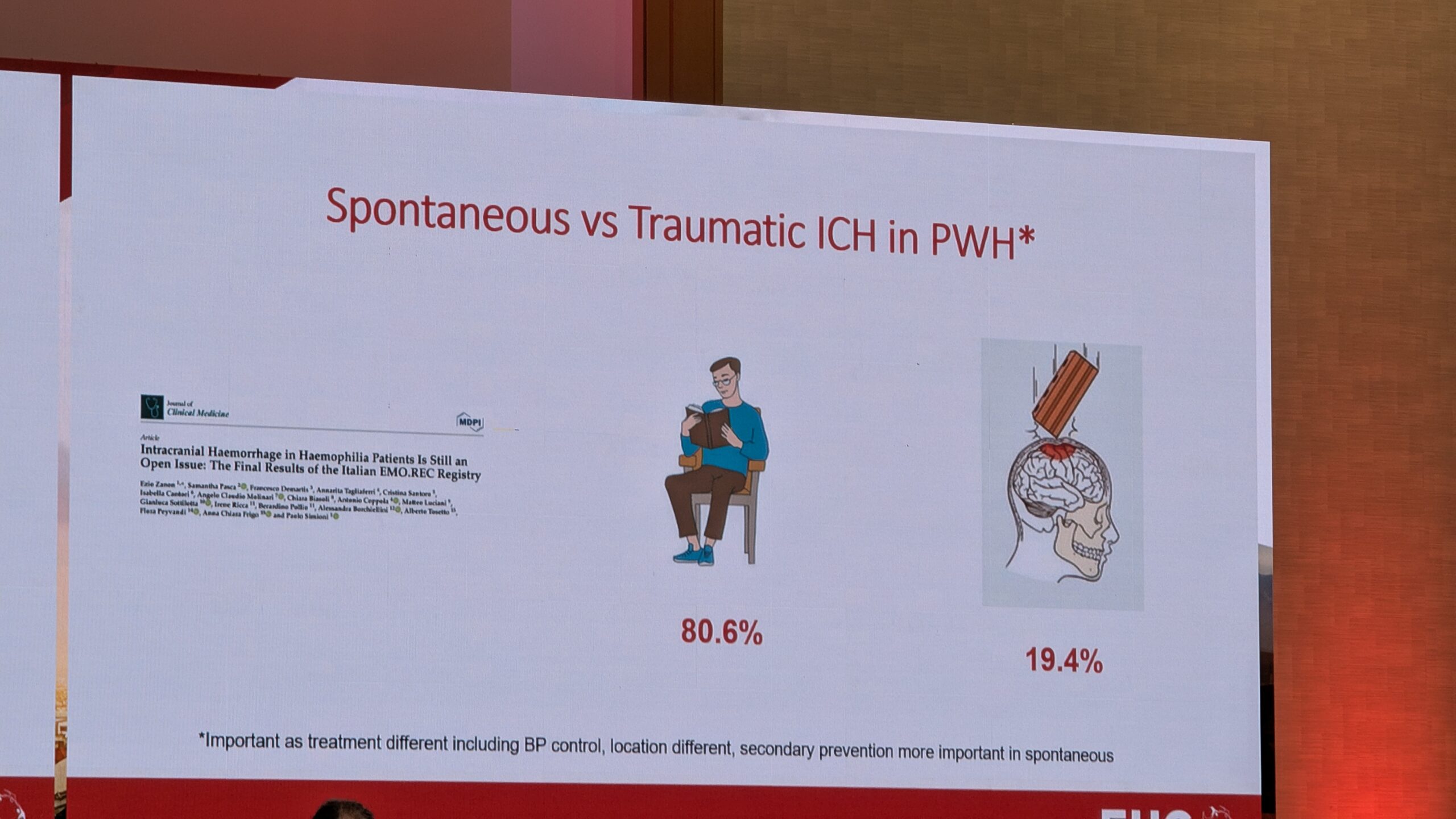
William McKeown, kes on nii raske hemofiilia A patsient kui ka insuldi konsultant, käsitles vananeva aju teemat, keskendudes intrakraniaalsele hemorraagiale (ICH, ajuverejooks).
ICH kui kõige surmav amplikatsioon
ICH on hemofiilia kõige surmav komplikatsioon. See on oluline teema, mida tuleb pidevalt käsitleda. ICH esineb nii spontaanselt (ilma traumata) kui ka trauma tagajärjel. Hemofiilia puhul on valdav enamus ajuverejooksudest spontaansed. ICH mõjutab nii noori patsiente (imikud) kui ka vanemaid hemofiiliaga inimesi.
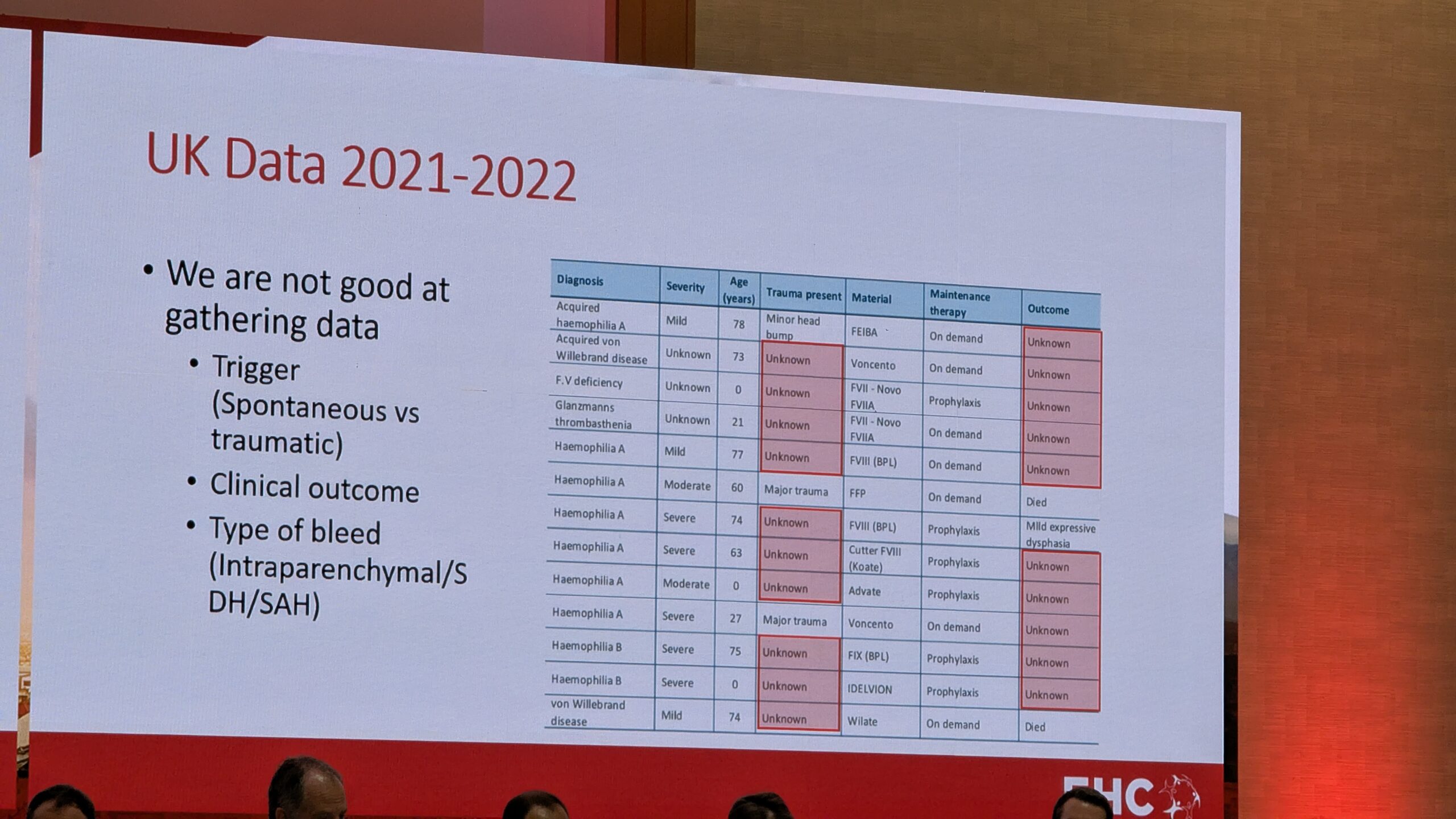
Statistika ja riskifaktorid
ICH on jätkuvalt tõsine probleem. Ühendkuningriigi andmed näitasid, et ICH vastutas 10% surmajuhtumite eest hemofiiliaga inimeste hulgas (kõrgem määr kui üldpopulatsioonis). McKeown rõhutas, et andmete kogumine on puudulik. Näiteks riiklikud registrid ei kogu alati infot selle kohta, kas ICH oli traumaatiline või spontaanne.
Hemofiilia riskifaktorite hulka kuuluvad loomulikult madal faktori tase. Üldpopulatsioonis on peamine riskifaktor kõrge vererõhk (hüpertensioon), mis on hemofiilia populatsioonis sagedasem. McKeown hoiatas rahulolu eest: kuigi varem arvati, et hemofiiliaga inimestel on südame-veresoonkonna probleemid harvemad (veritsuse kalduvuse tõttu), ei ole see tegelikult nii ja riskifaktoreid tuleb aktiivselt hallata.
Mikroveritsused ajudes
McKeown mainis ka mikroverejookse, mis on väikesed tumedad täpid aju MRI-uuringul. Need mikroverejooksud on hemofiiliaga patsientidel sagedasemad. Kuna üldpopulatsioonis on kroonilise ICH-ga inimestel suurem dementsuse oht, on see teema, mida tuleks hemofiilia kontekstis põhjalikumalt uurida.
Lõpetuseks nentis ta, et kuigi raske hemofiilia ravi on väga hea, on kerge ja mõõduka hemofiiliaga inimeste ravi osas tehtud vähem edusamme.
7.6 Miks me oma haavu lakume? – Johannes Thaler
Johannes Thaler käsitles küsimust, miks inimesed refleksist haava lakkavad.
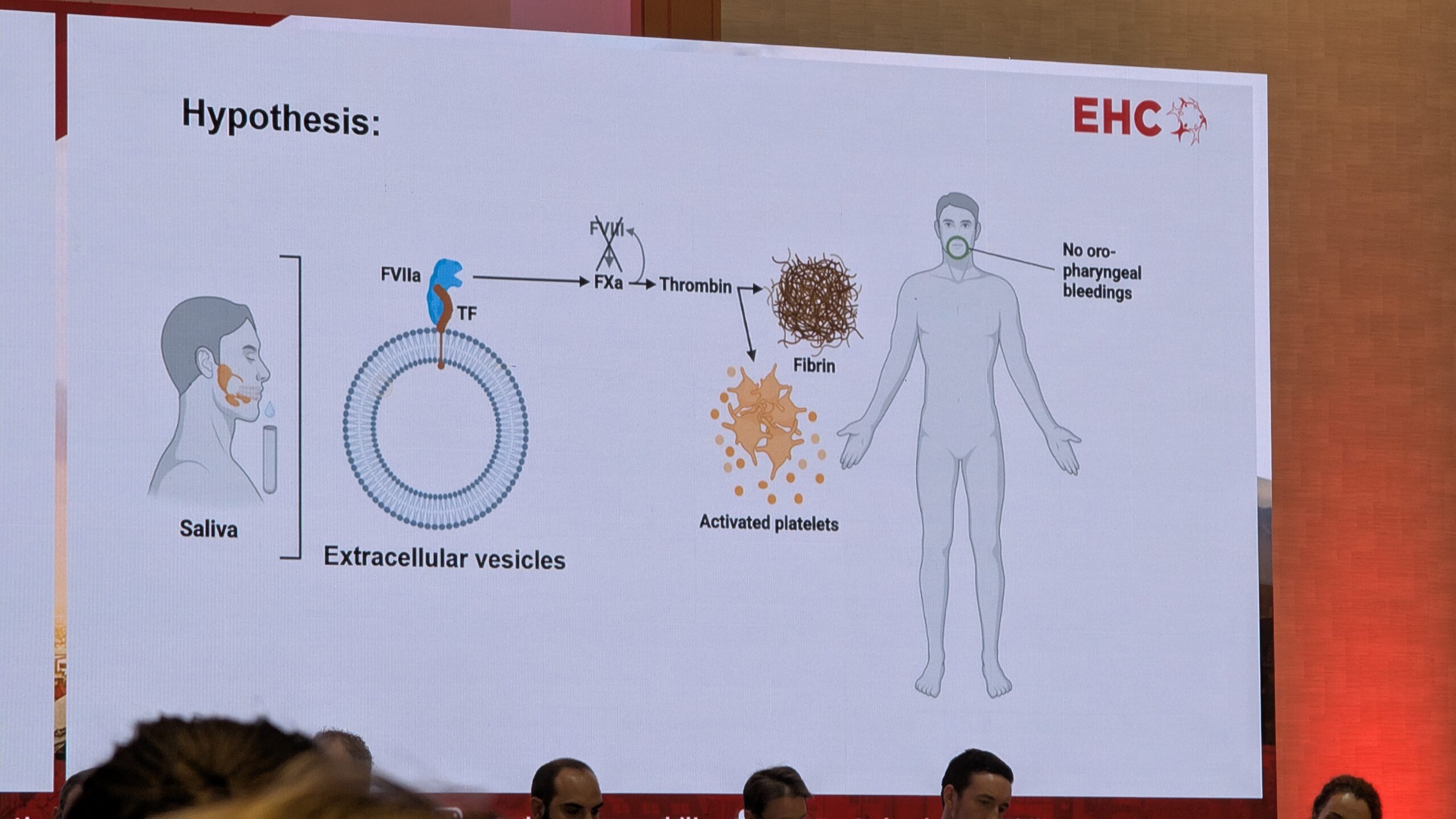
Sülg ja hüübimisfaktorid
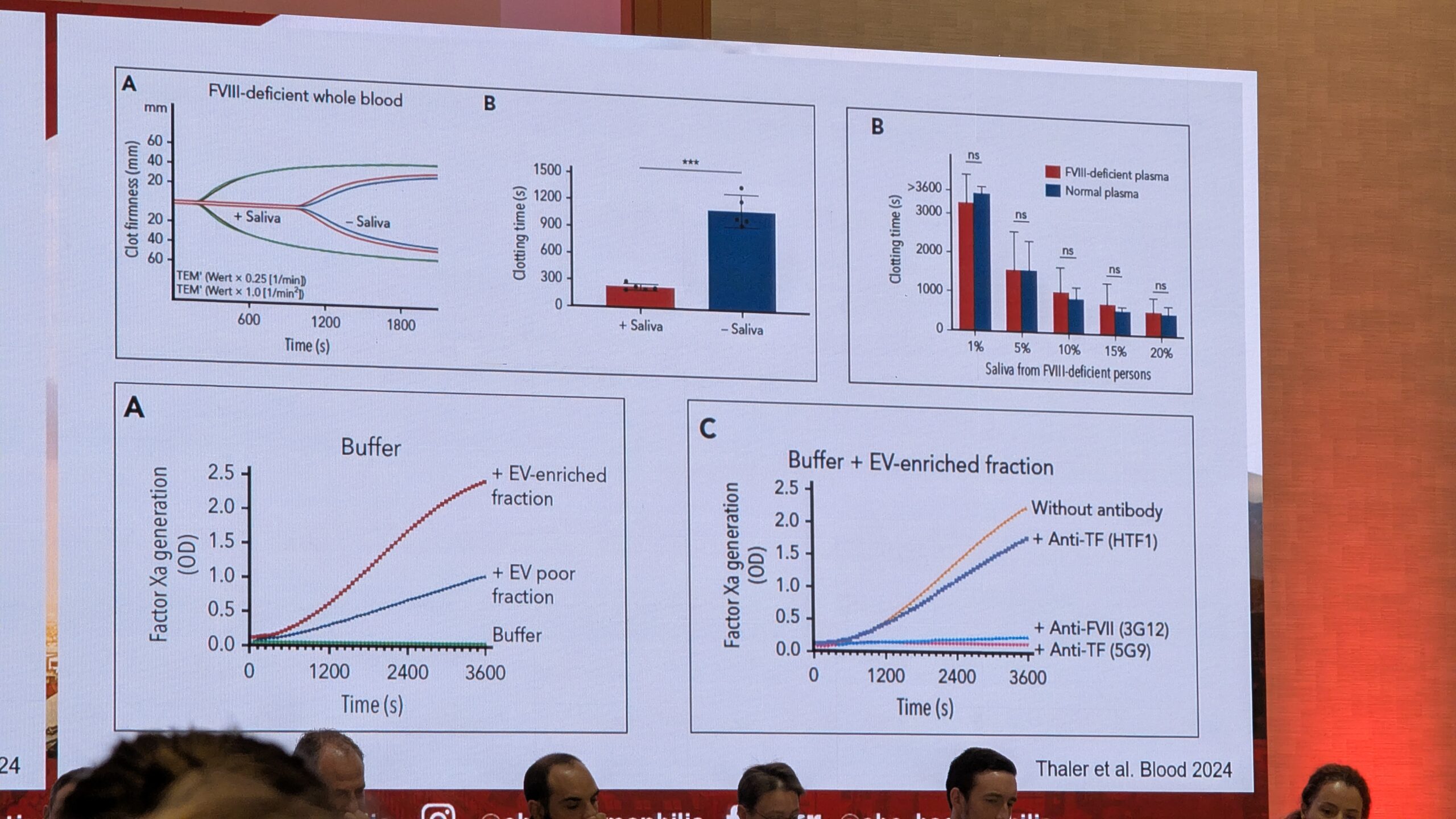
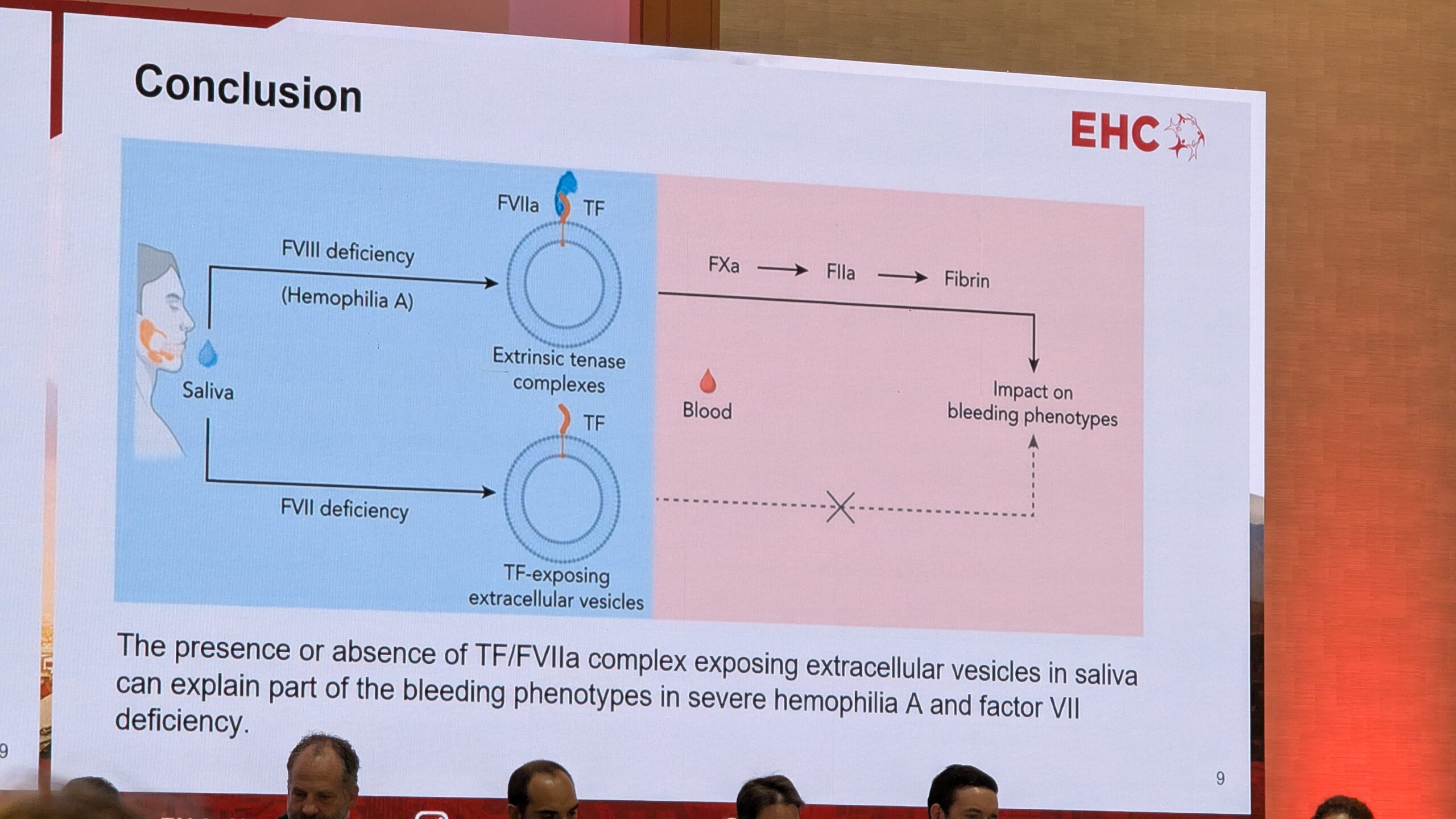
Loomulik refleks on viia verejooksu koht suhu ja lakkuda seda keelega. Seejärel seguneb sülg verega. Thaler selgitas, et sülg seguneb verega ja selles sisalduvad ekstratsellulaarsed vesiikulid eksponeerivad koefaktorit. See indutseerib hüübimiskaskaadi ja soodustab hüübimist.
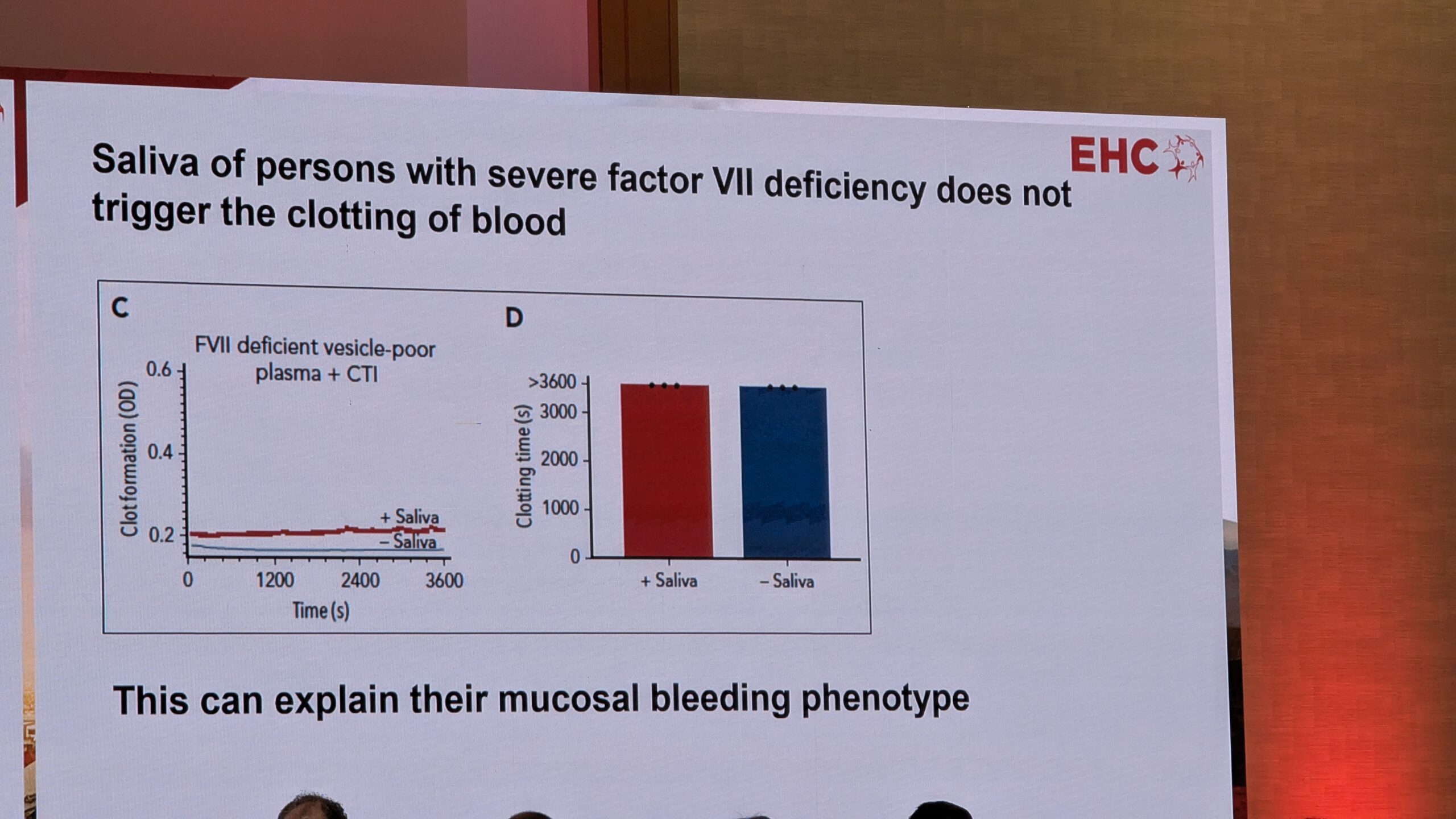
Thaler mainis, et uuringud on näidanud sarnast potentsiaalset mehhanismi ka patsientidel, kellel on faktori VII puudulikkus. Uurides sülge patsientidel, kellel on faktori VII puudulikkus, leiti, et sülg ei suutnud hüübimist esile kutsuda. See võib seletada patsientide verejooksu fenotüübi erinevusi. Thaler järeldas, et sülje hemostaatiline potentsiaal võib seletada hemofiilia A ja muude kergete verejooksuhäiretega patsientide verejooksu fenotüüpe, samuti seda, miks faktori VII puudulikkusega inimestel need verejooksud on sagedased.
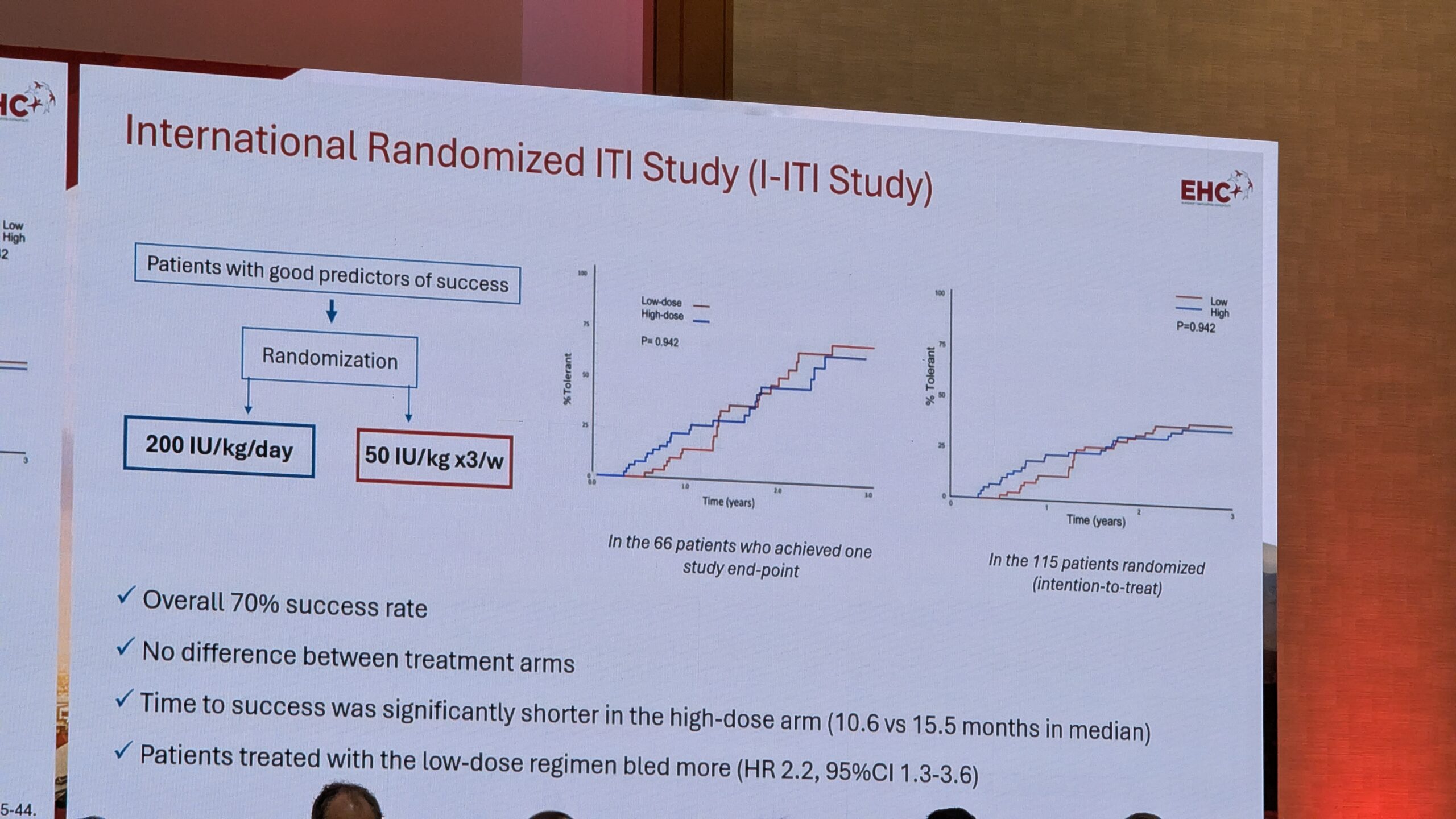
7.7 ITI emitsizumabiga ravitud patsientidel – Maria Elisa Mancuso
Maria Elisa Mancuso käsitles immuuntaluvusravi (Immune Tolerance Induction, ITI) hemofiilia patsientidel, keda ravitakse emitsizumabiga. ITI on ainus ravistrateegia inhibiitorite likvideerimiseks.
ITI ja Emitsizumab: dilemma
Varem oli ITI ainus eesmärk taastada tundlikkus faktor VIII-le. Nüüd on meil aga emitsizumab (mitte-faktorasendusravi), mis on efektiivne profülaktika inhibiitoritega patsientidel, ja see tekitab olulise küsimuse: miks peaksime tegema ITI-d emitsizumabi lisaks? ITI on kallis (miljoneid eurosid) ja võib kesta kaua (kuni kolm aastat).
Põhjused ITI jätkamiseks
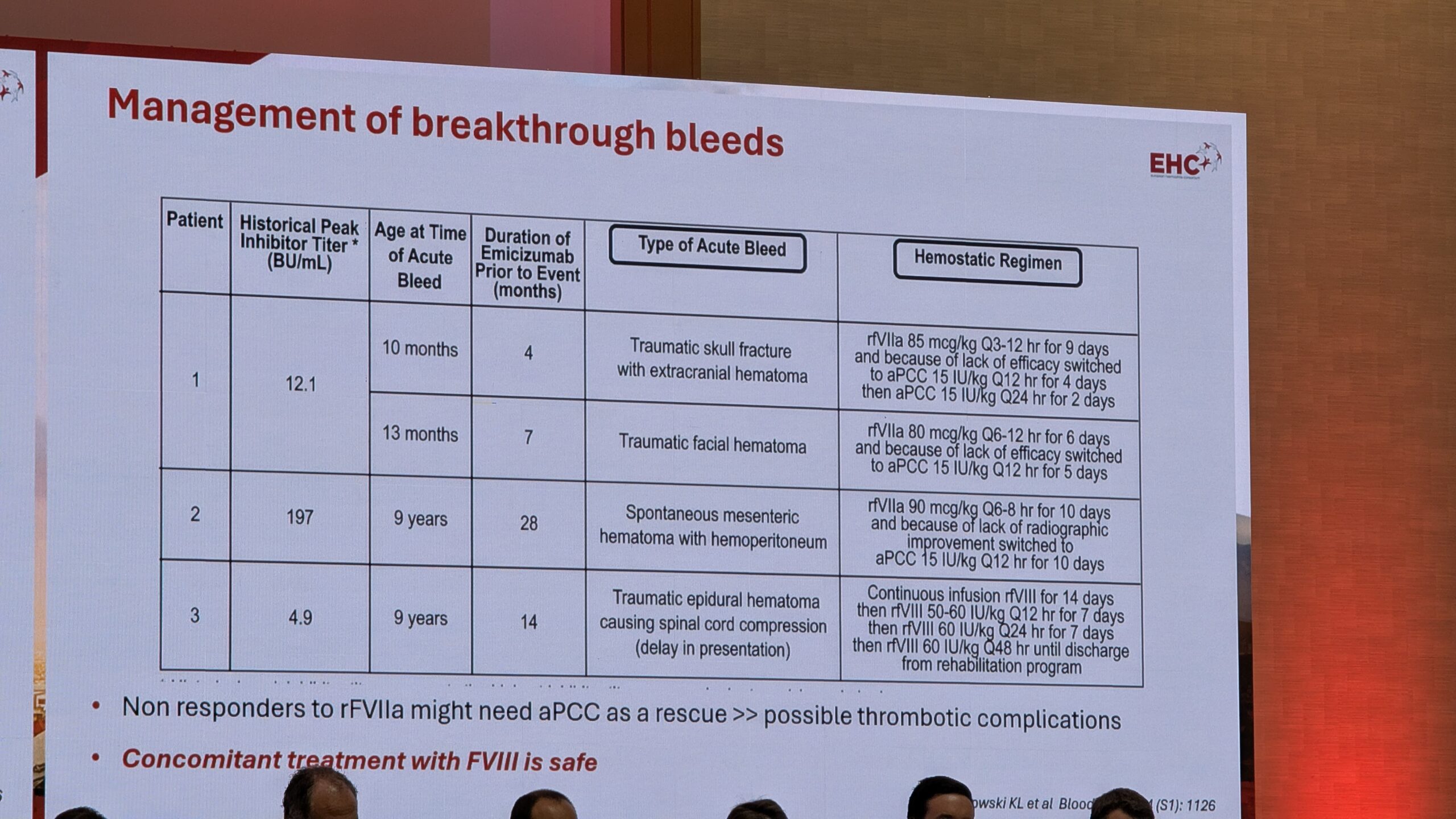
Mancuso tõi välja mitu põhjust, miks ITI on endiselt vajalik:
- Riskijuhtimine: Emitsizumabiga ravitud patsiendid võivad endiselt veritseda. Hädajuhtumite puhul on faktori VIII kontsentraat turvalisem kui möödaviivad ained, nagu näiteks FEIBA.
- Krooniliste tüsistuste vältimine: Inhibiitoritega elamine toob kaasa rohkem tüsistusi, nagu artropaatia (liigesehaigus) ja elukvaliteedi halvenemine.
- Juurdepääs tuleviku ravile: Patsiendid, kellel on aktiivsed inhibiitorid, ei saa praegu kasu uutest ravimeetoditest, näiteks geeniteraapiast.
ITI režiimid emitsizumabi kasutamisel
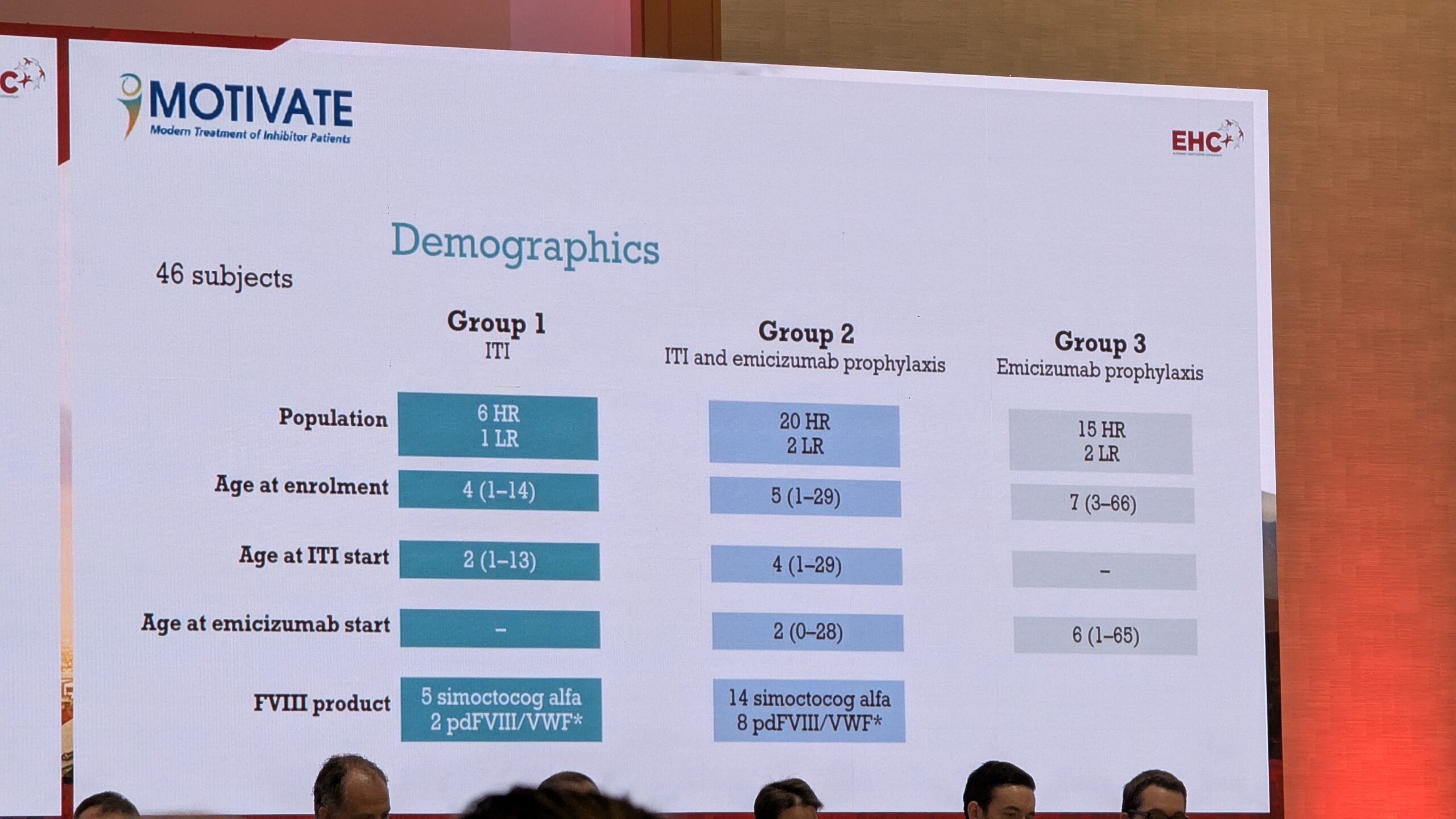
Mancuso tutvustas uuringuid, mis võrdlesid ITI-d üksi (tavaliselt kõrge annus) ja ITI-d koos emitsizumabiga. Leiti, et emitsizumabiga ravitud patsientide rühm kasutas ITI puhul sagedamini madalamat annust. Kuigi emitsizumabiga rühmal võttis inhibiitori likvideerimine kauem aega, olid nad siiski kaitstud verejooksude eest. Samuti näitasid andmed, et ITI-d koos emitsizumabiga saanud patsientidel oli vähem verejookse ITI-perioodi jooksul.
Mancuso soovitas, et uute inhibiitoritega lastele tuleks ITI-d proovida vähemalt korra, välja arvatud juhul, kui lapsel on väga halvad ennustajad ITI-le reageerimiseks. See on kliinikute vastutus tagada parim tulevik.
Lõpetuseks rõhutas Mancuso, et vaatamata uutele põnevatele ravimeetoditele ei ole inhibiitoriga elamine sama hea kui ilma selleta elamine.
8. Tööstussümpoosion 3: „Hemostaasi (taas)tasakaalustamine, patsiendihoolduse tasakaalustamine: teaduse, hoolduse ja kogukonna ühendamine“
1. Hemofiilia Ravi Evolutsioon ja Uued Eesmärgid
Ravi varajane eesmärk (umbes 1950. ja 1960. aastatel) oli tagada patsientide ellujäämine ja vältida surma, ravides lõpuks ka verejookse, mida oli võimalik ravida. See oli ravi peamine toime. Edasi keskenduti verejooksu kontrollile, mis hõlmas profülaktikat ja ennetamist, mida võimaldasid plasmapõhised kontsentraadid ja hiljem rekombinantsed kontsentraadid.
Aastate jooksul on ravi järjest paranenud. Patsientidele pakuti lühema poolestusajaga kontsentraate ja hiljem pikema poolestusajaga ravimeid (mis on muutnud elukvaliteeti). Pika poolestusajaga ravimid võimaldasid faktorit manustada harvemini, näiteks iga kolme päeva tagant või kaks korda nädalas. Veelgi võimsam ja revolutsioonilisem on profülaktika uute taktikatega (nt nahaalused manustamisviisid), mis muudavad ravi patsientidele veelgi lihtsamaks.
Põhieesmärgiks on mugavus
Tänapäeval ei keskenduta enam ainult verejooksu probleemide ravimisele, vaid peamine edasiviiv jõud on mugavus. Ravi eesmärk on lisaks verejooksude vältimisele ka ravimite lihtne kättesaadavus (nt varude hoidmine kodus).
Ülim eesmärk, mida üha enam arutatakse, on hemofiilia-vaba meel. Kuigi see võib tunduda ambitsioonikas, püütakse seda saavutada, et patsiendid saaksid elada oma elu ilma pideva hirmuta haiguse ees, mis on pidevalt nende südametes. Seda eesmärki püütakse saavutada mitme strateegia abil, sealhulgas supreemsete uuringute ja tasakaalustavate ravimeetoditega.
2. Hemostaasi Taastasakaalustamine: Uus Raviprintsiip
Hemostaas on vere hüübimisprotsessis oluline, kuna veres on alati tasakaal hüübimist soodustavate (prokoagulandid) ja hüübimist takistavate (antikoagulandid) tegurite vahel. Mõlemat on vaja: esiteks, et vältida verejooksu ja teiseks, et vältida vere klompide teket ja surma. Hemofiilia puhul on see tasakaal paigast ära, kuna faktorit VIII või IX ei ole piisavalt.
Tasakaalustav ravi
Traditsiooniline ravi (asendusravi) on lisanud puuduva faktori tagasi süsteemi, taastades sellega tasakaalu. Uute tasakaalustavate ravimeetodite põhimõte on aga erinev: kui ühel kaalukausil on midagi puudu, võetakse vastaspoolelt (antikoagulatsioonilt) midagi ära, et leida uus tasakaal.
See saavutatakse, sihtides antikoagulantseid valke, näiteks TFPI-d (Tissue Factor Pathway Inhibitor). TFPI on valk, mis oma definitsiooni kohaselt takistab koefaktori toimeid, mis muidu soodustaks hüübimist. Kui TFPI välja võetakse (inhibitseeritakse), eemaldatakse pidur ja seega on võimalik taastada trombi teket ja hüübimist. See lähenemisviis, kus eemaldatakse antikoagulandid, on sarnane põhimõttele, et isikutel, kellel puudub TFPI, ei esine tõsiseid haigusi. See on teatud mõttes “pioneeri” lähenemine.
Sarnast tasakaalustamist on võimalik saavutada ka teiste antikoagulantsete valkudega, näiteks antitrombiiniga. Kui antitrombiini on vähem, on korrelatsiooni (hüübimise) potentsiaal suurem.
3. Tasakaalustavate ravimite kasu ja ohutus
Need uued raviviisid pakuvad mitmeid olulisi eeliseid patsientide vajaduste rahuldamisel:
- Lai Toimespekter: Need töötavad nii hemofiilia A kui ka hemofiilia B puhul.
- Inhibiitorite Puudumine: Ravi ei sõltu inhibiitoritest, kuna see ei ole seotud faktori VIII või IX puudulikkusega. Seetõttu toimib see hästi patsientidel, kellel on või ei ole inhibiitoreid.
- Mugav Manustamine: Mõningaid ravimeid manustatakse nahaaluse süstina pikkade intervallidega, mis on mugav ja lihtne.
- Kliiniline Kasu: On tõestatud, et need ravimeetodid parandavad verejooksu kontrolli ja elukvaliteeti ohutult.
Ohutuse kaalutlused
Kuigi uued ravimid on põnevad, on alati vaja hoolikalt kaaluda nende ohutust. Iga Euroopas litsentseeritud uus ravim peab olema ohutu, sest muidu ei saaks see müügilitsentsi. Kogu meditsiinikogukond peab tegema originaalset tööd, koguma andmeid iga uue ravimi kohta, et tagada patsientide ohutu ja tõhus ravi. Seepärast on vajalikud nii võimalikud uuringud kui ka seire, mida arstid eelistavad teha, et “kontrollida aadresse”.
Need uued ravimeetodid muudavad hemofiilia maastikku. Sessiooni lõpus väljendati usku, et kogukond on nende muutustega toimetulemiseks valmis ning igas uues muutuses peitub võimalus paranemiseks.
9. Tööstussümpoosion 4: „Uued horisondid VWD ravis“
9.1 Veritsemisest kuuluvustundeni: elamine von Willebrandi tõvega – Baiba Ziemele
Baiba Ziemele, patsiendiekspert Lätist, jagas oma enam kui 40 aasta pikkust isiklikku ja puudutavat lugu VWD-ga elamisest. Ta vabandas, et ei saanud terviseprobleemide tõttu isiklikult kohal olla, märkides, et see oli esimene kord peaaegu 20 aasta jooksul, mil ta hemofiiliakonverentsil osalemata jättis. Ta rõhutas, et kuigi VWD on väga keeruline haigus, ei tohi see olla põhjus, miks inimestele ei võimaldata vajalikku ravi.
Diagnoosi teekond ja fragmentaarne ravi
Ziemele, kes on üks neljast VWD-ga inimesest oma perekonnas (suurema tõenäosusega on peres haigus laiemalt levinud), diagnoositi alles seitsmeaastaselt, olles kogenud juba palju tõsiseid sümptomeid, mis jäid ravimata. Täpne diagnoosimine oli pikk ja keeruline protsess, mis algas alles 2012. aastal, ning alles mõned aastad tagasi sai ta geneetilise testimise. Minevikus oli tal raskusi isegi valitsuse poolt pakutava kontsentraadi efektiivsuse tõestamisega, kuna see tema organismis ei toiminud, nõudes temalt arsti veenmist, et teha 2017. aastal väljakutsetest.
Sümptomite eiramine ja kriisid
Baiba Ziemele tõi esile, et VWD patsiente koheldakse sageli ebaõiglaselt. Talle on järjepidevalt öeldud, et tema sümptomid on kerged, isegi kui testitulemused kinnitasid vastupidist. Ta rõhutas, et kui VWF tase on alla 50% ja esinevad verejooksu sümptomid, peaks inimene saama VWD diagnoosi, ning alla 30% faktoritasemega patsiente peab alati klassifitseerima haigetena, kes vajavad hoolikat ravi. Tema enda sümptomite raskusastet kinnitas ISTH-BAT (Bleeding Assessment Tool), mille skoor (16–22) näitas väga tõsist raskusastet.
Lisaks igapäevastele raskustele on probleemiks ka meditsiinitöötajate hirm ja teadmatus. Ta kirjeldas hiljutist olukorda, kus haigla erakorralise meditsiini osakonna arst keeldus temaga seoses verejooksu kartusega hematoloogiga konsulteerimast ja kartis manustada faktorkontsentraati trombi tekke hirmus. Ta pidi pöörduma oma kogukonna sõprade poole, et ületada hirm faktori manustamise ees, mis päästis tema elu.
Ravi lõhe ja kogukonna tunde puudumine
Ziemele tõi välja, et hemofiilia ravi on arenenud 150 aasta jooksul, samas kui VWD ravi vajab samale tasemele jõudmiseks ilmselt veel 50 aastat. Hetkel on VWD ravivõimalused piiratud (mõned faktorkontsentraadid ja desmopressiin), ning isegi need valikud ei ole Euroopa Liidu riikides alati kättesaadavad.
Lõpetuseks rõhutas ta, et VWD patsientidel on neli peamist puudujääki: sümptomite ebapiisav tunnustamine; haiguse ebapiisav mõistmine (erinevad arvamused, kas haigus on tõsine või mitte); teabe puudumine ravi ja tulevaste ravivõimaluste kohta; ning kuulumistunde puudumine, kuna kogukond keskendub sageli hemofiiliale. Andmete kogumine (WFH andmebaasidesse) on tema sõnul kriitilise tähtsusega eestkostetööks.
9.2 Süstemaatiline kliiniline lähenemine veritsushäiretega naiste ja tüdrukute tuvastamiseks – Cedric Hermans
Professor Giancarlo Castaman keskendus VWD diagnoosimise keerukusele ja vajadusele minna kaugemale pelgalt Von Willebrandi faktori (VWF) taseme mõõtmisest. Ta kordas VWF kahte peamist funktsiooni: hemostaasis (soodustab vereliistakute adhesiooni ja koostööd fibrinogeeniga) ja Faktori VIII kaitsmine (stabiliseerib FVIII-t vereringes, kaitstes seda lagunemise eest).
Diagnoosi kriteeriumid ja hindamisvahendid
VWD diagnoosimiseks peavad olema täidetud kolm kriteeriumi: verejooksuhäire olemasolu pereliikmetel, VWF defekti (kvantitatiivne või kvalitatiivne) tõestamine laboratoorsete testidega ja kliiniline manifestatsioon. Kliinilised sümptomid on enamasti limaskestade verejooksud (mukokutaansed), naistel fertiilses eas on oluline sümptom menorraagia (raske menstruatsioon).
Kuna terved inimesed võivad samuti teatada mõningatest verejooksuepisoodidest, rõhutas Castaman objektiivse mõõtmise olulisust. Selleks kasutatakse ISTH Bleeding Assessment Tool’i (BAT). BAT on eriti väärtuslik negatiivse prognoosi vahendina: negatiivne BAT skoor välistab olulise verejooksuhäire.
Laboratoorsed testid ja klassifikatsioon
Pärast positiivset BAT tulemust viiakse läbi esmase taseme sõeluuring, mis hõlmab VWF kontsentratsiooni (antigeen), VWF aktiivsust ja Faktori VIII aktiivsust. FVIII tase on kirurgiliste verejooksude või raske fenotüübi oluline ennustaja.
VWD jagatakse kahte põhigruppi: kvantitatiivne puudulikkus (Tüüp 1 osaline, Tüüp 3 raske) ja kvalitatiivsed kõrvalekalded (Tüüp 2). Hiljutiste juhiste kohaselt loetakse Tüüp 1 kindlaks diagnoosiks (definite diagnosis), kui VWF tase on alla 30 RÜ/dl. Diagnoosi kahtlustatakse, kui tase on alla 50 RÜ/dl ja esineb verejooksu fenotüüp. Tüüp 1 moodustab umbes 70% juhtudest, samas kui Tüüp 3 on haruldane (2–3%). Verejooksu raskusaste suureneb tüübist 1 tüübini 3.
Geneetiline analüüs
Geneetiline testimine (nt NGS abil) on muutunud lihtsamaks, kuigi on kättesaadav vaid vähestes keskustes. Geneetiline analüüs on vajalik keeruliste olukordade puhul, nagu näiteks raseduse nõustamine, Tüüp 2N ja Tüüp 3 diferentseerimine, ning perekonnasisene fenotüübi varieeruvus. Castaman rõhutas, et VWD on enamasti autosoomne dominantne häire, mis tähendab, et perekonnaliikmeid tuleb uurida.
9.3 Kultuurilised küsimused diagnoosimisel ja ravis – Rezan Abdul-Kadir
Professor Cihan Ay, olles sessiooni juhataja, keskendus isikupärastatud ravi vajadusele ja uutele arenevatele teraapiatele, märkides, et VWD patsientidel on oluliselt vähenenud elukvaliteet. Ta nentis, et VWD valdkonna eksperdid on hemofiilia ravi arengute suhtes “kadedad”.
Juhiste lõhe ja profülaktika
Ay tõi esile, et kuigi verejooksuhäiretega patsientide jaoks on sarnased tervisetulemuste mõõdikud olulised (nt elukvaliteet), on VWD juhised isikupärastatud ravi osas puudulikud. Ameerika Seltside (ASH) koostatud juhistes leiti termin “isikupärastatud ravi” vaid ühel korral ja “individualiseeritud ravi” vaid kirurgiliste protseduuride kontekstis.
Juhised soovitavad profülaktikat patsientidele, kellel on rasked ja sagedased verejooksud, kuid see soovitus on tingimuslik, kuna tõenduspõhise teabe kindlus on madal. Praegu on ravivõimalusteks faktorkontsentraadid ja desmopressiin (DDAVP), mida manustatakse intravenoosselt või subkutaanselt, kuna ninakaudne manustamine pole enam saadaval.
Arenevad ravivõimalused
Ay tutvustas mitmeid paljutõotavaid uusi ravistrateegiaid, rõhutades VWD heterogeensust ja vajadust isikupärastatud lähenemise järele:
- Faktor VIII Mimikad: Emitsizumab, mida kasutatakse hemofiilia A raviks, on potentsiaalne ka VWD patsientidele, eriti raske Tüüp 3 hemofiiliaga inimestele, kellel on ka FVIII aktiivsus vähenenud. Arendamisel on ka uued FVIII mimikad (nt SPN114, HAV8), millel on pikem poolväärtusaeg (nädalane/kuine manustamine) ja kõrgem potents.
- Targeting tüüp 2B VWD: on kvalitatiivne defekt, mida iseloomustab trombotsüütide arvu langus ja kõrge molekulmassiga VWF multimeeride kadu. Uuritud on molekuli nimega BD200 (nüüd RanaCaplan), mis on aptameer ja sihib VWF A1 domeeni. See molekul takistab VWF interaktsiooni trombotsüütidega, tõstes trombotsüütide arvu ja taastades VWF kõrge molekulmassiga multimeerid. Kliinilises uuringus läbisid kaks Tüüp 2B patsienti edukalt suure ortopeedilise operatsiooni, kasutades seda ühendit.
- Antikoagulatsiooni sihtimine: Uus suund on hemostaasi tasakaalustamine antikoagulantide inhibeerimise teel. Näiteks monoklonaalne antikeha VG-A0038, mis sihib proteiini, on jõudmas faasi 3 uuringutesse.
- Poolväärtusaja pikendamine: Prekliinilises uuringus VWD Tüüp 1 hiiremudelil arendati nanokehi, mis seonduvad VWF-ga ja albumiiniga, pikendades seeläbi kehasisese VWF poolväärtusaega.
Ay lõpetas, märkides, et VWD on heterogeenne haigus, mis väärib isikupärastatud ravi, kuigi meditsiinikogukond pole selle saavutamiseni veel jõudnud. Ta väljendas lootust, et VWD patsiendid saavad kasu hemofiilia valdkonna arengutest, sealhulgas geeniteraapia potentsiaalist.
10. 6. sessioon – Uued piirid hemofiilia geenteraapias
10.1 Reaalsed andmed kliinilistest uuringutest – Wolfgang Miesbach
Wolfgang Miesbach keskendus oma ettekandes reaalse elu andmete kogumise olulisusele ja meetoditele geeniteraapia valdkonnas. Ta nentis, et RWD valdkond on keeruline ja informatsioon võib olla piiratud.
Andmekogumise strateegiad
Miesbach tutvustas mitmeid andmekogumise infrastruktuure ja algatusi:
- Euroopa Hemofiilia Konsortsiumi (EHC) andmebaas: See on prospektiivne, observatsiooniline ja pikaajaline uuring, mis on loodud koos teadlaste, farmaatsiatööstuse ja patsientidega, et koguda andmeid nii kliiniliste uuringute kui ka kommertslikult kättesaadavate toodete kohta. See on kõige olulisem vahend ohutuse kohta. Andmebaas sisaldab teavet geeniteraapia uuringute kohta ja on vabalt kättesaadav EHC veebilehel. Seda uuendatakse iga 30 kuu tagant ning see pakub ajakohastatud teavet geeniteraapia valdkonnas toimuvast.
- Geeniteraapia uuringute küsimustik: See on tervishoiutöötajate poolt koostatud küsimustik, mis võtab täitmiseks umbes 15–20 minutit ja mis on kättesaadav erinevates keeltes. See keskendub spetsiifilistele küsimustele ravitulemuste, ohutuse ja teatud tasakaalustatud ravimeetodite kohta.
- Saksa, Austria ja Šveitsi (DACH) geeniteraapia tööriist: See on käsitsi andmekogumise ja analüüsi süsteem, mis keskendub peamiselt immunosupressioonile ja kõrvaltoimetele. See pakub neljanda faasi uuringutele sarnaseid andmeid.
Andmed kommertslikult kättesaadava geeniteraapia kohta
Kuna geeniteraapia tooted on nüüd kommertslikult kättesaadavad, on vaja koguda andmeid ka patsientide kohta väljaspool kliinilisi uuringuid. EHC-l on olemas protokoll, mille alusel küsitakse patsientide andmeid. Andmete kogumise piiratud arv küsimusi (nt vanus, ravimi nimi, infusiooni kuupäev) valiti selleks, et vältida tervishoiutöötajate ülekoormamist.
- Raviandmed: Seni (enne septembrit 2023) oli 16 keskuses viiest riigist dokumenteeritud 44 patsienti, keda raviti geeniteraapiaga. See annab vähemalt osalise ülevaate, kuigi ettevõtete andmetel on kommertslikult ravitud 70–100 patsienti.
• Tooted: Rakendatud on 27 ravi Octaviaga ja 17 ravi Hemgenixiga. - Efektiivsus ja ohutus: Uuringuandmed näitavad, et pärast ravi lõpetati profülaktiline ravi väga lühikese aja jooksul. Samuti näitavad süsteemsed ülevaated suurepärast efektiivsust kuni kaks aastat pärast geeniteraapiat. Immuunsupressiooni osas on viimati ravitud patsientidel immunosupressiooni määr oluliselt madalam (umbes 40%), võrreldes faasi 3 uuringute 90%-ga. See viitab sellele, et arstid on immunosuppressiooni manustamisel ettevaatlikumad.
10.2 Seni vastuvõetud hüvitamismudelid – Gaetan Duport
Gaetan Duport, kes tegutseb aktiivselt Prantsuse kogukonnas, käsitles uute geeniteraapiate (nagu Zynteglo, Hemgenix ja Luxturna) kättesaadavust Euroopas, rõhutades, et ravile ligipääs on endiselt keeruline. Peamine põhjus on hind ja vajadus saavutada kokkulepe tootja ja valitsuse vahel.
Hindamise alused ja kvaliteedi mõõtmine
Ravi hinna üle läbirääkimiste pidamiseks kasutavad valitsused Tervishoiutehnoloogia Hindamise (Health Technology Assessment, HTA) aruandeid. HTA-d hindavad ravi väärtust, vastates küsimusele, kas ravi on väärt seda hinda, mida selle eest küsitakse (väärtuspõhine hindamine). Tervishoiuökonoomikas kasutatakse ravi väärtuse hindamiseks spetsiifilist mõõdikut – QUALY (Quality-Adjusted Life Years), mis mõõdab, kui kaua ja kui hästi inimene elab.
Läbirääkimiste elemendid ja riskijagamine
Läbirääkimised ei puuduta ainult hinda, vaid ka tootja ja valitsuse (maksja) vahelist julgeolekut. Maksja kaalutlused hõlmavad regulatsioone, ravi tõelist varieeruvat kasu ja eelarvet. Tootja jaoks on oluline väline võrdlushind, mis on avalik hind, kuid mis ei ole tegelik hind, mida valitsus maksab.
Kuna geeniteraapiad on ette nähtud pikaks ajaks, on oluline jagada riske tootja ja maksja vahel. See motiveerib innovatsiooni ja vähendab ebakindlust ravi pikaajalise efektiivsuse osas (nt kas ravi kestab 5 või 10 aastat). Duport rõhutas, et andmete kogumine on ebakindluse vähendamisel maksja vaatenurgast võtmetähtsusega.
Tulemuspõhised lepingud
Geeniteraapiate puhul on Euroopas hakatud kasutama tulemuspõhiseid lepinguid (outcome-based contracts). See tähendab, et maksmine on seotud kliinilise tulemusega. Valitsused maksavad ainult siis, kui ravi töötab. Näiteks Hispaanias on otsustatud maksta ainult siis, kui Faktori IX tase on aasta pärast ravi viis protsenti või rohkem.
Duport tõi välja ka tekkivaid eetilisi ja praktilisi probleeme. Näiteks, mis juhtub, kui patsient kaob jälgimisest? Kas valitsus peaks maksma? Ja mis juhtub, kui patsient sureb? Ta soovitas, et riigid, kes ei saa endale lubada kõrgeid hindasid, võiksid kaaluda regulaarseid sandkarpe – alternatiivseid regulatiivseid raamistikke, mis lubaksid läbirääkimisi teistsuguste reeglite alusel.
Patsiendiorganisatsioonide aktiivsus on Duport’i sõnul ülioluline HTA protsesside mõistmisel ja patsiendikogemuse kohta andmete esitamisel.
10.3 Uued lähenemisviisid, mis erinevad AAV-vektoritest – Paul Batty
Dr Paul Batty käsitles geeniteraapia uusi lähenemisviise, mis erinevad traditsioonilistest adenoviirus-seotud vektoritest (AAV). Ta rõhutas, et AAV-l on piirangud, näiteks see, et paljudel patsientidel on juba AAV vastu antikehad, mis muudab AAV-l põhinevad programmid võimatuks. See eeldab alternatiivseid ravimeetodeid.
Geeniteraapia põhimõtted
Geeniteraapia põhiprintsiip on geneetilise materjali kasutamine haiguste raviks või ennetamiseks. Kuna DNA on iseenesest habras, vajab see sihtrakku toimetamiseks “sõidukit”. AAV on mitte-integreeriv viis, samas kui teised, uuemad lähenemisviisid tuginevad integreerimisele.
Uued (Mitte-AAV) lähenemisviisid
Batty tutvustas kolme peamist alternatiivset lähenemisviisi:
- Geeni Redigeerimine (Gene Editing – CRISPR/Cas9):
- See lähenemisviis kasutab mitteviiruslikku infusiooni, mis sisaldab juhtjärjestust (guide sequence) ja ensüümi, mis sihib konkreetset kohta DNA-s. Sel juhul on sihtmärk albumiini geen. See protsess võimaldab geenijärjestuse otsest sisestamist soovitud kohta.
- Eelis: potentsiaal pikaajaliseks ja püsivaks ekspressiooniks. See meetod võib laiendada geeniteraapiat ka populatsioonidele, kellel on AAV vastased antikehad. Andmed näitasid stabiilset faktori ekspressiooni.
- Vereloome tüvirakkude geeniteraapia:
- See on mitmeetapiline protsess, mis sarnaneb luuüdi siirdamisega. Patisendi rakud eemaldatakse, transdukteeritakse (geenimaterjali viiakse rakku) ja viiakse uuesti kehasse tagasi, kus nad integreeruvad peremeesrakkude DNA-sse.
- Eelised: Kuna protsess viiakse läbi ex vivo (väljaspool keha), on sellel madalam immuunsüsteemi vastuse tõenäosus ja see ei tekita probleeme maksa toksilisusega. See lubab pikaajalist ekspressiooni. Tüvirakkude siirdamine on paljudes hemofiiliakeskustes juba tuttav protseduur.
- Puudused: Siiski on olemas riske, mis on seotud konditsioneerimisega – kemoteraapia ja immunosupressiooni kasutamisega, mis vähendab immuunsüsteemi, suurendades infektsioonide ja limaskestade põletiku riski. Uuringud (nt Beaumont uuring) on näidanud edukaid tulemusi, kus patsiendid saavutasid faktoritasemed vahemikus 2% kuni 20%.
- B-rakkudel põhinev lähenemisviis:
- See on uus lähenemisviis, kus Faktor IX ekspresseeritakse B-rakkude poolt, mis on juhuslikult sekreteerivad rakud. See ei nõua konditsioneerimist ega sihi maksa.
- Eelised: See ei nõua konditsioneerimist, vältides sellega seotud kõrvalmõjusid. Kuna geeniteraapia toimub väljaspool keha, ei ole ka immuunsüsteemi probleeme. Samuti on sellel lähenemisviisil potentsiaal kordusraviks.
Batty lõpetas rõhutades, et kuigi AAV-l põhinev geeniteraapia on muutumas kättesaadavamaks, on piirangud ja küsimused. Uued AAV-st erinevad tehnoloogiad (nagu geeni redigeerimine ja tüvirakkude/B-rakkude teraapia) pakuvad olulisi tulevasi lahendusi, mis võivad ravida ka neid patsiente, kellele traditsioonilised AAV-vektorid ei sobi.
12. 8. sessioon – Ravi psühhosotsiaalse mõju navigeerimine
12.1 Suuõõne tervis: ühiskondlik koorem? – Alison Dougall
Alison Dougall käsitles suutervise alahinnatud ühiskondlikku koormust, rõhutades, et suu põletik võib avaldada tohutut mõju üldtervisele, sealhulgas südamehaiguste, dementsuse, enneaegse sünnituse ja kopsuhaiguste arengule.
Globaalne koormus ja kulud
Suutervise probleemide ulatus on šokeeriv: umbes kaks ja pool miljonit inimest üle maailma kannatab ravimata hambakaariese all, miljardil inimesel on raske igemehaigus, kus luu on kokku kuivanud ning hambad on lahti ja liikuvad, ning 380 000-l on suuvähk. Kuigi neid haigusi saab varajases staadiumis väga lihtsalt ennetada ja ravida, kasvab probleem pigem suuremaks. Suutervishoid maksab ülemaailmselt 380 miljardit, kuid tervishoiusüsteem ebaõnnestub, sest enamikul juhtudel peab patsient ravi eest ise maksma. See tähendab, et paljud ei saa endale hambaarsti külastamist lubada, mistõttu varajane ravi viibib ja probleemid muutuvad järjest keerulisemaks ja kallimaks.
Miks on suutervis oluline?
Terve suu väärtus ulatub kaugemale lihtsast iluvaatlusest. Dougall tõi esile, et hambaid on vaja tervisliku toitumise närimiseks. Inimesed, kellel ei ole häid hambaid, kalduvad kiiresti töödeldud, ebatervislikele, soolapõhistele dieetidele. Lisaks on elamine vaba valust ja infektsioonist ülioluline. Hambavalu on talumatu, ulatudes sageli skaalal 9 või 10-ni 10-st. Halb suutervis kahjustab ka suhteid ja intiimsust ning põhjustab tuhandete tundide kaotust töölt ja koolist. Visuaalselt on suutervis seotud enesekindluse ja enesehinnanguga; kehva suutervise tõttu on inimesi ebaõiglaselt hinnatud ja neil on näiteks raskem teatud töökohti saada.
Verejooksuhäiretega patsientide eestkostetöö
Verejooksuhäiretega (BD) inimestel ei ole suurenenud eelsoodumust igemehaigustele – terved igemed ei veritse. Siiski on sellel populatsioonil spetsiifilised takistused suutervise säilitamisel. Paljudel on kohutav hirm hambaarsti ees (dental fear). See hirm on tingitud nii hambaarsti külastamise intiimsusest kui ka varasematest isiklikest või tunnistatud kogemustest veritsemisega. Dougall kirjeldas näidet, kus patsient oli lapsepõlves näinud, kuidas tema isal oli verejooks, mis kestis päevi või nädalaid. Hambaarstid ise võivad keelduda BD patsientide ravimisest teadmiste puudumise või hirmu tõttu.
Müütide kummutamine ja elukvaliteet
Dougall jagas juhtumi VWD Tüüp 2B patsiendiga, kes uskus, et tema meditsiiniline seisund põhjustab veritsust ja et ta peab sellega elama. Talle soovitati isegi veritsuse kontrollimiseks suitsetada. Ta oli vältinud hammaste harjamist, kartes igemeid traumeerida. See valearusaam on laialt levinud. Patsiendi elukvaliteet oli äärmiselt madal – ta oli liiga häbelik intiimsuheteks ja pidi igapäevaselt vahetama padjapüüre ning voodipesu. “Nägemine on uskumine” meetodi abil näidati patsiendile, et veritsuse põhjuseks oli hoopis hambakatt ja põletik. Pärast igapäevast põhjalikku harjamist ja hambaniidi kasutamist lakkas igemete veritsemine kolme kuu jooksul ja tema elukvaliteet paranes drastiliselt. Dougall lõpetas sõnumiga, et NMO-d ja EHC peavad aitama kummutada müüte ja julgustama inimesi hambaarsti külastama, et ennetada probleeme varakult.
12.2 Uute ravimeetoditega seotud vaimse tervise väljakutsed – Christina Burgess
Christina Burgess keskendus uute, eriti geeniteraapial põhinevate raviviiside psühhosotsiaalsele mõjule, rõhutades, et vaimse tervise tugi on sama oluline kui füüsiline ravi. Ta nõustus Alison Dougalliga, et suutervis mõjutab igakülgselt vaimset tervist ja suhteid.
Positiivsed muutused ja tugivajadus
Burgess rõhutas kohe alguses, et uued ravimeetodid on transformatiivsed ja pakuvad uskumatult positiivseid eeliseid. Kuid nagu iga uue olukorraga, võivad ka need tekitada hirmu ja ärevust. Tema ettekande peamine sõnum oli see, et kõik, kes alustavad geeniteraapiat või muid uusi keerulisi ravimeetodeid, peavad saama juurdepääsu ekspert psühholoogilisele toetusele.
Patsientide teekond ja psühholoogilised väljakutsed
Geeniteraapia eelne faas hõlmab palju kaalutlemist, motivatsiooni ja ootusi. Tekib küsimus, miks peaks muutma praegust, toimivat ravi. Patsiendid elavad ootuses (anticipation), mis võib olla hirmutav, kuna nad on sageli esimesed ja on teadlikud potentsiaalsetest kõrvalmõjudest.
Ravi käigus või pärast seda ilmnev oluline psühholoogiline probleem on identiteedi muutus. Patsiendid, kes on pikka aega identifitseerinud end hemofiilia kogukonna liikmetena või “haigetena”, tunnevad end nüüd “normaalsete inimestena”, mis tekitab võõra ja kummalise tunde. Lisaks kardetakse, et füüsiline probleem (nt steroidsravi vajadus maksaensüümide tõusu tõttu) võib peegeldada ravi ebaõnnestumist.
Mõju perekonnale ja inimestele
Burgess rõhutas, et verejooksuhäire ei mõjuta kunagi ainult patsienti ennast; see mõjutab ka nende vanemaid, partnereid, õdesid-vendi ja lapsi. Partnerid ja vanemad, kelle identiteet on seotud lapse hooldamisega, võivad tunda oma eesmärgi kadumist. Ka tütred, kes võivad olla kandjad, seisavad silmitsi väljakutsetega ja vajavad teadmisi oma tervisest kogu elu jooksul. Seetõttu peab psühhosotsiaalne tugi laienema ka neile, kes on eemalt seotud.
Unustatud rühm: ebasobivad patsiendid
On äärmiselt oluline toetada ka neid patsiente, kes uute ravivõimaluste jaoks ei sobi (nt lapsed, inhibiitoritega patsiendid, vanemate AAV-antikehadega patsiendid). Nende vaimset tervist mõjutab teadmine, et teised saavad elumuutvaid ravimeid, samas kui nemad jäävad ilma.
Burgess lõpetas, lugedes ette vana luuletuse, mis tabas uue ravi ees seisva kogukonna ambivalentsust: lootus vabadusele ja mugavusele, samal ajal kui tundub kurbust ja viha, et paljudel puudub endiselt juurdepääs nendele „inimõigustele“.
12.3 Kangelastest tavalisteks inimesteks – Miguel Crato
Robert Sidonio alustas ettekannet, kaitstes veendunult seisukohta, miks faktorravi, eelkõige faktor 9 asendus, peaks olema hemofiilia B puhul optimaalne teraapia.
Ta tõi esile faktor 9 unikaalsed omadused võrreldes faktor 8-ga, märkides, et faktor 9 on ensüüm ja sellel on oluliselt väiksem molekulmass ning kõrgem kontsentratsioon plasmas. Samuti on faktor 9-l laialdane ja oluline jaotus mitmetes kudedes, mitte ainult plasmas, sidudes end näiteks tüüp 4 kollageeniga veresoone seintes.
Sidonio rõhutas, et kuigi on olemas erinevaid faktor 9 tooteid (nii modifitseeritud kui ka modifitseerimata), on nende kõigi puhul näidatud sarnast hemostaatilist efektiivsust ja väga madalat verejooksude esinemissagedust (ABR(Annual Bleed Rate) nullist kolmeni), kui neid kasutatakse õiges doosis. Ta lükkas ümber varasemad mured N9GP-ga seotud toksilisuse osas ajus, öeldes, et need pole lastel kinnitust leidnud. Sidonio rõhutas ka faktorravi pikka ja head ohutusprofiili, viidates madalale tromboosiriskile, eriti noorematel patsientidel. Ta seisis vastu ideele, et geeniteraapia “ravib kõik” ja teised ravimeetodid on vaid palliatiivsed, kinnitades, et faktorravimid on ohutud, laialdaselt kättesaadavad ja jäävad kasutusse.
13. Tööstuse sümpoosion 6: „Väljakutsuvad väärarusaamad patsientide teekonnad ja VWD hoolduse tulevik”
1. Sümpoosioni kontekst ja eesmärk
Sümpoosion keskendus VWD-ga inimeste vajadustele (Von Willebrand Disease). Juhataja Manon Degenaar Dujardin rõhutas, et edu saavutamine algab kuulamisest ja VWD-ga inimeste igapäevaste reaalsuste mõistmisest. Kohal olid patsiendid (Sunny ja teine esineja, keda mainiti kui Joe) ja arstid (hematoloog Carolyn ja õde/praktik).
Peamine probleem on see, et patsientidele öeldakse liiga sageli, et nende sümptomid on minimaalsed või neid peetakse normaalseks. Sümptomeid eiratakse ja minimeeritakse, kuigi need võivad olla sagedased ja invasiivsed. Tekib tunne, et ravi – näiteks profülaktika saamine – tuleb “välja teenida” piisava verejooksuga. See näitab kiiruse puudumist nii diagnoosimisel, ravil kui ka uuringutes.
VWD ravi on hemofiilia omast oluliselt maas: kui hemofiilia jaoks on tänapäeval umbes 39 erinevat ravi, siis VWD jaoks on neid vaid kuus, mis on olnud kasutusel aastakümneid. Patsientide ühine pettumus on ka sümptomite alahindamine, mis põhjustab isolatsiooni, mõjutades negatiivselt vaimset tervist. Inimesed tunnevad end vaigistatuna ja kardavad end ise tsenseerida.
2. Patsiendikogemused: viivitused, trauma ja nähtamatus
Panelistid Sunny (Tüüp 3 VWD) ja Joe jagasid oma isiklikke lugusid. Nad leidsid, et hoolimata erinevatest tüüpidest ja soost, on nende kogemused ja takistused väga sarnased.
Diagnoosimise pikk teekond: Joe diagnoositi alles 37-aastaselt, kuigi ta kannatas kogu elu verevalumite all. Tema meditsiinilises kaardis oli aastaid tiitel „tundmatu veritsushäire“. Tema diagnoos tuli alles pärast katastroofilist verejooksu, mille põhjustas keisrilõige ja poja sünnitus. Ta kaotas 15 liitrit verd, mis oli haiglas enneolematu juhtum, mille tulemusel viidi läbi erakorraline hüsterektoomia. Tema elu päästis see, et operatsiooni ajal oli kohal hematoloog. Pärast seda küsis ta endalt, miks ta pidi kannatama katastroofilise verejooksu, et teda hakataks tõsiselt võtma.
Nähtamatuks jäämine: Sunny tõi välja, et paljud VWD-ga inimesed tunnevad end nähtamatu, kuuldamatu ja alaravituna. Üks patsient kahtlustas, et ta on hüpohondrik, kuni arvas, et talle tehakse operatsioon Londonis, kus kirurgid ei teadnud tema veritsushäirest. Kogu pere (õed-vennad, lapsed) tuli pärast tema diagnoosimist testida. Joe rõhutas, et isegi VWD „kergeima“ tüübi (Tüüp 1) patsientidel võib olla raskeid tagajärgi, näiteks suur ajuverejooks. See rõhutab vajadust ravida inimesi nende sümptomite ja ajaloo, mitte vaid labortulemuste alusel.
Vaimne Trauma: Patsiendid tunnevad end gaasivalgustatuna ja alahinnatuna. On vaikne trauma õppida elama sümptomite ümber, mitte neid ravima. Sümptomite eitamine viib enesekahtluseni ja õõnestab enesekindlust. VWD “varastab aega” ja unistusi.
3. Diagnoosimise takistused tervishoiutöötaja perspektiivist
Hematoloog Carolyn ja Manon Degenaar Dujardin arutlesid diagnoosi saamise peamiste takistuste üle:
- Väärarusaam haigusest: Ühiskond ja isegi mitte-eksperdid tervishoius tajuvad VWD-d kui kerget haigust.
- Ebaefektiivne Küsimuste Esitamine: Tervishoiutöötajad ei esita alati õigeid küsimusi. Küsimused ei tohiks piirduda vaid verejooksu episoodidega, vaid tuleks küsida ka igapäevaelus tehtud kohanduste ja kompensatsioonide kohta (nt tööl või koolis). See aitaks luua täpsema pildi.
- Lai teadmiste puudumine: Patsiendid käivad erinevate mitte-ekspertide juures (perearst, hambaarst), kellel puudub VWD kohta piisav teadlikkus.
- Laste ebakindlus: Varasemate verevalumite tõttu on endiselt sagedane laste kuritarvitamises süüdistamine, kuigi teadlikkus on suurenenud.
Naiste eriväljakutsed
Naistel on VWD diagnoosiga seotud täiendavad väljakutsed ja viivitused. Kuigi menstruaalverejooks (menstruaalmeedia) on peaaegu kõigil VWD-ga naistel, saab neist vaid väike osa tegelikult testitud. Diagnoosimine naistel võtab kauem aega – mõned uuringud näitavad viivitusi kuni kuus aastat. See pikenemine püsib isegi siis, kui võetakse arvesse soospetsiifilisi sümptomeid. Oluline on alustada tüdrukute harimist menstruaaltsükli osas juba varakult (7–9-aastaselt) ning pakkuda ravi (nt hormoonravi või muud lahendused).
4. Tuleviku visioon ja ühine vastutus
Patsiendid ja arstid rõhutasid, et muutuse saavutamiseks on vajalikud konkreetsed meetmed.
Tuleviku tegevused:
- Haridus ja Ausus: Haridus on kõige võimsam relv. Patsiendid peavad olema ausad oma sümptomitega ja mitte neid varjama, sest arstid saavad abi pakkuda vaid siis, kui nad teavad täit pilti.
- Kättesaadavus ja Kuulamine: Tervishoiutöötajad peavad olema kättesaadavad ja kuulama patsiente, mitte minimeerima nende sümptomeid.
- Ootuste Tõstmine: Arvestades arenenud meditsiinisüsteeme (nt kõrge sissetulekuga riigid), tuleb VWD patsientide raviootusi oluliselt tõsta, sest VWD on jäänud teiste verejooksuhäiretega võrreldes liiga kaugele maha.
- Proaktiivne Hoolduse Edendamine: Tuleb tunnustada ja käsitleda diagnostika- ja ravipuudujääke, edendada proaktiivset multidistsiplinaarset hooldust ja innovatsiooni ning tagada ravi õiglus.
- Ühine Vastutus: Muutuse toomine on ühine vastutus, mis lasub nii arstidel, õdedel, farmaatsiaettevõtetel, poliitikakujundajatel kui ka patsientidel endil. Iga vestlus ja tegevus on oluline.
14. Ülevaade WFH eestkostetööst, ravijuhistest ja globaalsest seirest
Sessiooni oluline osa keskendus edule, mis saavutati Maailma Terviseorganisatsiooni (WHO) PõhiRavimite Loendi (EML) uuendamisel ja selle viimisel vastavusse kaasaegsete kliiniliste standarditega. Eestkostetöö algas umbes kaks aastat enne sümpoosioni, kuna 2023. aasta loendisse lisati krüopretsipitaat hemofiilia ja Von Willebrandi tõve raviks. Verejooksuhäiretega kogukond, sealhulgas Euroopa Hemofiilia Konsortsium (EHC), pidas seda ebarahuldavaks ja potentsiaalselt ohtlikuks regressiks.
1. WHO Põhi Ravimite Loendi (EML) uuendamine: eestkostetöö edu
WFH asus tegelema ulatusliku eestkostetööga, kaasates eksperte ja toetuskirju paljudelt teaduslikelt ja patsiendiorganisatsioonidelt. Nende peamised taotlused WHO-le olid järgmised: lisada loendisse uued ja kaasaegsed ravimid; viia plasmapõhised kontsentraadid (mis on patogeenidega töödeldud ja mittetöödeldud) täiendavast nimekirjast põhinimekirja; ning eemaldada krüopretsipitaat ja faktori IX kompleks.
Saavutatud Muudatused
Kogukonna üllatuseks ja heameeleks võeti enamik taotlusi arvesse. Olulisemad muudatused olid:
- Uued ravimid lisati loendisse: See hõlmab emitsizumabi (mis on soovitatav nii inhibiitoritega kui ka ilma patsientidele) ja rekombinantseid kontsentraate, mida varem nimekirjas üldse polnud.
- Varem kasutatavad ravimeetodid eemaldati verejooksuhäirete ravist: Krüopretsipitaat ja faktori IX kompleks eemaldati Hemofiilia ja Von Willebrandi tõve ravinäidustusena. Krüopretsipitaat jääb loendisse, kuid on näidustatud ainult verepankade komponendina ja muuks haiglakasutuseks.
- Ohutuse ja efektiivsuse vastavus: Need muudatused viisid WHO EML-i paremini kooskõlla kliiniliste ohutus- ja efektiivsusjuhistega.
- Sessioon rõhutas kogukonna ühise töö jõudu, mis suutis mõjutada keerulist ja bürokraatlikku protsessi, tagades, et EML-i sisu on parem. WFH plaanib tulevikus rakendada uusi taotlusi (nt Von Willebrandi faktori lisamine) ning uurida, kuidas riiklikud hüvitamise nimekirjad on kooskõlas WHO EML-iga, et pakkuda paremat sihipärast eestkostetööd kohalikul tasandil.
2. WFH Ravijuhiste Arendamine ja Ühine Otsustamine
Sessioon andis ülevaate WFH pidevast tööst ravijuhiste ajakohastamisel, mis avaldati viimati 2020. aastal. Uute ravimeetodite kiire arengu tõttu on WFH asunud muutma ja uuendama juhiste peatükke vastavalt vajadusele, et vältida kogu dokumendi massiivset ümberkirjutamist, mis on ajamahukas ja kulukas.
Geneetika ja ravijuhised
WFH on avaldanud uued juhised hemofiilia A geenteraapia haldamise kohta. Need on väga põhjalikud ja sisaldavad soovitusi koha ettevalmistamise, teadliku otsustusprotsessi, sobivuse sõeluuringu ning infusioonieelse ja -järgse jälgimise kohta. Järgmiseks plaanitakse uuendada 2020. aasta juhiste 5. ja 6. peatükki (ravi ja profülaktika), mis liidetakse, kuna profülaktika on nüüd hemofiilia standardne ravi.
Ühise Otsustamise (SDM) tööriist
WFH tutvustas oma ühist otsustamist (Shared Decision Making, SDM) toetavat digitaalset tööriista, mis käivitati kaks aastat tagasi ja mida on pidevalt uuendatud, et kajastada uusi ravimeetodeid (nt Altuvio ja kolm tasakaalustajat). Tööriist aitab patsientidel reflekteerida oma ravieelistuste ja väärtuste üle ning viia patsiente ja tervishoiuteenuse osutajaid kokku arutelu pidamiseks. Tööriist on saadaval mitmes keeles (sh inglise, prantsuse, hispaania, jaapani, saksa ja hollandi keeles) ning seda on kasutanud üle 18 000 aktiivse kasutaja 157 riigist.
SDM rakendamise parandamiseks kliinilises praktikas töötati ekspertide poolt välja 15 parima praktika soovitust. Need soovitused on kategoriseeritud vajalike materjalide/tööriistade, patsiendi omaduste ja toe, patsiendi ja tervishoiuteenuse osutaja suhte ning vajaliku infrastruktuuri alusel.
3. Ülemaailmne Seire ja Tulevikuplaanid (AGS)
WFH iga-aastane ülemaailmne uuring (Annual Global Survey, AGS) on oluline eestkostevahend, mida on läbi viidud 26 aastat ja mis kogub andmeid patsientide arvu, ravi kättesaadavuse ning demograafia kohta.
Tulemused ja Väljakutsed
2024. aastal vastas uuringule 135 riiki, mis oli WFH andmetel seni kõrgeim vastanute arv. Euroopa näitas suurt edu patsientide identifitseerimisel: 85% hemofiiliaga inimestest Euroopas on identifitseeritud, mis on märkimisväärne tõus võrreldes 10 aasta taguse 68%-ga.
Siiski on väljakutseks endiselt naiste ja tüdrukute identifitseerimine verejooksuhäiretega. Hemofiilia A diagnoosidest on naised/tüdrukud vaid 5,1% ja hemofiilia B puhul 9,1%, kuigi ootuspärane osakaal oleks 30%. Von Willebrandi tõve (VWD) puhul on naised 63% diagnoosidest, mis on oodatust kõrgem (50/50), peamiselt seotud menstruatsioonide ajal saadud diagnoosidega.
Sessiooni lõpus rõhutati, et WFH pakub tugi ja vahendeid, et aidata liikmesorganisatsioonidel AGS andmeid koguda ja kasutada eestkostevahendina kohalikul tasandil.
Tuleviku Kongressid ja Üritused
WFH teatas ka tulevastest sündmustest, sealhulgas:
- WFH maailmakongress Malaisias 2026. aastal.
- Ulatusliku ravi (Comprehensive Care) tippkohtumine Euroopas 2027. aastal.
Aitäh meie toetaja Sobile, kelle toetusega õnnestus osaleda EHC konverentsil!